Éter je to okysličená organická funkcia, to znamená, že má okrem uhlíka a vodíka aj chemický prvok kyslík. Táto funkcia má ako svoju hlavnú štrukturálnu charakteristiku prítomnosť dvoch organické radikály naviazaný na atóm kyslíka.
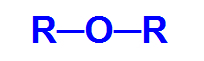
Všeobecný štruktúrny vzorec éteru
Uhlíkový reťazec éteru je teda heterogénny a môže mať dva rovnaké alebo rôzne radikály alkyl, typy radikálov, ktoré nemajú aromatickú štruktúru, alebo aryl, radikály, ktoré nemajú štruktúru aromatický.
Fyzikálne vlastnosti éteru
Pokiaľ ide o fyzický stav pri izbovej teplote: keď éter má vo svojom zložení štyri alebo viac atómov uhlíka, je kvapalný;
Pokiaľ ide o teplotu topenia a teplotu varu: v porovnaní s inými hromadnými organickými zlúčeninami približne molárne, majú teplotu topenia podobnú ako v prípade alkánov a nižšiu ako zvyšok zlúčenín organický;
Pokiaľ ide o hustotu: sú to zlúčeniny, ktoré majú malú hustotu v porovnaní s vodou;
Pokiaľ ide o interakčné sily: étery sú zložené s nízkou polaritou a navzájom interagujú prostredníctvom slabej trvalej dipólovej interakcie. S vodou a alkoholmi majú étery schopnosť interagovať pomocou vodíkových väzieb.
Pokiaľ ide o polarita: sú zlúčeniny, ktoré majú uhlovú geometriu, sú teda polárne.
Pokiaľ ide o organoleptické vlastnosti: sú to látky, ktoré vydávajú veľmi príjemný zápach, ale ich vdýchnutie môže spôsobiť závislosť.
Oficiálna nomenklatúra éteru
Menšia predpona kmeňa + kyslík + hlavná predpona kmeňa + infix + o
Na vykonávanie úradnej nomenklatúry a éter, Je rozhodujúce určiť, ktorý je váš hlavný ligand a ktorý je váš vedľajší ligand. Postupujte podľa nasledujúcich dvoch príkladov aplikácie pre toto pravidlo pomenovania:
1. príklad:
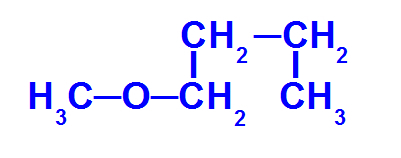
Štruktúrny vzorec éteru s menším počtom uhlíkov
Éter vyššie má nasledujúce radikály:
Metyl (CH3-);
Butyl (CH3-CH2-CH2-CH2-).
Na pomenovanie tejto zlúčeniny máme:
menšia radikálna predpona: Met
+
oxy
+
hlavná predpona kmeňa: ale
+
(pretože má iba jednotlivé odkazy)
+
O
Takže názov tohto éter bude to metoxybután.
2. príklad:
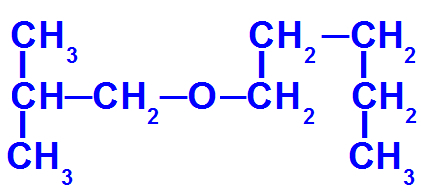
Štruktúrny vzorec éteru s väčším počtom uhlíkov
Tento éter má nasledujúce radikály:
Izobutyl [(CH3)2-CH-CH2-);
pentyl (CH3-CH2-CH2-CH2-CH2).
Aby sme to pomenovali, máme teda:
menšia radikálna predpona: izobut
+
oxy
+
hlavná predpona kmeňa: pent
+
(pretože má iba jednotlivé odkazy)
+
O
Teda názov éter bude to izobutoxypentán.
Obvyklá nomenklatúra éteru
Éter + názov radikálov (najjednoduchší a potom najkomplexnejší) + ico
alebo
Radikálne mená + éter
Nasledujte dva príklady použitia tohto pravidla pomenovania:
1. príklad:

Štruktúrny vzorec éteru, ktorý má štyri uhlíky
To éter predstavuje nasledujúce radikály:
Metyl (CH3);
Izopropyl (CH3-CH-CH3).
Takže pre túto zlúčeninu máme:
Éter
+
menší radikál: metyl
+
hlavná radikálna predpona: izopropyl
+
ich
Teda názov éter bude to metylizopropyléter alebo tiež metylizopropyléter.
2. príklad:

Štruktúrny vzorec éteru, ktorý má päť uhlíkov
Éter vyššie má nasledujúce radikály:
Etyl (CH3-CH2-);
Propyl (CH3-CH2-CH2-).
Na pomenovanie tejto zlúčeniny máme:
Éter
+
menší radikál: etyl
+
hlavná radikálna predpona: propyl
+
ich
Teda názov éter ide o etylpropyléter, ktorým môže byť tiež etylpropyléter.
Použitie éterov
Všeobecne sa étery používajú:
Ako inertné organické rozpúšťadlá, to znamená, že sa nezúčastňujú žiadnej reakcie;
Používa sa na extrakciu esencií, ako sú kvety, drevo atď.;
Používa sa pri extrakcii rôznych olejov a tukov.
Podľa mňa. Diogo Lopes
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eter.htm
