V štúdii o ideálne plyny vidíme, že plyn sa skladá z atómov a molekúl, ktoré sa pohybujú podľa zákonov stanovených kinematikou. V plyne sú jeho častice zvyčajne veľmi ďaleko od seba a majú medzi sebou medzeru. Vidíme tiež, že hlavnou charakteristikou plynov je to, že medzi ich časticami existuje prakticky iba interakcia, keď sa navzájom zrazia.
Pokiaľ ide o zákon ideálneho plynu, môžeme povedať, že nám ukazuje vzťah medzi tlakom, objemom, teplotou a počtom mólov. Tento vzťah sa získal z jednoduchého modelu pre plyny, ktorý umožňuje na základe štúdia pohybu atómov a molekúl určiť vzťah medzi makroskopickými veličinami. Kinetická teória plynov je založená na štyroch postulátoch:
1 – plyn je tvorený molekulami, ktoré sú v neusporiadanom a trvalom pohybe. Každá molekula môže mať inú rýchlosť ako ostatné.
2 – každá molekula plynu interaguje s ostatnými iba prostredníctvom kolízií (bežné kontaktné sily). Jedinou energiou molekúl je kinetická energia.
3 – všetky zrážky medzi molekulami a stenami nádoby obsahujúcej plyn sú dokonale elastické. Celková kinetická energia je zachovaná, ale rýchlosť každej molekuly sa môže meniť.
4 – molekuly sú nekonečne malé. Väčšina objemu, ktorý zaberá plyn, je prázdny priestor.
Na základe týchto postulátov Boltzmann a Maxwell ukazujú, že priemerná kinetická energia celkových molekúl ideálneho plynu je úmerná teplote podľa výrazu:
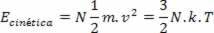
Kde k je Boltzmannova konštanta a N je počet molekúl. Hodnota k sa dá vypočítať z plynovej konštanty R a Avogadrovho čísla NTHE za
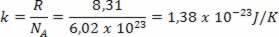
Získaný výraz ukazuje, že teplota je úmerná priemernej kinetickej energii molekúl ideálneho plynu. Vidíme teda, že teplota je priemerom stupňa rozrušenia molekúl v plyne. Pomocou počtu krtkov máme:
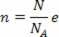
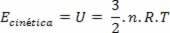
Autor: Domitiano Marques
Vyštudoval fyziku
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/fisica/teoria-cinetica-dos-gases.htm


