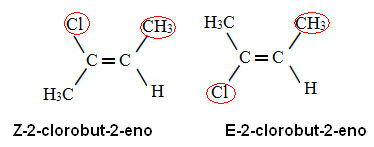
THE molekulárna geometria, to znamená usporiadanie atómov molekuly, možno určiť chemickým pravidlom Gillespie, v ktorej uvádza počet atómov pripojených k centrálnemu atómu a počet oblakov elektronika.
Znalosti o geometrii molekuly sú mimoriadne dôležité, pretože nám v tom pomáhajú stanovte polaritu a následne rozpustnosť (podľa pravidla podobných sa rozpúšťa podobný).
s hovorom štvorboká geometria, sa nelíši. Pozrite si kritériá na jej stanovenie podľa pravidiel Gillespie:
Pentatomické molekuly (päť atómov);
Absencia elektronických mračien v centrálnom atóme;
zložené molekuly alebo zložené anióny.
Niektoré príklady molekúl, ktorých geometria je štvorboká oni sú:
CH4

CH štruktúrny vzorec4
Uhlík má vo svojej valenčnej škrupine štyri elektróny a všetky tieto elektróny sa viažu s vodíkmi. Preto uhlík nemá elektronický mrak (pár elektrónov navyše).
IBA4-2
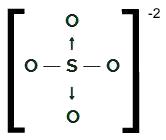
Štrukturálny vzorec OS4-2
Síra, ktorá má vo valenčnej škrupine šesť elektrónov, vytvára dve jednoduché väzby s dvoma atómami kyslíka a dvoma datívne kovalentné väzby
s ďalšími dvoma kyslíkmi. V jednoduchých väzbách používa dva zo svojich elektrónov a v každom datíve používa ďalšie dva (spolu štyri elektróny zapojené do datívov) v celkovom počte šesť elektrónov. Preto mu nezostal žiadny mrak.NH4+

NH štruktúrny vzorec4+
Dusík, ktorý má vo valenčnej škrupine päť elektrónov, vytvára tri jednoduché väzby s atómami vodíka a datívnu väzbu s druhým vodíkom. V jednoduchých väzbách používa tri zo svojich elektrónov a v datíve používa ďalšie dva, spolu päť elektrónov. Preto mu nezostal žiadny mrak.
CH3Cl
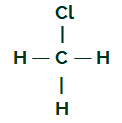
CH štruktúrny vzorec3Cl
Teraz neprestávajte... Po reklame je toho viac;)
Uhlík má vo svojej valenčnej škrupine štyri elektróny a všetky tieto elektróny sa viažu s vodíkmi a atómom chlóru. Z tohto dôvodu uhlík nemá elektronický mrak.
→ Polarita molekúl
Ak vieme, že daná molekula má štvorbokú geometriu, môžeme určiť jej polaritu veľmi jednoduchá forma, pretože molekula má svoje štyri póly obsadené (štyri ligandy v atóme centrálny). Na to stačí poznať vlastnosti spojív a zvážiť jedno z nasledujúcich pravidiel:
Ak sa počet oblakov rovná počtu rovnakých ligandov = nepolárna molekula;
Ak je počet oblakov odlišný od počtu rovnakých ligandov = polárna molekula.
V nasledujúcich dvoch molekulách, ktorých geometria je štvorboká, môžeme použiť pravidlá uvedené vyššie a označiť ich polaritu:
Molekula metánu
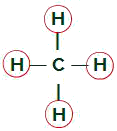
Rovnaké ligandy v molekule metánu
Molekula metánu má štyri elektrónové oblaky (štyri jednoduché väzby) a tiež štyri atómy vodíka pripojené k centrálnemu atómu. Teda mámeštyrimraky a štyri rovnaké spojiváčoskoro molekula je nepolárna.
Pozorovanie: Ak je molekula látky apolát, dobre sa rozpúšťa v inej látke, ktorej molekuly sú tiež nepolárny.
Chlórmetánová molekula

Rovnaké ligandy v molekule chlórmetánu
Molekula chlórmetánu má štyri elektrónové oblaky (štyri jednoduché väzby) a tri atómy vodíka a jeden atóm chlóru pripojený k centrálnemu atómu. Teda mámeštyrimraky a tri rovnaké ligandy (tri vodíky); čoskoro molekula je polárna.
Pozorovanie: Ak je molekula látky polárny, dobre sa rozpúšťa v inej látke, ktorej molekuly sú tiež polárny.
Podľa mňa. Diogo Lopes Dias
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
DNI, Diogo Lopes. „Štvorboká geometria“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/geometria-tetraedrica.htm. Prístup k 28. júnu 2021.