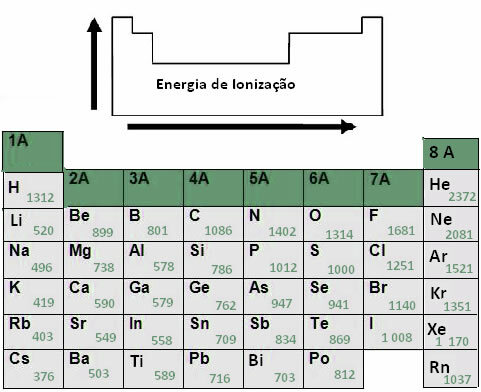
Periodická tabuľka zobrazuje elementárnu podobnosť a prostredníctvom nej je možné poznať vlastnosti prvku na základe člena patriaceho do rovnakej rodiny alebo skupiny. Prezrite si skupinu 2 periodickej tabuľky a zistite, prečo sú členovia umiestnené blízko seba:
Konfigurácia elektroniky atómového čísla
4 B a 2 s2
12 mg 3 sek2
20 Ca 4 s2
38 Mr 5 s2
56 Ba 6 s2
88 Ra 7 s2
Poznámka: Toto nastavenie je ekvivalentné s poslednou úrovňou, ktorá prijímala elektróny.
Skupina 2 A, ktorá sa tiež nazýva alkalická rodina Zeme, obsahuje kovy s elektronickou distribúciou končiace na nižších úrovniach2. Aj keď sa atómové čísla prvkov líšia, počet elektrónov vo valenčnom obale je rovnaký a zodpovedá 2. Elektronické konfigurácie týchto prvkov sú podobné, a preto sú si chemicky podobné, čím sa dostávame k periodickému zákonu:
Teraz neprestávajte... Po reklame je toho viac;)
„Fyzikálne a chemické vlastnosti prvkov sú periodické funkcie ich atómových čísel.“
štruktúra tabuľky
V tabuľke sú prvky usporiadané vodorovne v číselnom poradí podľa ich atómových čísel, čo vedie k vzniku siedmich vodorovných čiar (alebo bodiek). Každé obdobie, s výnimkou prvého, sa začína kovom a končí sa ušľachtilým plynom. Obdobia sa líšia svojou dĺžkou, pričom niektoré majú iba 2 prvky (krátke obdobie) a iné už majú 32 prvkov (dlhé obdobie).
Skupiny zodpovedajú zvislým čiaram, ktoré boli zoskupené na základe podobných štruktúr vonkajšej vrstvy (ako v príklade skupiny 2). V niektorých z týchto skupín sú prvky vo svojich vlastnostiach tak úzko spojené, že sa nazývajú rodiny, napríklad skupina 1 A je skupina Alkaline Metals.
Líria Alves
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
SOUZA, Líria Alves de. „Organizácia periodickej tabuľky“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/organizacao-tabela-periodica.htm. Prístup k 27. júnu 2021.