О смещение химического равновесия это способ, которым реакционная система выходит из ситуации химический баланс. При этом переключении скорость, с которой происходит прямая реакция (стрелка 1), такая же, как и обратная реакция (стрелка 2).
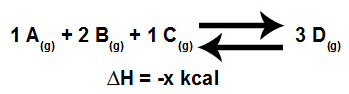
Модель уравнения химического равновесия
Итак, во время смещение химического равновесия, обратная реакция преобладает над прямой реакцией и имеет тенденцию к образованию реагентов A, B, C, или прямая реакция преобладает над обратной реакцией и имеет тенденцию к образованию продукта D.
Об этих случаях сообщил французский химик Анри Луи Ле Шателье. Он обнаружил, что когда система в равновесии нарушается, она имеет тенденцию работать против создаваемого возмущения и для этого стремится достичь новой ситуации равновесия. Этот системный тренд называется принцип Ле Шателье.
Согласно исследованиям, проведенным Ле Шателье, единственные факторы, способные продвигать смещение химического равновесия они есть:
Концентрация участников;
Температура;
Давление.
Влияние концентрации на смещение баланса
Изменение концентрации участника реакции является фактором, способствующим смещение химического равновесия. В целом, согласно принципу Ле Шателье, при изменении концентрации одного из участников баланс ведет себя следующим образом:
Повышенная концентрация: баланс движется в направлении, противоположном участнику;
Снижение концентрации: баланс движется в том же направлении, что и участник.
Пример отношения равновесия:
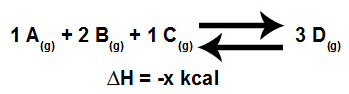
Модель уравнения химического равновесия
Так что если:
Увеличиваем концентрацию реагентов A, B или C: баланс будет смещен в противоположную им сторону, то есть будет смещен вправо (направление образования D);
Увеличиваем концентрацию продукта D: баланс будет смещен в противоположную сторону от баланса реагентов, то есть будет смещен влево (направление образования реагентов A, B и C);
Уменьшить концентрацию реагентов A, B или C: равновесие будет смещено в их же направлении, то есть смещено влево (направление образования реагентов);
Уменьшаем концентрацию продукта D: баланс будет смещен в том же направлении, что и он, то есть будет смещен вправо (направление формирования продукта).
Примечание: Изменение концентрации солидных участников не меняет баланса.
Влияние температуры на смещение равновесия
Изменение температуры во время химической реакции является фактором, способствующим смещение химического равновесия. Что касается этого изменения температуры, в целом, согласно принципу Ле Шателье, весы ведут себя следующим образом:
При повышении температуры: баланс смещается в сторону эндотермической реакции;
При понижении температуры: баланс смещается в сторону экзотермической реакции.
Чтобы провести анализ влияния температуры на равновесие, необходимо знать природу прямых и обратных реакций, которая определяется изменением энтальпии реакции. Так что если:
∆H положительный: прямая эндотермическая реакция и обратная экзотермическая реакция;
∆H отрицательный: прямая экзотермическая реакция и обратная эндотермическая реакция.
Например, по следующему балансу:
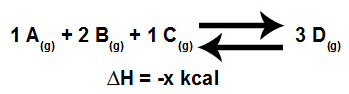
Модель уравнения химического равновесия
В этом случае при отрицательной ∆H прямая реакция является экзотермической, а обратная реакция эндотермической. Так что если:
Повышаем температуру системы, равновесие будет смещено в противоположном направлении (эндотермической реакции), то есть смещено влево (направление образования реагентов);
Снижаем температуру системы, равновесие будет смещено в прямом направлении (экзотермической реакции), то есть смещено вправо (направление образования продукта D).
Влияние давления на смещение баланса
Во время химической реакции изменение давления в окружающей среде является фактором, способствующим смещение химического равновесия. В общем, согласно принципу Ле Шателье, баланс ведет себя следующим образом с (а):
повышение давления: баланс движется в сторону наименьшего объема;
Снижение давления: баланс смещается в сторону большей громкости.
Чтобы проанализировать влияние давления на равновесие, необходимо знать объем, установленный в реагенты и продукты, которые можно определить с помощью коэффициентов, которые делают уравнение сбалансированным, как в примере следить:
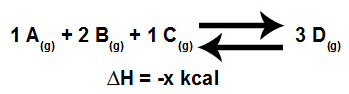
Модель уравнения химического равновесия
Таким образом, реагенты имеют объем 4 л, который получается суммой коэффициентов 1, 2 и 2, а уникальный продукт имеет объем 3 л (определяется коэффициентом 3).
Таким образом, в отношении вышеуказанного баланса, если:
Повышаем давление в системе, баланс будет смещен в прямом направлении (от наименьшего объема, 3L), то есть будет смещен вправо (направление образования продукта D).
Уменьшаем давление в системе, равновесие сместится в обратную сторону (от наибольшего объема, 4 л), то есть сместится влево (направление образования реагентов).
Примечание: Увеличение или уменьшение давления в равновесной системе может способствовать вытеснению только в тех случаях, когда объем реагентов отличается от объема продуктов.
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/fatores-que-alteram-equilibrio-quimico.htm


