В константа гидролиза (Kh) относится к химический баланс установлено в результате гидролиза соли (химическая реакция с участием растворимой соли и воды).
Как константа любого другого равновесия, выражение константа гидролиза рассчитывается как произведение концентраций продукта, деленное на произведение концентраций реагентов, следующим образом:
Kh = [продукты]
[реагенты]
Работа с константой гидролиза требует знания трех важных явлений:
- Диссоциация солей;
- Ионизация воды;
- Гидролиз соли.
Диссоциация солей
Когда растворимая соль добавляется к воде, она диссоциирует и высвобождает катион, отличный от гидроксония (H +), и анион, отличный от гидроксила (OH-).

Чтобы напомнить вам, когда соль растворяется или не растворяется в воде, кликните сюда и изучите таблицу растворимости солей.
ионизация воды
Вода - это вещество, которое естественным образом подвергается феномену самоионизации, то есть образует катион гидроксония и гидроксил-анион.
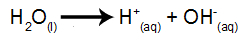
уравнение ионизации воды
гидролиз соли
Как растворимая соль он выделяет ионы в воду, и вода подвергается ионизации, производя
ионы в середине может происходить реакция (гидролиз) между ионами соли и ионами воды. Когда происходит эта реакция, возможны следующие взаимодействия:- Катион соли с анионом воды (образование основания);
- Анион соли с катионом воды (образование соли);
Вышеуказанные взаимодействия будут происходить только в том случае, если образовавшееся основание или кислота являются слабыми.
См. Пример гидролиза соли:
→ Гидролиз гипохлорита аммония (NH4ClO)
Когда гипохлорит аммония добавляется в воду, он растворяется и диссоциирует, высвобождая ионы катиона аммония (NH4 +) и анион гипохлорита (ClO-):

Уравнение, показывающее ионы, выделяющиеся при диссоциации гипохлорита аммония
Поскольку вода, подвергаясь ионизации, производит H + и OH-, мы имеем в растворе два катиона и два аниона, которые могут вступать в реакцию. Катион NH4 + реагирует только с анионом OH-, потому что он образует слабое основание (NH4OH). Анион ClO- реагирует только с катионом H +, потому что он образует слабую кислоту (HClO).

Уравнение равновесия гидролиза гипохлорита аммония
Построение выражения константы гидролиза
Построение константы гидролиза соли зависит исключительно от уравнения гидролиза этой соли. Например, гидролиз гипохлорита аммония, рассмотренный в предыдущем пункте, дает следующее уравнение:

Уравнение равновесия гидролиза гипохлорита аммония
Как построить выражение константа гидролиза с учетом продуктов и реагентов выражение константы будет:
Kh = [HClO]. [NH4OH]
[ClO -]. [NH4 +]
ПРИМЕЧАНИЕ. Вода не участвует в уравнении, потому что это жидкий реагент, а также потому, что она является основным средством возникновения гидролиза, то есть она постоянна.
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-constante-hidrolise.htm