Основные неорганические функции: кислоты, основания, соли и оксиды.
Неорганические соединения обладают разными свойствами и присутствуют во многих ситуациях нашей повседневной жизни. По этой причине эта тема широко обсуждается на вступительных экзаменах, в Enem и на конкурсах.
Чтобы помочь вам подготовиться к экзаменам, мы создали этот список 15 вопросов с прокомментированными разрешениями и различными подходами для каждой неорганической функции.
Общие понятия
1. (FGV) Некоторые соединения при растворении в воде образуют водный раствор, который проводит электричество. Из соединений ниже:
| Я. В2ТОЛЬКО4 |
| II. О2 |
| III. Ç12ЧАС22О11 |
| IV. KNO3 |
| В. CH3COOH |
| УВИДЕЛ. NaCl |
Они образуют водный раствор, проводящий электричество:
а) только I, IV и VI
б) только I, IV, V и VI
вызов
г) только I и VI
д) только видел
Правильная альтернатива: б) только I, IV, V и VI.
Электропроводность в растворе происходит из-за образования электрически заряженных частиц, ионов, как обнаружил Аррениус в своих экспериментах.
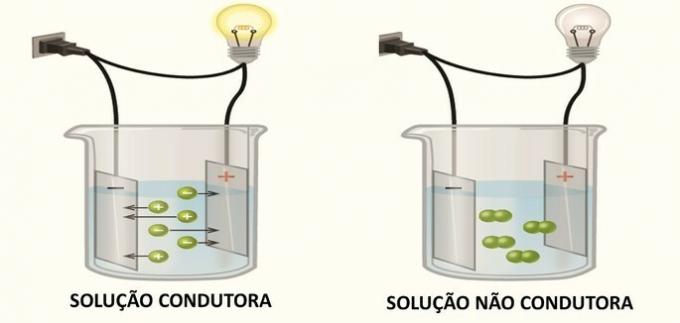
Когда ионы образуются в растворе, катионы (положительный заряд) мигрируют к отрицательному полюсу, а анионы (отрицательный заряд) перемещается к положительному полюсу, замыкая электрическую цепь и позволяя прохождение цепь.
Соединения, которые в растворе образуют нейтральные частицы, не проводят электричество.
Согласно этой информации мы должны:
Я. ПРИВОД
В растворе соль диссоциирует и образуются ионы.
II. НЕ ПРИВОДИТ
Двухатомный кислород при комнатной температуре представляет собой инертную молекулу.
III. НЕ ПРИВОДИТ
Представленная формула предназначена для сахарозы, молекулярного соединения, молекулы которого при контакте с водой диспергируются, но не теряют своей идентичности.
IV. ПРИВОД
В растворе соль диссоциирует и образуются ионы.
В. ПРИВОД
Уксусная кислота - это слабая кислота, которая имеет небольшую ионизированную часть в растворе.
УВИДЕЛ. ПРИВОД
В растворе соль диссоциирует и образуются ионы.
2. (Маккензи-СП)
Вышеприведенное уравнение представляет собой реакцию
а) ионной диссоциации.
б) который содержит двухосновную кислоту в качестве реагента.
в) полной ионизации с образованием катиона гидроксония.
г) ионизации с образованием фосфид-аниона.
д) который при полной ионизации дает одновалентный анион.
Правильная альтернатива: в) полная ионизация с образованием катиона гидроксония.
Фосфорная кислота - это химическое соединение, которое ионизируется при контакте с водой и выделяет ионы H.+.
Ионизация происходит в три этапа:
| Первый шаг | |
| Вторая стадия | |
| третий шаг | |
| сумма шагов |
Катионы (H+) реагируют с водой, образуя ион гидроксона (H3О+).
В соответствии с этим рассуждением мы должны:
а) НЕПРАВИЛЬНО. Диссоциация происходит в ионных соединениях, а фосфорная кислота является молекулярным соединением.
б) НЕПРАВИЛЬНО. Фосфорная кислота является трехкислотой, потому что она имеет три ионизируемых атома водорода.
в) ПРАВИЛЬНО. Катион гидроксония, также называемый гидроксонием, представляет собой разновидность, образующуюся при соединении ионизируемого водорода с водой.
г) НЕПРАВИЛЬНО. Производимый анион - фосфат (). Формула фосфида:
д) НЕПРАВИЛЬНО. Образовавшийся анион () трехвалентен, потому что имеет 3 заряда.
3. Правильно свяжите указанные ниже соединения с их соответствующими неорганическими функциями.
| Я. HBr, H3ПЫЛЬ4 и H2CO3 | () кислоты |
| II. CO2, ТОЛЬКО2 и Al2О3 | () базы |
| III. Al2(ОЙ)3, КОН и NH4ой | () соли |
| IV. NaCℓ, KNO3 и BaSO4 | () оксиды |
Кислоты - это соединения, содержащие ионизируемые атомы водорода.
(я) кислоты: HBr, H3ПЫЛЬ4 и H2CO3
Основания содержат гидроксил-ион.
(III) основания: Al2(ОЙ)3, КОН и NH4ой
Соли - это ионные соединения, образованные катионами и анионами.
(IV) соли: NaCℓ, KNO3 и BaSO4
Оксиды - это соединения, образующиеся при соединении кислорода с другими элементами, кроме фтора.
(II) оксиды: CO2, ТОЛЬКО2 и Al2О3
Кислоты
4. Напишите названия следующих кислот:
а) HCl и HBr
Соляная кислота и бромистоводородная кислота.
Вышеуказанные соединения представляют собой гидраты. Кислоты этого класса имеют формулу HИксA, где x представляет количество атомов водорода (H), а A соответствует связанному металлу.
Номенклатура этих веществ сделана следующим образом:
| ЧАС | Cl | |
| Кислота | Хлор | гидрик |
| Соляная кислота |
| ЧАС | br | |
| Кислота | Бром | гидрик |
| бромистоводородная кислота |
б) HNO3 и HNO2
Азотная кислота и азотистая кислота.
Вышеуказанные соединения представляют собой оксикислоты с двумя степенями окисления. Кислоты этого класса имеют формулу HИксАО, образованный водородом, неметаллом и кислородом.
Номенклатура этих веществ сделана следующим образом:
| ЧАС | N | О3 |
| Кислота | Нитр | ich |
| Азотная кислота. NOx азота в этом соединении +5. |
Соединение с самым низким содержанием NOx - это азотистая кислота: HNO.2.
| ЧАС | N | О2 |
| Кислота | Нитр | кость |
| Азотистая кислота. NOx азота в этом соединении +3. |
в) HClO, HClO2, HClO3 и HClO4
Хлорноватистая, хлорноватистая, хлорная и хлорная кислоты.
Вышеуказанные соединения представляют собой оксикислоты с четырьмя степенями окисления. Кислоты этого класса имеют формулу HИксАО, образованный водородом, кислородом и неметаллом семейства 7А.
Номенклатура этих веществ сделана следующим образом:
| Nox +1 | Кислота | Бегемот | префикс элемента | кость |
| Nox +3 | Кислота | - | префикс элемента | кость |
| Nox +5 | Кислота | - | префикс элемента | ich |
| Нокс +7 | Кислота | на | префикс элемента | ich |
Соединения, указанные в альтернативе, имеют следующие названия:
| ЧАС | Cl | О | |
| Кислота | Бегемот | хлор | кость |
| Хлорноватистая кислота. NOx хлора в этом соединении +1. |
| ЧАС | Cl | О2 |
| Кислота | хлор | кость |
| Хлорная кислота. NOx хлора в этом соединении +3. |
| ЧАС | Cl | О3 |
| Кислота | хлор | ich |
| Хлорная кислота. NOx хлора в этом соединении +5. |
| ЧАС | Cl | О4 | |
| Кислота | на | хлор | ich |
| Хлорная кислота. NOx хлора в этом соединении +7. |
5. (UVA-CE) HClO кислоты4, H2MnO4, H3ПЫЛЬ3, H4Суббота2О7По количеству ионизируемых водородов их можно разделить на:
а) одноосновная, двухосновная, трехосновная, четырехкислота.
б) одноосновная кислота, двухосновная кислота, трехосновная кислота, трехосновная кислота.
в) одноосновная кислота, двухосновная кислота, двухосновная кислота, четырехкислота.
г) одноосновная кислота, одноосновная кислота, двухосновная кислота, трехосновная кислота.
Правильная альтернатива: в) одноосновная кислота, двухосновная кислота, двухосновная кислота, четырехкислота.
Ионизация представленных кислот происходит следующим образом:
Структурные формулы показывают нам, что ионизируемые водороды связаны с кислородом.
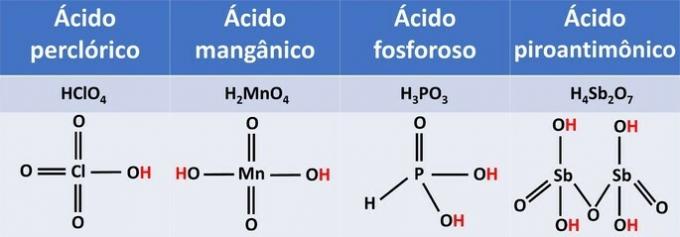
По количеству ионизируемых водородов кислоты можно разделить на:
| HClO4 | ионизируемый водород | одноосновная кислота |
| ЧАС2MnO4 | Два ионизируемых водорода | двухосновная кислота |
| ЧАС3ПЫЛЬ3 | Два ионизируемых водорода | двухосновная кислота |
| ЧАС4Суббота2О7 | Четыре ионизируемых атома водорода | тетрацид |
Для оксикислот ионизируемые водороды - это те атомы, которые непосредственно присоединены к кислороду. Фосфорная кислота имеет один из трех атомов водорода, связанных с центральным элементом, фосфором, и поэтому является двухосновной кислотой.
6. (UESPI) Пусть кислоты будут перечислены ниже с их соответствующими степенями ионизации в процентах (α%):
|
HClO4 (α% = 97%) |
ЧАС2ТОЛЬКО4 (α% = 61%) |
ЧАС3BO3 (α% = 0,025%) |
ЧАС3ПЫЛЬ4 (α% = 27%) |
HNO3 (α% = 92%) |
Проверьте правильность утверждения:
а) H3ПЫЛЬ4 сильнее H2ТОЛЬКО4.
б) HNO3 это мягкая кислота.
в) HClO4 слабее HNO3.
г) H3ПЫЛЬ4 это сильная кислота.
д) H3BO3 это слабая кислота.
Правильная альтернатива: e) H3BO3 это слабая кислота.
Значение соответствует степени ионизации и рассчитывается по формуле:
Чем выше значение , тем сильнее кислота, потому что это означает, что в раствор попало больше ионизированных частиц.
В соответствии с этим рассуждением мы должны:
а) НЕПРАВИЛЬНО. Чем выше значение , тем сильнее кислота. H2ТОЛЬКО4 имеет более высокую степень ионизации, чем H3ПЫЛЬ4.
б) НЕПРАВИЛЬНО. HNO3 он имеет степень ионизации более 90%. Это сильная кислота.
в) НЕПРАВИЛЬНО.4 имеет более высокую степень ионизации, чем HNO3 будучи, следовательно, сильнее, чем он.
г) НЕПРАВИЛЬНО. H3ПЫЛЬ4 это умеренная кислота, так как она имеет степень ионизации от 5% до 50%.
д) ПРАВИЛЬНО. H3BO3 он имеет степень ионизации менее 5% и поэтому является слабой кислотой.
Базы
7. Введите название следующих баз:
а) LiOH и Be (OH)2
Гидроксид лития и гидроксид бериллия.
Представленные базы имеют фиксированную плату и поэтому номенклатура составлена следующим образом:
LiOH: гидроксид лития.
Будь (ОН)2: гидроксид бериллия.
б) CuOH и Cu (OH)2
Гидроксид меди и гидроксид меди.
Медь имеет две степени окисления: +1 и +2. Один из способов назвать переменную базу nox следующим образом:
| Nox +1 | CuOH | гидроксид одновалентной меди |
| Nox +2 | Cu (OH)2 | гидроксид меди |
в) Sn (ОН)2 и Sn (OH)4
Гидроксид олова (II) и гидроксид олова (IV).
Олово имеет две степени окисления: +2 и +4. Номенклатура переменной базы nox также может быть выполнена следующим образом:
| Nox +2 | Sn (ОН)2 | Гидроксид олова II |
| Nox +4 | Sn (ОН)4 | Гидроксид олова IV |
8. (Fiam-SP) Для борьбы с кислотностью желудка, вызванной избытком соляной кислоты, обычно принимают внутрь антацид. Из перечисленных ниже веществ, встречающихся в повседневной жизни людей, наиболее подходящими для борьбы с кислотностью являются:
газировка.
б) апельсиновый сок.
в) вода с лимоном.
г) уксус.
д) молоко магнезии.
Правильная альтернатива: д) молоко магнезии.
Антациды - это вещества, которые используются для повышения pH желудка, потому что избыток соляной кислоты вызывает снижение pH и, как следствие, повышение кислотности.
Для борьбы с кислотностью желудка рекомендуется принимать внутрь вещество с основным характером, потому что, вступая в реакцию с желудочной кислотой, она вызывает реакцию нейтрализации с образованием соли и воды.
В соответствии с этим рассуждением мы должны:
а) НЕПРАВИЛЬНО. Соду использовать нельзя, так как она содержит в своем составе угольную кислоту.
б) НЕПРАВИЛЬНО. Апельсин использовать нельзя, так как он содержит в своем составе лимонную кислоту.
в) НЕПРАВИЛЬНО. Лимон использовать нельзя, так как он содержит в своем составе лимонную кислоту.
г) НЕПРАВИЛЬНО. Уксус использовать нельзя, так как он содержит в своем составе уксусную кислоту.
д) ПРАВИЛЬНО. Следует использовать молоко магнезии, так как оно содержит в своем составе основу гидроксида магния.
Образуется реакция нейтрализации:
9. (Осек) Сильная база должна быть связана с группой ОН-:
а) очень электроположительный элемент.
б) очень электроотрицательный элемент.
в) полуметалл.
г) металл, дающий 3 электрона.
д) неметалл.
Правильная альтернатива: а) очень электроположительный элемент.
Сильное основание - это основание с высокой степенью диссоциации, то есть свободные гидроксильные ионы в растворе.
Ион гидроксила имеет отрицательный заряд, так как ему удается притягивать электрон к себе при диссоциации из-за электроотрицательности кислорода.
Таким образом, очень электроположительный элемент имеет способность терять электроны и отдавать их гидроксилу, оставаясь в растворе в катионной форме.
а) ПРАВИЛЬНО. Электроположительные элементы, такие как щелочные и щелочноземельные металлы, образуют сильные основания.
б) НЕПРАВИЛЬНО. Элемент более электроотрицательный, чем кислород, вызвал бы конкуренцию за электрон.
в) НЕПРАВИЛЬНО. Полуметалл обладает большой электроотрицательностью.
г) НЕПРАВИЛЬНО. Ион гидроксила имеет заряд 1. металл, дающий 3 электрона, будет образовывать основание с 3 гидроксилами.
Пример:
д) НЕПРАВИЛЬНО. Самые сильные основания - это основания, образованные из металлов.
соли
10. Напишите названия следующих солей:
а-н-а2CO3
Карбонат натрия.
Это разновидность нейтральной соли, номенклатура которой следующая:
| анион | катион |
| В+ | |
| карбонат | натрий |
| Карбонат натрия |
б) KNaSO4
Сульфат натрия и калия.
Это тип двойной соли, и его номенклатура такая же, как у нейтральной соли, а названия двух катионов написаны.
| анион | катионы | |
| K+ | В+ | |
| Сульфат | калий | натрий |
| Сульфат натрия и калия |
в) NaHCO3
Моногидрокарбонат натрия.
Это разновидность кислотной соли, и ее номенклатура представлена следующим образом:
| Количество водородов | анион | катион |
| 1 | В+ | |
| Мононуклеоз | карбонат | натрий |
| Моногидрокарбонат натрия |
Популярное название этого соединения - бикарбонат натрия.
г) Al (OH)2Cl
Дигидроксихлорид алюминия.
Это разновидность основной соли, и ее номенклатура представлена следующим образом:
| Количество гидроксилов | анион | катион |
| 2 | Cl- | Al3+ |
| Ди | хлористый | алюминий |
| Дигидроксихлорид алюминия |
Это соединение также известно как двухосновный хлорид алюминия.
д) CuSO4. 5 часов2О
Пентагидрат сульфата меди.
Это тип гидратированной соли, и его номенклатура представлена следующим образом:
| анион | катион | количество молекул воды |
| Жопа2+ | 5 | |
| Сульфат | медь | пента |
| Пентагидрат сульфата меди |
11. (Unirio) Соли также являются продуктами, полученными реакцией полной или частичной нейтрализации ионизируемых водородов кислот с основаниями или гидроксидами в соответствии с общей реакцией:
Кислота + Основание Соль + Вода
Основываясь на этом утверждении, какая единственная кислота не имеет всех связанных с ней возможных продуктов?
а) соляная кислота дает только нейтральную хлоридную соль.
б) азотная кислота дает только нейтральную нитратную соль.
c) фосфорная кислота дает только нейтральную фосфатную соль.
г) сульфид может давать либо нейтральную сульфидную соль, либо кислотную соль, кислотный сульфид или сероводород.
д) серная кислота может давать либо нейтральную сульфатную соль, либо кислотную соль, кислый сульфат или гидросульфат.
Неправильная альтернатива: в) фосфор производит только нейтральную фосфатную соль.
а) ПРАВИЛЬНО. Соляная кислота имеет только один ионизируемый водород, который реагирует с образованием воды. В этом случае соль будет образована анионом кислоты, в данном случае хлоридом, и катионом основания.
Примеры:
б) ПРАВИЛЬНО. Азотная кислота имеет только один ионизируемый водород, который реагирует с образованием воды. В этом случае соль будет образована анионом кислоты, в данном случае нитратом, и катионом основания.
Примеры:
в) НЕПРАВИЛЬНО. Фосфорная кислота имеет три ионизируемых атома водорода и, следовательно, может подвергаться частичной или полной ионизации. В этом случае могут образоваться три типа солей:
- Полная нейтрализация, генерирующая нейтральная соль:
- Частичная нейтрализация, генерирующая кислотная соль:
- Частичная нейтрализация, генерирующая основная соль:
г) ПРАВИЛЬНО. При полной нейтрализации образуется нейтральная соль, а при частичной нейтрализации может образовываться кислая соль.
- Полная нейтрализация:
- Частичная нейтрализация:
д) ПРАВИЛЬНО. При полной нейтрализации образуется нейтральная соль, а при частичной нейтрализации может образовываться кислая соль.
- Полная нейтрализация:
- Частичная нейтрализация:
| Я. В2B4О70,10 ч2О | THE. основная соль |
| II. Mg (OH) Cl | Б. двойная соль |
| III. НАКСО4 | Ç. кислотная соль |
| IV. NaHCO3 | Д. гидратированная соль |
Правильная связь между ними:
а) AI, BIII, CIV, DII
б) AII, BIV, CIII, DI
в) AI, BII, CIII, DIV
г) AII, BIII, CIV, DI
Правильная альтернатива: d) AII, BIII, CIV, DI
| AII. основная соль: Mg (OH) Cl | Он имеет в своей структуре гидроксил. |
| BIII. двойная соль: NaKSO4 | Он имеет в своей структуре два катиона металла. |
| CIV. кислотная соль: NaHCO3 | В его структуре есть водород. |
| DI. гидратированная соль: Na2B4О70,10 ч2О | В его структуре есть молекулы воды. |
Оксиды
13. Напишите названия следующих оксидов:
стали2 и нет2О3
Двуокись углерода и трехокись азота.
Эти оксиды являются молекулярными оксидами, поскольку кислород связан с неметаллами. Номенклатура этого класса оформлена следующим образом:
| количество кислорода | Количество атомов углерода |
| 2 | 1 |
| Двуокись углерода или двуокись углерода |
| количество кислорода | Количество азота |
| 3 | 2 |
| триоксид диазота |
б) Al2О3 и дальше2О
Оксид алюминия и оксид натрия.
Эти оксиды являются ионными оксидами, поскольку кислород связан с металлами. Металлы, связанные с кислородом, имеют фиксированный заряд. Поэтому номенклатура этого класса сделана следующим образом:
Al2О3: оксид алюминия
В2O: оксид натрия
б) Cu2O и CuO
Оксид меди I и оксид меди II.
Эти оксиды являются ионными оксидами, потому что кислород связан с металлом. Металл, связанный с кислородом, имеет переменный заряд. Один из способов назвать этот класс следующим образом:
| Nox +1 | Жопа2О | оксид меди I |
| Nox +2 | CuO | оксид меди II |
в) FeO и Fe2О3
Закись железа и оксид железа.
Эти оксиды являются ионными оксидами, потому что кислород связан с металлом. Металл, связанный с кислородом, имеет переменный заряд. Номенклатура переменного оксида оксида азота также может быть сделана следующим образом:
| Nox +2 | FeO | закись железа |
| Nox +3 | Вера2О3 | оксид железа |
14. (UEMA) Нейтральные атомы определенного репрезентативного элемента M имеют два электрона в валентной оболочке. Правильные формулы для нормального оксида и бромида соответственно:
(Данные: O = 6A и Br = 7A.)
являюсь2О и МБр
б) МО2 и МБр2
в) МО и МБр2
г) М2О2 в2br
в2О и МБр2
Правильная альтернатива: в) МО и МБр2
Элементы M имеют два электрона в валентной оболочке. Чтобы соединиться с другими элементами, он может потерять эти два электрона и образовать катион М.2+.
Кислород принадлежит к семейству 6A, и ему нужно еще 2 электрона, чтобы достичь стабильности с электронной конфигурацией благородного газа, как указано в правиле октетов.
Точно так же бром из семейства 7A нуждается только в 1 электроне, чтобы иметь 8 электронов в валентной оболочке.
Согласно этой информации мы должны:
а) НЕПРАВИЛЬНО. Для образования соединения M2O и MBr, элемент M должен образовывать катион M+.
б) НЕПРАВИЛЬНО. Кислород имеет 2-заряд, а не 1-заряд, как показано при образовании соединения МО.2.
в) ПРАВИЛЬНО. В зависимости от валентности ионов альтернатива верна.
г) НЕПРАВИЛЬНО. Бромид имеет 1-, а не 2-заряд, как показано при образовании соединения M2Br.
д) НЕПРАВИЛЬНО. Катион элемента имеет заряд 2+, а не заряд 1+, как показано при образовании соединения M.2О.
15. (PUC-MG) Обратите внимание на следующие химические реакции:
| Я. MgO + H2О |
| II. CO2 + H2О |
| III. K2O + 2HCl |
| IV. ТОЛЬКО3 + 2NaOH |
Неправильное утверждение:
а) В реакциях II и IV участвуют кислотные оксиды или ангидриды.
б) В реакциях I и III участвуют основные оксиды.
в) Соль, полученная в реакции IV, называется сульфатом натрия.
г) Соль, полученная в реакции III, называется хлоридом калия.
д) Основной характер оксидов усиливается, поскольку кислород связывается с большим количеством электроотрицательных элементов.
Неправильная альтернатива: д) Основной характер оксидов увеличивается по мере того, как кислород связывается с большим количеством электроотрицательных элементов.
а) ПРАВИЛЬНО. Когда кислые оксиды, такие как диоксид углерода и триоксид серы, реагируют с водой, они образуют кислоту в растворе.
б) ПРАВИЛЬНО. При взаимодействии с водой основные оксиды, такие как оксид магния и оксид калия, образуют основание в растворе.
в) ПРАВИЛЬНО. В2ТОЛЬКО4 формула сульфата натрия.
г) ПРАВИЛЬНО. KCl - это формула хлорида калия.
д) НЕПРАВИЛЬНО. Основной характер оксидов усиливается, поскольку кислород связывается с большим количеством элементов. электроположительный, как щелочные и щелочноземельные металлы, потому что, реагируя с водой, они образуют сильные основания, а при взаимодействии с кислотами образуют соль и воду.

