Химический баланс - один из предметов, который больше всего приходится на Enem и вступительные экзамены.
В вопросах рассматриваются аспекты обратимых реакций, и кандидаты оцениваются как расчетами, так и концепциями, связанными с этой темой.
Имея это в виду, мы составили список вопросов с разными подходами к химическому балансу.
Воспользуйтесь комментариями к решению, чтобы подготовиться к экзаменам, и ознакомьтесь с пошаговыми инструкциями, как решать вопросы.
Общие представления о химическом равновесии
1. (Уэма) В уравнении , после достижения химического равновесия можно сделать вывод о константе равновесия
, о котором правильно сказать, что:
а) чем выше значение Kc, тем ниже выход прямой реакции.
б) Кç независимо от температуры.
в) если скорости прямой и обратной реакции равны, то Кс = 0.
г) Кç это зависит от исходной молярности реагентов.
д) чем больше значение Kc, тем больше концентрация продуктов.
Правильный ответ: д) чем больше значение Кс, тем больше концентрация продуктов.
Прямая реакция обозначается цифрой 1, где:
Обратная реакция представлена
Значение Kç он рассчитывается по соотношению концентраций продуктов и реагентов.
Числитель (который содержит продукты) прямо пропорционален константе равновесия. Следовательно, чем выше значение Kç, чем больше выход прямой реакции, чем больше продукта образуется и, следовательно, тем больше концентрация продуктов.
Значение Kç изменяется в зависимости от температуры, потому что, когда мы меняем его значение, может происходить эндотермическая (поглощение тепла) или экзотермическая (выделение тепла) реакция. предпочтительнее, и с этим можно потреблять или создавать больше реагента или продукта, тем самым изменяя константу равновесия, которая зависит от концентрации реагенты.
Kc зависит от молярных количеств компонентов, когда устанавливается равновесие и когда скорости прямой и обратной реакций равны.
2. (УФРН) Химический баланс характеризуется динамичностью на микроскопическом уровне. Для получения количественной информации о степени химического равновесия используется величина константы равновесия. Рассмотрим следующую полосу:

Применительно к химическому балансу идея баланса персонажа:
а) Это правильно, потому что в химическом равновесии половина количества всегда продукты, а другая половина - реагенты.
б) Это неверно, поскольку в химическом равновесии концентрации продуктов и реагентов могут быть разными, но постоянными.
c) Это правильно, потому что в химическом равновесии концентрации реагентов и продуктов всегда одинаковы, пока равновесие не нарушается внешним воздействием.
г) Это неверно, поскольку в химическом равновесии концентрации продуктов всегда выше, чем концентрации реагентов, если на равновесие не влияет внешний фактор.
д) Это правильно, потому что в химическом равновесии концентрации реагентов и продуктов не всегда одинаковы.
Правильный ответ: б) Это неверно, так как в химическом равновесии концентрации продуктов и реагентов могут быть разными, но постоянными.
В состоянии равновесия количество продуктов и реагентов можно рассчитать на основе константы баланс, и не обязательно должна быть половина количества продуктов, а другая половина реагенты.
Равновесные концентрации не всегда одинаковы, они могут быть разными, но постоянными, если не происходит нарушений равновесия.
Равновесные концентрации должны зависеть от того, какая реакция предпочтительна, прямая или обратная. Мы можем узнать это по значению Kç: если Kç 1. Прямая реакция предпочтительна. уже если Kç
1 предпочтительна обратная реакция.
Графики химического баланса
3. (UFPE) В начале 20 века ожидание Первой мировой войны вызвало большую потребность в соединениях азота. Хабер был пионером в производстве аммиака из азота в воздухе. Если аммиак помещен в закрытую емкость, он разлагается в соответствии со следующим несбалансированным химическим уравнением: NH3(грамм) → N2 (г) + H2 (г). Изменения концентраций во времени показаны на следующем рисунке:

Из анализа приведенного выше рисунка мы можем утверждать, что кривые A, B и C представляют собой временное изменение концентраций следующих компонентов реакции, соответственно:
а) H2, нет2 и NH3
б) NH3, H2 и нет2
в) NH3, нет2 и H2
г) Нет2, H2 и NH3
д) H2, NH3 и нет2
Правильный ответ: г) Н2, H2 и NH3.
1-й шаг: сбалансировать химическое уравнение.
2 NH3(грамм) → N2 (г) + 3 ЧАС2 (г)
Благодаря сбалансированной реакции мы поняли, что для разложения на азот и водород требуется 2 моля аммиака. Кроме того, количество водорода, образующегося в реакции, в три раза больше, чем количество аммиака.
2-й шаг: интерпретировать данные диаграммы.
Если аммиак разлагается, то на графике его концентрация максимальная и уменьшается, как видно на кривой C.
Концентрация продуктов по мере их образования в начале реакции равна нулю и увеличивается по мере того, как реагент становится продуктом.
Поскольку количество производимого водорода в три раза больше, чем количество азота, кривая для этого газа является наибольшей, как отмечено в B.
Другой образующийся продукт представляет собой азот, как показано на кривой А.
4. (Cesgranrio) Система, представленная уравнением был в равновесии. Состояние равновесия было резко изменено добавлением вещества G. Система реагирует на восстановление баланса. Какая из следующих диаграмм лучше всего отображает изменения, произошедшие во время описанного процесса?
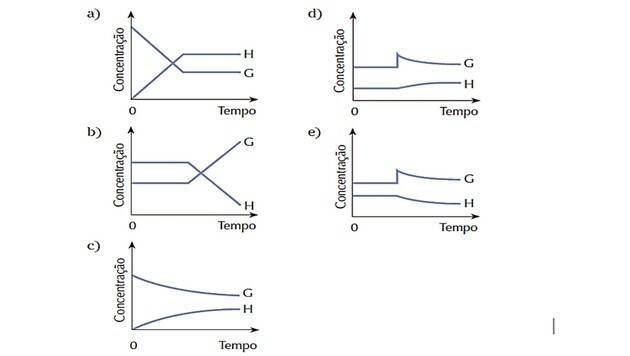
Правильный ответ: г).

Поскольку вначале система находилась в равновесии, количества веществ G и H оставались постоянными.
Нарушение возникло, когда концентрация G увеличилась, и система отреагировала преобразованием этого реагент в большем количестве продукта H, смещая баланс вправо, то есть в пользу реакции непосредственный.
Мы наблюдаем, что кривая G реагента уменьшается по мере его расходования, а кривая продукта H увеличивается по мере его образования.
Когда устанавливается новое равновесие, количества снова становятся постоянными.
Константа равновесия: соотношение между концентрацией и давлением
5. (УФРН) Зная, что Kп = Kç (RT)п, можно сказать, что Kп = Kç, для:
стали2(грамм) + H2 (г) ↔ CO(грамм) + H2О(грамм)
б) H2 (г) + ½2 (г) ↔ H2О(1)
в) Нет2 (г) + 3 часа2 (г) ↔ 2 NH3(грамм)
г) НЕТ(грамм) + ½ O2(грамм) ↔ НЕТ2(грамм)
д) 4 FeS(s) + 7 O2 (г) ↔ 2 Fe2О3 (с) + 4 СО2(грамм)
Правильный ответ: а) СО2(грамм) + H2 (г) ↔ CO(грамм) + H2О(грамм)
Кп быть равным Kç вариация количества родинок должна равняться нулю, так как любое число, возведенное в ноль, дает 1:
Kп = Kç (RT)0
Kп = Kç х 1
Kп = Kç
Изменение количества родинок рассчитывается по:
∆n = Количество молей продуктов - Количество молей реагентов
В этом расчете участвуют только коэффициенты веществ в газообразном состоянии.
Применяя к каждому альтернативному уравнению, мы имеем:
| стали2(грамм) + H2 (г) ↔ CO(грамм) + H2О(грамм) | ∆n = [(1 + 1) - (1 + 1)] = 2–2 = 0 |
| б) H2 (г) + ½2 (г) ↔ H2О(1) | ∆n = [0 - (1 + 1/2)] = 0 - 3/2 = - 3/2 |
| в) Нет2 (г) + 3 часа2 (г) ↔ 2 NH3 (г) | ∆n = [2 - (1 + 3)] = 2–4 = - 2 |
| г) НЕТ(грамм) + ½2 (г) ↔ НЕТ2 (г) | ∆n = [1 - (1 + 1/2)] = 1 - 3/2 = - 1/2 |
| д) 4 FeS(s) + 7 O2 (г) ↔ 2 Fe2О3 (с) + 4 СО2 (г) | ∆n = [(0 + 4) - (0 + 7)] = 4–7 = - 3 |
С этими результатами мы можем заметить, что альтернатива, значение которой соответствует требуемому результату, является альтернативой в первом уравнении.
6. (Адаптировано для UEL) Для реакции, представленной константы равновесия Kç и Kп выражаются уравнениями: (Дано: p = парциальное давление)
Правильная альтернатива:
Константа равновесия рассчитывается по формуле:
Твердые соединения из-за их постоянной концентрации не участвуют в расчете Kç, следовательно, константа равновесия для данного уравнения равна:
Для константы равновесия с точки зрения давления в расчетах участвуют только газы, поэтому:
Расчет константы равновесия
7. (Enem / 2015) Некоторые кислоты используются в отраслях промышленности, которые сбрасывают сточные воды в водоемы, такие как реки и озера, что может повлиять на экологический баланс. Чтобы нейтрализовать кислотность, в сточные воды можно добавлять соль карбоната кальция в соответствующих количествах, поскольку она производит бикарбонат, который нейтрализует воду. Представлены уравнения, участвующие в процессе:
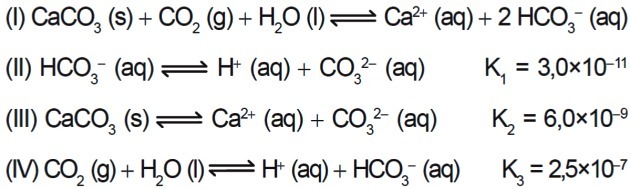
Исходя из значений констант равновесия реакций II, III и IV при 25 ° C, каково численное значение константы равновесия реакции I?
а) 4,5 х 10-26
б) 5,0 х 10-5
в) 0,8 х 10-9
г) 0,2 х 105
д) 2,2 х 1026
Правильный ответ: б) 5,0 х 10-5
1-й шаг: используйте закон Гесса, чтобы внести необходимые поправки.
Учитывая химическое уравнение:
Константа рассчитывается по формуле:
Но если перевернуть уравнение, мы получим в результате:
И константа становится обратной:
Чтобы прийти к уравнению 1, заданному в вопросе, нам нужно обратить уравнение II, как в предыдущем примере.
2-й шаг: манипулируйте уравнениями II, III и IV, чтобы получить результат уравнения I.
3-й шаг: вычислить константу равновесия уравнения I.
Расчет Kя выполняется путем умножения постоянных значений.
Поскольку в расчете у нас есть равные степени оснований, мы повторяем основание и складываем показатели.
Поскольку теперь у нас есть деление с равными степенями оснований, мы повторяем основание и вычитаем показатели степени.
8. (UnB) Пентахлорид фосфора - очень важный реагент в органической химии. Его получают в газовой фазе по реакции:
Колба емкостью 3,00 л содержит при равновесии при 200 ° C 0,120 моль PCl.5(грамм), 0,600 моль ПКл3(грамм) и 0,0120 моль CL2(грамм). Какое значение имеет константа равновесия при этой температуре?
Правильный ответ: 50 (моль / л)-1
1-й шаг: Составьте выражение константы равновесия для реакции.
2-й шаг: рассчитайте концентрации в моль / л каждого компонента в состоянии равновесия.
Формула молярной концентрации:
| PCl3 | Cl2 | PCl5 |
3-й шаг: замените концентрации в постоянном выражении и вычислите значение Kç.
Приложения для равновесия равновесия
9. (Enem / 2016) После полного износа шины можно сжигать для выработки энергии. Среди газов, образующихся при полном сгорании вулканизированной резины, некоторые являются загрязнителями и вызывают кислотные дожди. Чтобы предотвратить их утечку в атмосферу, эти газы можно барботировать в водный раствор, содержащий подходящее вещество. Обратите внимание на информацию о веществах, указанную в таблице.
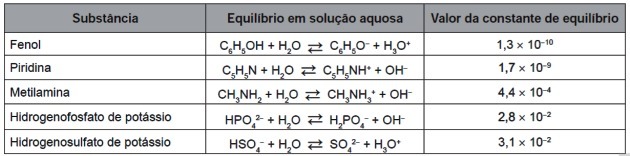
Среди веществ, перечисленных в таблице, наиболее эффективно удалять загрязняющие газы способно (а)
а) Фенол.
б) Пиридин.
в) Метиламин.
г) гидрофосфат калия.
д) Гидросульфат калия.
Правильный ответ: г) Гидрофосфат калия.
сотрудничество2, оксиды серы (SO2 и другие3) и оксидов азота (NO и NO2) являются основными загрязняющими газами.
Когда они вступают в реакцию с водой, присутствующей в атмосфере, возникает образование кислоты которые вызывают повышение кислотности дождя, поэтому его называют кислотным дождем.
Константы равновесия, приведенные в таблице, рассчитываются по соотношению концентраций продуктов и реагентов следующим образом:
Обратите внимание, что константа равновесия пропорциональна концентрации продуктов: чем больше количество продуктов, тем больше значение Kç.
Обратите внимание на значения первой и последней композиции в таблице для Kç:
| пиридин | ||
| Гидросульфат калия |
Сравнивая два числа, мы видим, что чем меньше отрицательная степень, тем больше значение константы.
Для более эффективного удаления загрязняющих веществ OH- реагировать с ионами H+ присутствует в кислотах через реакция нейтрализации.
Среди представленных веществ те, которые производят гидроксилы, необходимые для нейтрализации кислотных соединений, включают: пиридин, метиламин и гидрофосфат калия.
Чтобы выяснить, какое соединение наиболее эффективно, мы наблюдаем константы равновесия: чем выше значение константы, тем больше концентрация OH.-.
Таким образом, водный раствор, содержащий подходящее для этой цели вещество, представляет собой гидрофосфат калия, так как он более щелочной и более эффективно нейтрализует кислоты.
Чтобы узнать больше, прочтите эти тексты.:
- ионный баланс
- Реакция нейтрализации
10. (Enem / 2009) Мыла - это соли длинноцепочечных карбоновых кислот, используемые для облегчения, во время процессов стирки удаление веществ с низкой растворимостью в воде, например масел и жиры. На следующем рисунке представлена структура молекулы мыла.
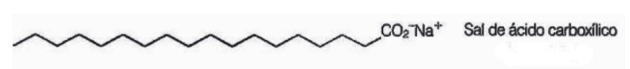
В растворе анионы мыла могут гидролизовать воду и тем самым образовывать соответствующую карбоновую кислоту. Например, для стеарата натрия устанавливается следующий баланс:
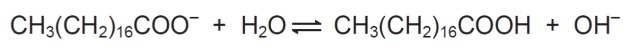
Поскольку образующаяся карбоновая кислота плохо растворяется в воде и менее эффективно удаляет жиры, рН среды необходимо контролировать, чтобы не допустить смещения указанного выше баланса вправо.
Основываясь на информации в тексте, можно сделать вывод, что мыло действует следующим образом:
а) Более эффективен при щелочном pH.
б) Более эффективен при кислом pH.
в) Более эффективен при нейтральном pH.
г) Эффективен в любом диапазоне pH.
д) Более эффективен при кислом или нейтральном pH.
Ответ: а) Более эффективен при основном pH.
В показанном балансе мы видим, что стеарат натрия при взаимодействии с водой образует карбоновую кислоту и гидроксил.
Цель регулирования pH - не допустить образования карбоновой кислоты, и это достигается смещением баланса путем изменения концентрации OH.-.
тем более ОН- в растворе происходит нарушение на стороне продуктов, и химическая система реагирует, потребляя вещество, концентрация которого увеличилась, в данном случае гидроксил.
Следовательно, произойдет превращение продуктов в реагенты.
Следовательно, мыло наиболее эффективно работает при основном pH, поскольку избыток гидроксила смещает баланс влево.
Если бы pH был кислым, концентрация H была бы выше.+ что повлияет на баланс, потребляя ОН- и баланс будет действовать, производя больше гидроксила, смещая баланс влево и производя больше карбоновой кислоты, что не представляет интереса в представленном процессе.
Сдвиг химического равновесия
11. (Enem / 2011) Безалкогольные напитки все чаще становятся объектом политики общественного здравоохранения. Клеевые продукты содержат фосфорную кислоту - вещество, которое вредно для фиксации кальция, минерала, который является основным компонентом зубного матрикса. Кариес - это динамический процесс дисбаланса в процессе деминерализации зубов, потери минералов из-за кислотности. Известно, что основным компонентом зубной эмали является соль гидроксиапатита. Сода из-за присутствия сахарозы снижает pH биопленки (бактериального налета), вызывая деминерализацию зубной эмали. Механизмам защиты слюны требуется от 20 до 30 минут, чтобы нормализовать уровень pH и реминерализовать зуб. Следующее химическое уравнение представляет этот процесс:
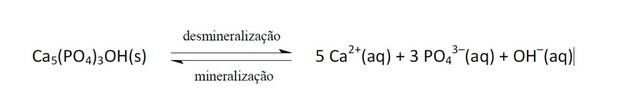 ГРОЙСМАН, С. Воздействие соды на зубы оценивается без отмены диеты. Доступно в: http://www.isaude.net. Доступ: 1 мая 2010 г. (адаптировано).
ГРОЙСМАН, С. Воздействие соды на зубы оценивается без отмены диеты. Доступно в: http://www.isaude.net. Доступ: 1 мая 2010 г. (адаптировано).
Учитывая, что человек употребляет безалкогольные напитки ежедневно, может произойти процесс деминерализации зубов из-за повышенной концентрации
а) ОН–, который реагирует с ионами Ca2+, смещая баланс вправо.
б) H+, который реагирует с гидроксилами ОН–, смещая баланс вправо.
в) ОН–, который реагирует с ионами Ca2+, смещая баланс влево.
г) H+, который реагирует с гидроксилами ОН–, смещая баланс влево.
д) Ca2+, который реагирует с гидроксилами ОН–, смещая баланс влево.
Правильный ответ: б) Н+, который реагирует с гидроксилами ОН–, смещая баланс вправо.
Когда pH снижается, это происходит из-за увеличения кислотности, то есть концентрации ионов H+, как говорится в заявлении, присутствует фосфорная кислота.
Эти ионы реагируют с ОН- заставляя это вещество потребляться и, следовательно, сдвигать баланс вправо, поскольку система действует, производя больше этих удаленных ионов.
Смещение равновесия между реагентами и продуктами произошло из-за уменьшения концентрации ОН.-.
Если ионы Са2+ и ох- если бы концентрация увеличилась, это сместило бы баланс влево, поскольку система реагировала бы, потребляя их и образуя больше гидроксиапатита.
Изменение предыдущего баланса, связанного с утечкой хладагента при описанных условиях, приводит к:
а) выброс CO2 для окружающей среды.
б) Повышение температуры контейнера.
в) Повышение внутреннего давления в емкости.
г) Повышение концентрации CO2 в жидкости.
д) образование значительного количества H2О.
Правильный ответ: а) выброс СО2 для окружающей среды.
Внутри бутылки углекислый газ растворялся в жидкости из-за высокого давления.
Когда бутылка открыта, давление внутри контейнера (которое было больше) равно давлению в окружающей среде, и при этом происходит утечка углекислого газа.
Смещение равновесия между реагентами и продуктами произошло из-за снижения давления: при понижении давления равновесие смещается к наибольшему объему (количеству молей).
Реакция сместилась влево и СО2 который был растворен в жидкости, вытекла при открытии бутылки.