О балансировка уравнений позволяет нам сопоставить количество атомов, присутствующих в химическом уравнении, чтобы оно стало истинным и представляло собой химическую реакцию.
Используйте приведенные ниже вопросы, чтобы проверить свои знания, и проверьте ответы, прокомментированные после отзыва, чтобы ответить на свои вопросы.
Вопрос 1
(Маккензи-СП)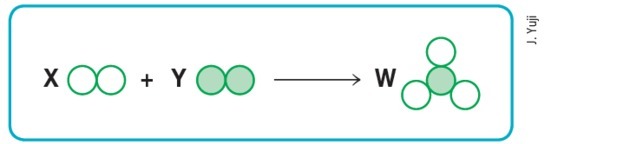
Если предположить, что пустые и темные кружки соответственно означают разные атомы, то схема выше будет представлять собой сбалансированную химическую реакцию, если мы заменим буквы X, Y и W соответственно на значения:
а) 1, 2 и 3.
б) 1, 2 и 2.
в) 2, 1 и 3.
г) 3, 1 и 2.
д) 3, 2 и 2.
Альтернатива d) 3, 1 и 2.
1 шаг: Мы назначаем буквы, чтобы уравнение было легче понять.
2 шаг: мы складываем индексы, чтобы узнать, у кого больше всего атомов в уравнении.
| THE | |
| B |
A и B появляются только один раз в каждом члене уравнения. Однако, если мы сложим индексы, мы увидим, что A имеет наибольшее значение. Поэтому мы приступили к балансировке за него.
3 шаг: Мы уравновешиваем элемент A, переставляя индексы и превращая их в коэффициенты.
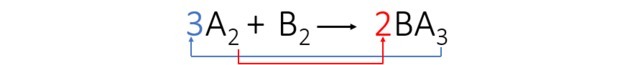
Мы заметили, что элемент B был автоматически сбалансирован, а коэффициенты уравнения равны: 3, 1 и 2.
вопрос 2
(Unicamp-SP) Прочтите следующее предложение и преобразуйте его в (сбалансированное) химическое уравнение, используя символы и формулы: «молекула газообразного азота, содержащая два атома азота на молекулу, реагирует с тремя молекулами двухатомного газообразного водорода, образуя две молекулы газообразного аммиака, который состоит из трех атомов водорода и одного из азот ».
Отвечать:
Представляя атомы, описанные в вопросе, мы можем понять, что реакция происходит следующим образом:
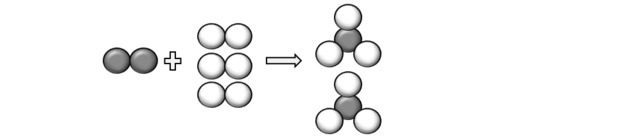
Итак, мы приходим к уравнению:
вопрос 3
Перекись водорода - это химическое соединение, которое может разлагаться с образованием воды и кислорода в соответствии с химическим уравнением, приведенным ниже.
Что касается этой реакции, правильно сбалансированное уравнение:
а) H2О2 → The2 + H2О
б) 2ч2О2 → The2 + 2H2О
в) H2О2 → 2O2 + H2О
г) 2ч2О2 → 2O2 + 2H2О
Правильная альтернатива: б) 2H2О2 → The2 + 2H2О
Обратите внимание, что перекись водорода - это химическое вещество, состоящее из атомов двух химических элементов: водорода и кислорода.
После реакции разложения у вас должно быть одинаковое количество атомов двух элементов как в реагентах, так и в продуктах. Для этого нам нужно сбалансировать уравнение.
Обратите внимание, что у нас есть 2 атома водорода в реагенте (H2О2) и два атома в произведении (H2О). Однако кислород имеет два атома в реагенте (H2О2) и три атома в продуктах (H2О и О2).
Если поставить коэффициент 2 перед перекисью водорода, мы удвоим количество атомов элементов.
Обратите внимание, что если мы сопоставим один и тот же коэффициент с формулой для воды, у нас будет одинаковое количество атомов с обеих сторон.
Следовательно, правильно сбалансированное химическое уравнение - 2H2О2 → The2 + 2H2О.
вопрос 4
(UFPE) Рассмотрим химические реакции ниже.
Можно сказать, что:
а) все уравновешены.
б) 2, 3 и 4 сбалансированы.
в) сбалансированы только 2 и 4.
г) только 1 неуравновешен.
д) ни один из них не сбалансирован правильно, потому что физические состояния реагентов и продуктов различны.
Вариант б) 2, 3 и 4 сбалансированы.
Варианты 1 и 5 неверны, потому что:
- Уравнение 1 неуравновешено, правильный баланс будет:
- Уравнение 5 неверно, поскольку в реакции образуется соединение H2ТОЛЬКО3.
Чтобы сформировать H2ТОЛЬКО4 должно быть включено в уравнение окисления SO2.
вопрос 5
(Mackenzie-SP) При нагревании до 800 ° C карбонат кальция разлагается на оксид кальция (чистая известь) и диоксид углерода. Правильно сбалансированное уравнение, соответствующее описанному явлению, выглядит следующим образом:
(Дано: Ca - щелочноземельный металл.)
Альтернатива c)
Кальций - это щелочноземельный металл, и для стабильности кальций требуется 2 электрона (Ca2+), который представляет собой заряд кислорода (O2-).
Таким образом, атом кальция связывается с атомом кислорода, и образуется соединение CaO, которое представляет собой негашеную известь.
Другой продукт - диоксид углерода (CO2). Оба образованы карбонатом кальция (CaCO3).
Представьте это в уравнении:
Отметим, что количество атомов уже правильное и не требует балансировки.
вопрос 6
(UFMG) Уравнение не сбалансирован. Уравновешивая это с наименьшими возможными числами, сумма стехиометрических коэффициентов будет:
а) 4
б) 7
в) 10
г) 11
д) 12
Альтернатива e) 12
При использовании пробного метода порядок балансировки будет:
1 шаг: Поскольку элемент, который появляется только один раз в каждом члене и имеет самый высокий индекс, - это кальций, мы начали балансировать для него.
2-й шаг: Следим за балансировкой по радикальному ПО43-, который также появляется только один раз.
3-й шаг: балансируем водород.
При этом мы видим, что количество кислорода было скорректировано автоматически, и баланс уравнения следующий:
Помните, что когда коэффициент равен 1, вам не нужно записывать его в уравнение.
Складывая коэффициенты, получаем:
вопрос 7
Горение - это тип химической реакции, при которой энергия выделяется в виде тепла.
При полном сгорании вещества, образованного углеродом и водородом, образуются углекислый газ и вода.
Наблюдайте за реакциями горения углеводородов и ответьте, какое из приведенных ниже уравнений сбалансировано неправильно:
а) CH4 + 2O2 → CO2 + 2H2О
до н.э3ЧАС8 +502 → 3CO2 + 4H2О
в) С4ЧАС10 + 13 / 3O2 → 4СО2 + 5ч2О
Округ Колумбия2ЧАС6 + 7 / 2O2 → 2CO2 + 3H2О
Неправильный ответ: в) В4ЧАС10 + 13 / 3O2 → 4СО2 + 5ч2О
Чтобы сбалансировать химические уравнения, давайте сначала посмотрим, какой элемент появляется только один раз в каждом члене уравнения.
Обратите внимание, что углерод и водород образуют только один реагент и один продукт в каждом представленном уравнении.
Итак, давайте начнем балансировать с водородом, поскольку он имеет большее количество атомов.
Следовательно, порядок балансировки будет таким:
- Водород
- Углерод
- Кислород
Водород
Поскольку продукт содержит 2 атома водорода, мы вставляем число в качестве коэффициента, умножение которого на 2 дает количество атомов водорода в реагенте.
а) CH4 + O2 → CO2 + 2ЧАС2О
до н.э3ЧАС8 + O2 → CO2 + 4ЧАС2О
в) С4ЧАС10 + O2 → CO2 + 5ЧАС2О
Округ Колумбия2ЧАС6 + O2 → CO2 + 3ЧАС2О
Углерод
Уравновешивание осуществляется путем транспонирования углеродного индекса в реагенте и использования его в качестве коэффициента для продукта, который имеет атомы этого элемента.
а) CH4 + O2 → 1CO2 + 2H2О
до н.э3ЧАС8 + O2 → 3CO2 + 4H2О
в) С4ЧАС10 + O2 → 4CO2 + 5ч2О
Округ Колумбия2ЧАС6 + O2 → 2CO2 + 3H2О
Кислород
Складывая количество атомов кислорода в образовавшихся продуктах, мы находим количество атомов элемента, которые должны вступить в реакцию.
Для этого мы должны ввести в качестве коэффициента число, умноженное на 2, и получится количество атомов кислорода в продуктах.
а) CH4 + O2 → 1СО2 + 2H2О
2х = 2 + 2
2x = 4
х = 2
Итак, правильное уравнение: CH4 + 2О2 → 1СО2 + 2H2О.
до н.э3ЧАС8 + O2 → 3CO2 + 4H2О
2х = 6 + 4
2x = 10
х = 5
Итак, правильное уравнение: C3ЧАС8 + 5О2 → 3CO2 + 4H2О
в) С4ЧАС10 + O2 → 4СО2 + 5ч2О
2х = 8 + 5
2x = 13
х = 13/2
Итак, правильное уравнение: C4ЧАС10 + 13/2О2 → 4СО2+ 5ч2О
Округ Колумбия2ЧАС6 + O2 → 2CO2 + 3H2О
2х = 4 + 3
2x = 7
х = 7/2
Итак, правильное уравнение: C2ЧАС6 + 7/2О2 → 2CO2 + 3H2О
Правильно сбалансированные уравнения:
а) CH4 + 2O2 → CO2 + 2H2О
до н.э3ЧАС8 +502 → 3CO2 + 4H2О
в) С4ЧАС10 + 13 / 2O2 → 4СО2 + 5ч2О
Округ Колумбия2ЧАС6 + 7 / 2O2 → 2CO2 + 3H2О
Таким образом, альтернатива c) C4ЧАС10 + 13 / 3O2 → 4СО2 + 5ч2Причина в том, что у него нет правильного баланса.
вопрос 8
(Enem 2015) Известняки - это материалы, состоящие из карбоната кальция, который может действовать как сорбенты для диоксида серы (SO2), важный загрязнитель воздуха. Реакциями, участвующими в процессе, являются активация известняка путем кальцинирования и фиксация SO.2 с образованием соли кальция, как показано упрощенными химическими уравнениями.
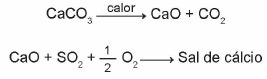
Учитывая реакции, участвующие в этом процессе обессеривания, химическая формула соли кальция соответствует:
Альтернатива б)
Поскольку реакция уравновешена, атомы, содержащиеся в реагентах, должны находиться в продуктах в одинаковом количестве. Таким образом,
Образовавшаяся соль состоит из:
1 атом кальция = Ca
1 атом серы = S
4 атома кислорода = O4
Следовательно, химическая формула кальциевой соли соответствует CaSO.4.
вопрос 9
(UFPI) Реакция X с Y показана ниже. Определите, какое уравнение наилучшим образом представляет сбалансированное химическое уравнение.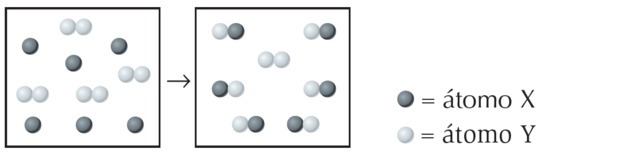
Альтернатива а)
На рисунке мы видим, что разновидность X представляет собой одиночный атом, а Y - двухатомный, то есть образованный соединением 2 атомов. Итак, X реагирует с Y2.
Образовавшийся продукт представлен XY, уравнение неуравновешено:
Балансируем уравнение следующим образом:
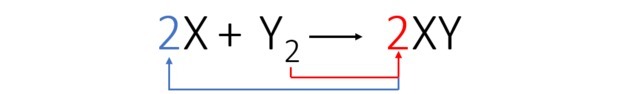
Согласно сбалансированному уравнению, на рисунке ниже показано, как происходит реакция и ее пропорции.
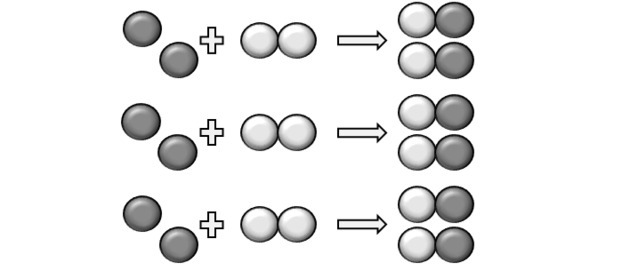
Чтобы реакция произошла, должно быть фиксированное соотношение, и поэтому некоторые соединения могут не вступать в реакцию. Это то, что показано на рисунке, потому что в продукте мы видим, что Y2 не отреагировал.
вопрос 10
(Enem 2010) Мобилизация, направленная на улучшение планеты для будущих поколений, становится все более частой. Большинство видов общественного транспорта в настоящее время работают на ископаемом топливе. В качестве примера бремени, вызванного такой практикой, достаточно знать, что автомобиль производит в среднем около 200 г углекислого газа на километр пути.
Журнал "Глобальное потепление". Год 2, 8. Публикация Instituto Brasileiro de Cultura Ltda.
Одна из основных составляющих бензина - октан (C8ЧАС18). За счет сгорания октана можно высвободить энергию, позволяющую автомобилю начать движение. Уравнение, представляющее химическую реакцию этого процесса, демонстрирует, что:
а) при этом выделяется кислород в виде O2.
б) стехиометрический коэффициент для воды составляет 8 к 1 октану.
в) в процессе происходит потребление воды, так что выделяется энергия.
г) стехиометрический коэффициент по кислороду составляет от 12,5 до 1 октана.
д) стехиометрический коэффициент для диоксида углерода составляет от 9 до 1 октана.
Альтернативный вариант d) стехиометрический коэффициент для кислорода составляет от 12,5 до 1 октана.
При балансировке уравнения находим следующие коэффициенты:
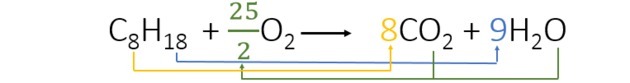
- Мы начали балансировку по водороду, который появляется только один раз в каждом члене и имеет более высокий индекс. Поскольку реагирующих атомов водорода 18, в произведении их 2, поэтому нам нужно добавить число, которое умножается на 2 и дает 18. Итак, 9 - это коэффициент.
- Затем добавляем коэффициент 8 перед CO2 иметь 8 атомов углерода в каждом члене уравнения.
- Наконец, просто добавьте количество кислорода в продукт и найдите значение, умноженное на 2, дает нам 25 атомов кислорода. Итак, мы выбрали 25/2 или 12,5.
Таким образом, на сжигание 1 октана расходуется 12,5 кислорода.
вопрос 11
(Fatec-SP) Важной характеристикой удобрений является их водорастворимость. Таким образом, промышленность по производству удобрений превращает фосфат кальция, растворимость которого в воде очень низка, в гораздо более растворимое соединение, которым является суперфосфат кальция. Этот процесс представлен уравнением:
где значения x, y и z соответственно равны:
а) 4, 2 и 2.
б) 3, 6 и 3.
в) 2, 2 и 2.
г) 5, 2 и 3.
д) 3, 2 и 2.
Альтернатива e) 3, 2 и 2.
Используя алгебраический метод, мы составляем уравнения для каждого элемента и приравниваем количество атомов в реагенте к количеству атомов в продукте. Следовательно:
Сбалансированное уравнение:
вопрос 12
Сбалансируйте приведенные ниже уравнения с помощью пробного метода.
Отвечать:
Уравнение состоит из элементов водорода и хлора. Балансируем элементы, просто добавляя коэффициент 2 перед продуктом.
Уравнение не требовалось балансировать, так как количество атомов уже отрегулировано.
Фосфор имеет два атома в реагентах, поэтому, чтобы сбалансировать этот элемент, мы доводим количество фосфорной кислоты в продукте до 2H.3ПЫЛЬ4.
После этого мы заметили, что водород имеет 6 атомов в продукте, мы уравновесили количество этого элемента, добавив коэффициент 3 к реагенту, который его содержит.
С помощью предыдущих шагов было скорректировано количество кислорода.
Глядя на уравнение, мы видим, что количество водорода и брома в продуктах вдвое больше, чем если есть в реагентах, поэтому мы добавляем коэффициент 2 к HBr, чтобы уравновесить эти два элементы.
Хлор имеет 3 атома в продуктах и только 1 в реагентах, поэтому мы уравновешиваем, ставя коэффициент 3 перед HCl.
Водород имеет 3 атома в реагентах и 2 атома в продуктах. Чтобы скорректировать количества, мы преобразуем индекс H2 в коэффициенте мы умножаем на 3, который уже был в HCl, и получаем результат 6HCl.
Мы регулируем количество хлора в продуктах, чтобы также было 6 атомов, и получаем 2AlCl.3.
В продуктах алюминия было 2 атома, мы довели количество в реагентах до 2Al.
Балансируем количество водорода в продукте до 3H2 и мы помещаем количество 6 атомов этого элемента в каждый член уравнения.
В уравнении нитратный радикал (NO3-) имеет индекс 2 в продукте, преобразуем индекс в коэффициент в реагенте для 2AgNO3.
Количество серебра необходимо было скорректировать, так как теперь у него в реагентах 2 атома, поэтому в продукте есть 2Ag.
В реагентах у нас есть 4 атома водорода, и чтобы сбалансировать этот элемент, мы добавляем коэффициент 2 к продукту HCl.
Теперь хлор содержит 4 атома в продуктах, поэтому мы устанавливаем количество в реагенте 2Cl.2.
У нас есть 6 атомов водорода в реагентах, и чтобы сбалансировать этот элемент, мы доводим количество воды до 3H.2О.
У нас есть 2 атома углерода в реагентах, и чтобы сбалансировать этот элемент, мы устанавливаем количество углекислого газа до 2CO.2.
Кислород должен иметь 7 атомов в реагентах, и чтобы сбалансировать этот элемент, мы устанавливаем количество молекулярного кислорода до 30.2.
Глядя на уравнение, нитратный радикал (NO3-) имеет индекс 2 в продукте. Преобразуем показатель в коэффициент 2 в реагенте AgNO3.
У нас есть 2 атома серебра в реагентах, и чтобы сбалансировать этот элемент, мы доводим количество хлорида серебра в продукте до 2AgCl.
У нас есть 3 атома кальция в продукте, и чтобы сбалансировать этот элемент, мы устанавливаем количество нитрата кальция в реагенте на 3Ca (NO3)2.
У нас остается 6 радикалов NO.3- в реагентах и чтобы сбалансировать этот радикал, мы доводим количество азотной кислоты в продуктах до 6HNO3.
Теперь у нас есть 6 атомов водорода в продуктах, и чтобы сбалансировать этот элемент, мы доводим количество фосфорной кислоты в реагенте до 2H.3ПЫЛЬ4.
Узнайте больше о расчетах с химическими уравнениями по адресу:
- Уравновешивание химических уравнений
- Стехиометрия
- Стехиометрические расчеты
- Упражнения по стехиометрии
- Упражнения по таблице Менделеева
