Некоторым соединениям не нужно иметь восемь электронов в валентной оболочке для достижения стабильности, поэтому они считаются исключениями из правила Октета. Теперь узнайте, почему некоторые элементы избегают обязательства иметь октет электронов в последней оболочке.
Бериллий (Быть)
Это исключение из правила Октета, поскольку оно способно образовывать соединения с двумя одинарными связями, поэтому оно стабилизируется только с четырьмя электронами в валентной оболочке. 
Поскольку водород (H) должен отдать два электрона, чтобы образовалась связь (H - Хорошо - H), атом бериллия (Be) делится своими электронами и достигает стабильности.
Алюминий (Al)
Это исключение из правила Октета, потому что оно обеспечивает стабильность с шестью электронами в валентной оболочке. Атом алюминия имеет тенденцию отдавать свои электроны и поэтому может образовывать три одинарные связи с другими атомами: 
В этом случае алюминий (Al) образовал три связи с тремя атомами фтора (F).
Бор (В)
Он образует молекулярные вещества с тремя одинарными связями.
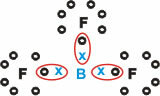
Обратите внимание, что бор (B) имеет тенденцию отдавать свои электроны атомам фтора (F), что подчиняется правилу октета, требующему восемь электронов в валентной оболочке. Поскольку бор отдает свои электроны, фтор стабилизируется с образованием октета.
Лирия Алвес
Окончила химический факультет
Бразильская школьная команда
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Узнать больше!
Теория октетов
Общая химия - Химия - Бразильская школа
Хотели бы вы ссылаться на этот текст в учебе или учебе? Посмотрите:
SOUZA, Líria Alves de. «Исключения из правила октетов»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/excecoes-regra-octeto.htm. Доступ 27 июня 2021 г.