Идеи о строении материи (атома) возникли в Древней Греции около 450 г. до н.э. а., главным образом, из Демокрито и Леучипо. Однако фактически атом получил научный характер только после так называемого Атомная теория Дальтона.
THE Атомная теория Дальтона он был фундаментальным для развития атомных знаний, так как он служил основой для других ученых, чтобы узнать атом и его характеристики.
Кто был Джон Далтон?
Джон Далтон, химик по образованию, родился в Камбрии, Англия, в 1766 году и умер в Манчестере в 1844 году. С раннего возраста его жизнь была предназначена для научных исследований и преподавания, причем настолько, что он преподавал или способствовал развитию различных областей знаний.
Однако его величайшим наследием как ученого было развитие первой теории атома. Именно благодаря нескольким экспериментам, связанным со смесью газов, и знанию работ, предложенных Лавуазье, в 1808 году возникла атомная теория Дальтона.
Постулаты атомной теории Дальтона
Атомная теория Дальтона была основана на экспериментах, но ни один из этих экспериментов не смог четко выявить атом. Поэтому Дальтон назвал атом мельчайшей частицей материи.
В теории Далтона гораздо больше постулатов, чем доказательств. Посмотрите некоторые из них:
Атомы массивные и сферические по форме (похожи на бильярдный шар);
Атомы неделимы;
Атомы неразрушимы;
Один химический элемент это набор атомов с одинаковыми свойствами (размером и массой);
Атомы разных химических элементов имеют разные свойства друг от друга;
Относительный вес двух атомов можно использовать для их различения;
Составное химическое вещество образуется из одной и той же комбинации различных типов атомов;
Различные химические вещества образуются путем объединения разных атомов.
Представления модели атома Дальтона
Дальтон назвал свою атомную модель бильярдным шаром и поэтому начал представлять атомы элементов, известных в его время, с помощью сферических символов.
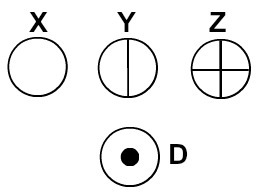
Атомы представлены согласно атомной теории Дальтона
Каждое атомное представление, имеющее определенную деталь, указывает на другой химический элемент. Дидактически в книгах и упражнениях начального и среднего уровня атомы представлены только сферами разного цвета.
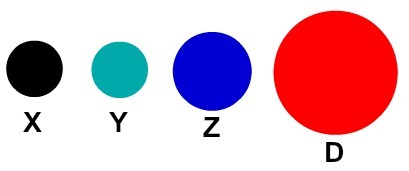
Дидактическое представление атомов
Вклад атомной теории Дальтона
-
понимание Закон сохранения массы Лавуазье
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Французский химик Лавуазье утверждал в 1785 году, что «В химической реакции масса сохраняется, потому что нет ни создания, ни разрушения атомов. ”. Атомная теория Дальтона доказала этот факт, поскольку один из его постулатов утверждает, что атом неуничтожим.
Следовательно, если мы проводим сжигание угля (C) в присутствии газообразного кислорода (O2), мы будем иметь химическую реакцию между одним атомом углерода и двумя атомами кислорода. В этой реакции образуется диоксид углерода (CO2), который имеет точно такие же атомы, которые составляли вещества до реакции.
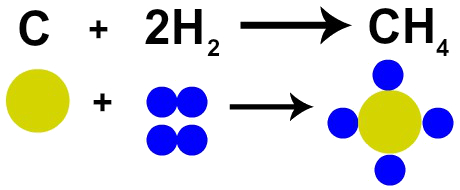
Представление закона Лавуазье атомной моделью Дальтона
понимание простые вещества
С помощью Атомная модель Дальтона, мы можем понять простое вещество, то есть такое, которое имеет атомы с одинаковыми характеристиками, образующие молекулу. Следовательно, у нас есть атомы, принадлежащие одному химическому элементу.
По существу F2Например, у нас есть два атома фтора, поэтому мы должны использовать два типа одинаковых атомов в представлении согласно атомной теории Дальтона.

Простое представление вещества согласно Атомная модель Дальтона
понимание сложные вещества
В составном веществе молекулы образуют атомы с разными характеристиками. Следовательно, у нас есть разные химические элементы, образующие вещество.
Вещество H2О, например, имеет три атома: два водорода и один кислород. Посмотрите его представление согласно атомной модели Дальтона:
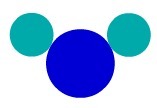
Представление составного вещества по кожеАтомная модель Дальтона
Понимание смесей
Понимание смеси (объединения двух или более разных веществ) с помощью атомной теории Дальтона простое: просто поместите две разные молекулы в один и тот же контейнер.

Представление второй смеси Атомная модель Дальтона
Другие научные вклады Джона Далтона
представил концепцию атомная масса;
Сформулировал закон парциальных давлений газов (Закон Дальтона);
Обнаружено нарушение зрения под названием дальтонизм;
Изучал поведение паров и газов при разных температурах;
Он обнаружил, что все газы расширяются (они пытаются занять определенное место) в пространстве одинаково.
Автор: Диого Лопес Диас
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
ДНИ, Диого Лопес. «Атомная теория Дальтона»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/teoria-atomica-dalton.htm. Доступ 27 июня 2021 г.