Полярность связи и молекулы связана с распределением электронов вокруг атомов.Если это распределение симметрично, молекула будет неполярной, но если она асимметрична, то молекула будет неполярной. и одна из частей молекулы имеет более высокую электронную плотность, поэтому это полярная молекула.
Полярность молекул можно визуализировать, когда составляющая их субстанция подвергается воздействию внешнего электрического поля. Если молекулы ориентируются в присутствии этого поля, то есть, если одна часть притягивается к положительному полюсу, а другая часть молекулы - к отрицательному полюсу, тогда, они полярны. Иначе, если они не ориентируются, они неполярны.
Например, если вы сильно потрете стеклянную палочку о фланель, она станет положительно заряженной. Если мы подойдем к струе воды, падающей из крана, мы увидим, что вода не будет продолжать падать по прямой вертикальной траектории, а будет притягиваться палкой, претерпевая отклонение. Это показывает, что вода полярна. Но если мы проделаем тот же эксперимент с масляной филе, она не изменит свою траекторию, показывая, что его молекулы неполярны.
Анализируя структуру молекул, мы можем определить, полярны они или нет, учитывая два важных фактора: разница в электроотрицательности между атомами и геометрия молекулы.
1) Электроотрицательность между атомами:
Если молекула образована связями между атомами одних и тех же химических элементов, то есть если это простые вещества, такие как O2, H2, нет2, Cℓ2, П4, S8и т. д., они будут неполярными, потому что между их атомами нет разницы в электроотрицательности.
Единственное исключение - молекула озона (O3), что будет видно позже.
Если молекула двухатомная и образована элементами с разной электроотрицательностью, то молекула будет полярной. Примеры: HCℓ, HF, HBr и HI.
2-й) Геометрия молекулы:
Геометрия молекулы влияет на то, как в ней будут распределяться электроны и, следовательно, на ее полярность. Если молекула состоит из трех или более атомов, нам нужно будет проанализировать каждую возникающую связь и геометрию молекулы. См. Пример: CO2 - линейная молекула:
δ- δ+ δ-
О = С = О
Обратите внимание, что кислород более электроотрицателен, чем углерод, поэтому электроны связи больше притягиваются к кислороду. В них образуется частичный отрицательный заряд (δ-), а в углероде образуется частичный положительный заряд (δ+). Умножение расстояния между ядрами атомов, связанных этими зарядами, по модулю (то есть только на число без знака плюс или минус) называется дипольный момент и представлен μ.
μ = d. |δ|
Этот дипольный момент обозначен стрелками, указывающими в направлении наиболее электроотрицательного элемента, притягивающего электроны: O ← C → O. Это показывает, что эта величина является вектором (величиной, имеющей величину или интенсивность, направление и направление). Поэтому лучше всего он представлен:  .
.

Складывая все векторы вместе, находим результирующий дипольный момент, 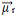 , который в этом случае был равен нулю, потому что два дипольных момента имеют равные значения, но идут в противоположных направлениях, компенсируя друг друга.
, который в этом случае был равен нулю, потому что два дипольных момента имеют равные значения, но идут в противоположных направлениях, компенсируя друг друга.
Когда результирующий вектор дипольного момента равен нулю, молекула неполярна, но если он отличен от нуля, она будет полярной.
Следовательно, в случае молекулы CO2Она аполярна.
Теперь посмотрим на другой пример: H2O - угловая геометрия (потому что у кислорода есть две пары электронов, доступные на самом внешнем уровне, которые отталкивают электроны от связей с атомами водорода):
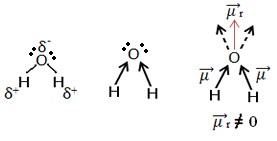
Электроны притягиваются к кислороду. Но в этом случае векторы не компенсируют друг друга, потому что молекулярная геометрия воды угловая, так как ее направления не противоположны, что дает ненулевой результирующий вектор дипольного момента, и поэтому молекула воды полярный.
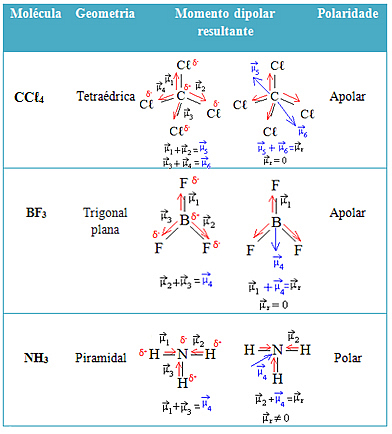
Дополнительные примеры см. В таблице ниже:
Дженнифер Фогача
Окончила химический факультет
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/polaridade-das-moleculas.htm


