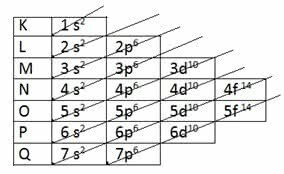
Для классифицируйте сигма-ссылку, важно знать, как распознать его в структуре молекулы. Сигма-связь на самом деле является ковалентной связью, которая происходит, когда две неполные атомные орбитали (только с одним электроном) взаимопроникают на одной оси. Примером может служить орбиталь p-типа (спирали), взаимопроникающая с другой p-орбиталью.

p-орбитали взаимопроникают в p-p сигма-связь
На практике (в упражнениях), Распознавание и классификация сигма-ссылки производится по структурной формуле вещества, как в структурном представлении ниже:

Структурная формула синильной кислоты
Перед тем как классифицировать сигма-ссылку, необходимо уметь распознать это в структурной формуле. Для этого просто помните способы как Ковалентная связь представлен: звонок просто обозначается одиночным тире (-), пара обозначается двумя (=) и ссылкой тройной представлен тремя (≡). Сигма-связь присутствует в любом из трех представлений ковалентных связей следующим образом:
Простой: имеет сигма-связь;
Пара: Из двух ссылок только одно - сигма;
Тройной: Одно из трех звеньев - сигма.
Зная, как распознать сигма-ссылку, следующий шаг - научиться ее ранжировать. Для этого мы должны знать, какова неполная орбиталь каждого атома, участвующего в связи:
ЧАС - представляет собой неполную s-орбиталь, поэтому в классификации она представлена s.
Аметалс- имеют неполную p-орбиталь, поэтому в классификации они представлены p, за исключением следующих элементов:
Углерод: Ваша неполная орбиталь зависит от типа гибридизация что он страдает. Возможные варианты: sp гибридизация3 (сколько стоит четыре простых звонка), зр2 (сколько получается двух одинарных и одной двойной связи) или sp (насколько он выполняет две двойные связи или одну одинарную и одну тройную). Таким образом, в классификации сигма-связи углерод может быть представлен как sp3, sp2 или sp в зависимости от звонка, который вы делаете.
Бериллий:страдать гибридизация sp-типа, таким образом, в классификации представлен пр.
Бор:страдать гибридизация sp-типа2, таким образом, в классификации он представлен пр.2.
Имея всю эту информацию, проще всего классифицировать сигма-ссылки, присутствующие в структуре. Давайте посмотрим на несколько примеров:
Пример 1: сигма-соединения в воде

Структурная формула воды
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Структурная формула выше показывает, что вода имеет две сигма-облигации (два простых), будучи они между кислородом (в лице p) это Водород (представлен s). Таким образом, у нас есть две сигма-ссылки, классифицированные на:
с-п
Пример 2: Сигма-связи в трихлориде фосфора

Структурная формула треххлористого фосфора
Структурная формула выше показывает, что трихлорид фосфора имеет три звонкасигмы (три простых), будучи они войти в фосфор (в лице p) это хлор (в лице p). Таким образом, у нас есть три сигма-ссылки, классифицированные на:
п-п
Пример 3: сигма-связи в трифториде бора
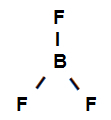
Структурная формула трифторида бора
Структурная формула выше показывает, что трифторид бора имеет три сигма ссылки (три простых), будучи они войти в бор (в лице sp2) это Фтор (в лице p). Таким образом, у нас есть три сигма-ссылки, классифицированные на:
p-sp2
Пример 4: сигма-связи в этаноле
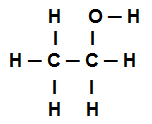
Структурная формула этанола
Структурная формула этанола выше показывает, что у нас в наличии восемь звонков сигмы (восемь простых ссылок). Они:
Один среди кислорода (представлен буквой p) и водород (представлен s). Таким образом, ссылка классифицируется на сигма s-p.
Один из двух атомов углерода которые выполняют только сигма-соединения (а затем в лице sp3). Таким образом, ссылка классифицируется на зр3-П3.
Один среди углерода (в лице sp3) и кислород (в лице p). Таким образом, сигма-ссылка подразделяется на p-sp3.
пять между углеродом (в лице sp3) и водород (представлен s). Таким образом, все пять классифицируются на s-sp3.
Пример 5: Сигма-связи в дихлорэтене

Структурная формула дихлорэтилена
Структурная формула дихлорэтена, приведенная выше, показывает, что мы имеем пять сигм ссылок (четыре одинарные связи и одна из двойных связей). Они:
Один из двух атомов углерода которые выполняют две одинарные и одну двойную связь (а затем в лице sp2). Таким образом, сигма-ссылка подразделяется на зр2-П2.
Четыре между углеродом(представлен sp2)и водород (обозначено буквой s). Таким образом, все четыре классифицируются на s-sp2.
Автор: Диого Лопес Диас
Хотели бы вы ссылаться на этот текст в учебе или учебе? Посмотрите:
ДНИ, Диого Лопес. «Классификация сигма-ссылки»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/classificacao-uma-ligacao-sigma.htm. Доступ 28 июня 2021 г.