Диаграмма Полинга, также известная как Энергетическая диаграмма, - это представление электронного распределения через подуровни мощности.
Используя эту схему, химик Линус Карл Полинг (1901–1994) предложил нечто большее, чем уже было известно о распределении электронов от атомов химических элементов.
Для улучшения настроения Полинг предложил подуровни энергии. С их помощью можно было бы расположить электроны от самого низкого до самого высокого энергетического уровня атома в его основном состоянии.
Электронное распространение Линуса Полинга
Согласно модели, предложенной Полингом, электросфера делится на 7 электронные слои (K, L, M, N, O, P и Q) вокруг атомного ядра, каждый из которых допускает максимальное количество электронов, которое составляет 2, 8, 18, 32, 32, 18 и 8, соответственно.
В распространение электроники в энергетические подуровни, показывая сначала электрон с наименьшей энергией, пока не достигнет электрона с наибольшей энергией.
| Электронные слои | Максимальное количество электронов | Энергетические подуровни | ||||
|---|---|---|---|---|---|---|
| 1 | K | 2 и- | 1 с2 | |||
| 2 | L | 8 и- | 2 с2 | 2p6 | ||
| 3 | M | 18 и- | 3 с2 | 3p6 | 3d10 | |
| 4 | N | 32 и- | 4 с2 | 4p6 | 4d10 | 4f14 |
| 5 | О | 32 и- | 5 с2 | 5p6 | 5d10 | 5f14 |
| 6 | п | 18 и- | 6 с2 | 6p6 | 6d10 | |
| 7 | Q | 8 и- | 7 с2 | 7p6 |
Слой K имеет только один подуровень (и), слой L имеет два подуровня (s и p), слой m имеет три подуровня (s, p и d) и так далее.
Подуровни s допускают до 2 электронов, а подуровни p допускают до 6 электронов. Далее, подуровни d допускают до 10 электронов, а подуровни f допускают до 14 электронов.
Обратите внимание, что сумма электронов, которые ведут себя на каждом подуровне на одну электронную оболочку, дает максимальное количество электронов в каждой из 7 оболочек.
К: с2 = 2
L и Q: s2 + p6 = 8
M и P: s2 + p6 + d10 = 18
N и O: y2 + p6 + d10 + f14= 32
Именно тогда Полинг открыл возрастающий порядок энергии:
1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d10 4p6 5 с2 4d10 5p6 6 с2 4f14 5d10 6p6 7 с2 5f14 6d10 7p6
Оттуда на диаграмме появляются диагональные стрелки, чтобы сделать электронное распределение элементов:
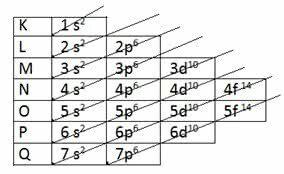 Диаграмма Полинга
Диаграмма Полинга
Пример электронного распределения фосфора 15П:
1 с2 2 с2 2p6 3 с2 3p3
вроде до 3сек2 у нас уже было всего 12 электронов (2 + 2 + 6 + 2), нам нужно еще 3 электрона с подуровня 3p6.
Таким образом, мы можем получить необходимое количество электронов, если оно не превышает 6, что является максимальным количеством, которое подуровень 3p6 ведет себя.
Тоже читай Слой Валенсии а также Квантовые числа.
Решенные упражнения по электронной рассылке
Вопрос 1
(Unirio) «Зубные имплантаты безопаснее в Бразилии и уже соответствуют международным стандартам качества. Большой скачок в качестве произошел в процессе изготовления титановых винтов и штифтов, из которых состоят протезы. Эти протезы, изготовленные из титановых сплавов, используются для фиксации зубных коронок, ортодонтических приспособлений и зубных протезов в костях челюсти и челюсти ». (Jornal do Brasil, октябрь 1996 г.)
Учитывая, что атомный номер титана равен 22, его электронная конфигурация будет следующей:
а) 1 с2 2 с2 2p6 3 с2 3p3
б) 1с2 2 с2 2p6 3 с2 3p5
в) 1 с2 2 с2 2p6 3 с2 3p6 4 с2
г) 1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d2
д) 1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d10 4p6
Правильная альтернатива: г) 1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d2.
Диаграмма Линуса Полинга для распределения электронов в титане:
вопрос 2
(ACAFE) Учитывая любой общий элемент M, имеющий электронную конфигурацию 1s2 2 с2 2p6 3 с2 3p6 4 с2 3d5, можно сказать, что:
Я. его атомный номер 25;
II. имеет 7 электронов в последней оболочке;
III. имеет 5 неспаренных электронов;
IV. принадлежат к семейству 7А.
Утверждения верны:
а) только I, II и III
б) только I и III
в) только II и IV
г) только I и IV
д) только II, III и IV
Правильная альтернатива: б) Только I и III.
Я. ВЕРНЫЙ Подсчитав количество электронов в электронном распределении, мы видим, что было использовано 25. Следовательно, атомный номер 25 и соответствует химическому элементу марганцу.
II. НЕПРАВИЛЬНЫЙ. Последний слой, то есть самый внешний слой, имеет 2 электрона, то есть 4s2.
III. ВЕРНЫЙ Непарные электроны находятся на подуровне d, который содержит до 10 электронов, но в электронном распределении марганца только 5 электронов отнесены к подуровню.
IV. НЕПРАВИЛЬНЫЙ. Марганец находится в семействе 7В и в 4 периоде.
вопрос 3
(UFSC) Число электронов на каждом подуровне атома стронция (38Sr) в порядке возрастания энергии:
а) 1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d10 4p6 5 с2
б) 1с2 2 с2 2p6 3 с2 3p6 4 с2 4p6 3d10 5 с2
в) 1 с2 2 с2 2p6 3 с2 3p6 3d10 4 с2 4p6 5 с2
г) 1 с2 2 с2 2p6 3 с2 3p6 4p6 4 с2 3d10 5 с2
д) 1 с2 2 с2 2p6 3p6 3 с2 4 с2 4p6 3d10 5 с2
Правильная альтернатива: а) 1 с.2 2 с2 2p6 3 с2 3p6 4 с2 3d10 4p6 5 с2.
Диаграмма Линуса Полинга для распределения электронов стронция:
Проверьте свои знания еще больше! Также разрешите:
- Упражнения по электронной дистрибуции
- Упражнения с периодической таблицей