Способность соединений притягивать электрические заряды определяется как полярность, которая принимает различный характер в зависимости от соединения, в котором она присутствует.
Что касается ионной и ковалентной связи, последняя делает молекулу неполярной. Молекула, в которой ионная связь отвечает за удержание атомов вместе, имеет полярность.
Преобладающая связь между органическими соединениями является ковалентной, поэтому они в основном становятся неполярными соединениями. Длинные углеродные цепи, присутствующие в органических веществах, не допускают никаких других признаков, кроме неполярности.
Объяснение исходит из того, что связь происходит между равными элементами. (Ç-Ç), следовательно, у них одинаковая шкала электроотрицательности. См. Пример:

неполярная молекула
Бутан, представленный структурой выше, представляет собой газ, обратите внимание, что связанные атомы одинаковы (4 атома углерода, связанных вместе).
Но это не означает, что каждое органическое соединение неполярно, наличие других атомов между атомами углерода придает молекуле полярный характер. Посмотрите на пример:
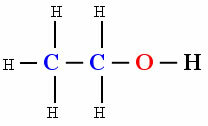
полярная молекула
Наличие гидроксила ой (Кислород, связанный с водородом) заставил молекулу органического соединения этанола проявить полярность.
Бутан используется в качестве газа для зажигалок, а этанол - это так называемый обычный спирт.
Лирия Алвес
Окончила химический факультет
Бразильская школьная команда
Узнать больше!
Свойства органических соединений
Полярность – Узнайте, почему электроотрицательность влияет на полярность вызова.
Полярность ионных и ковалентных связей
Органическая химия - Химия - Бразильская школа
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/polaridade-dos-compostos-organicos.htm

