Ideile despre constituirea materiei (atomul) au apărut în Grecia antică, în jurul anului 450 î.Hr. a., din, în principal, din Democrito și Leucipo. Cu toate acestea, atomul a primit de fapt un caracter științific numai după așa-numitul Teoria atomică a lui Dalton.
THE Teoria atomică a lui Dalton a fost fundamental pentru dezvoltarea cunoașterii atomice, deoarece a servit ca bază pentru ceilalți oameni de știință să cunoască atomul și caracteristicile sale.
Cine a fost John Dalton?
John Dalton, chimist de formare, s-a născut în Cumbria, Anglia, în 1766 și a murit la Manchester în 1844. Încă de la o vârstă fragedă, viața sa a fost destinată cercetării și predării științifice, atât de mult încât a predat sau a contribuit la dezvoltarea diverselor domenii ale cunoașterii.
Cu toate acestea, cea mai mare moștenire ca om de știință a fost dezvoltarea primei teorii atomice. Prin intermediul mai multor experimente legate de amestecul de gaze și de cunoașterea lucrărilor propuse de Lavoisier, teoria atomică a lui Dalton a apărut în 1808.
Postulatele teoriei atomice a lui Dalton
Teoria atomică a lui Dalton s-a bazat pe experimente, dar niciunul dintre aceste experimente nu a putut dezvălui în mod clar atomul. Prin urmare, Dalton a numit atomul cea mai mică parte a materiei.
Teoria lui Dalton prezintă mult mai multe postulate decât dovezi. Vedeți câteva dintre ele:
Atomii au o formă sferică și masivă (similar cu o bilă de biliard);
Atomii sunt indivizibili;
Atomii sunt indestructibili;
unu element chimic este un set de atomi cu aceleași proprietăți (dimensiune și masă);
Atomii diferitelor elemente chimice au proprietăți diferite între ele;
Greutatea relativă a doi atomi poate fi utilizată pentru a le diferenția;
O substanță chimică compusă este formată din aceeași combinație a diferitelor tipuri de atomi;
Diferite substanțe chimice se formează prin combinarea diferiților atomi.
Reprezentări ale modelului atomic Dalton
Dalton a numit modelul său atomic bila de biliard și, prin urmare, a început să reprezinte atomii elementelor cunoscute în zilele sale prin intermediul simbolurilor sferice.
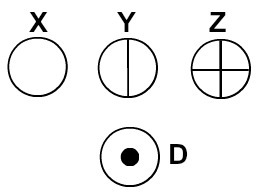
Atomi reprezentați conform teoriei atomice a lui Dalton
Fiecare reprezentare atomică care are un detaliu specific indică un element chimic diferit. În mod didactic cărțile și exercițiile de nivel elementar și mediu reprezintă atomii numai prin sfere cu culori diferite.
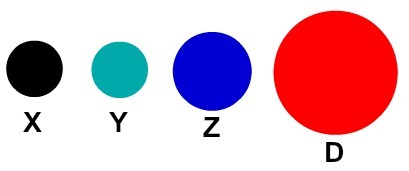
Reprezentarea didactică a atomilor
Contribuții ale teoriei atomice a lui Dalton
intelegerea de Legea lui Lavoisier privind conservarea masei
Chimistul francez Lavoisier a susținut în 1785 că „Într-o reacție chimică, masa este conservată deoarece nu există nici crearea, nici distrugerea atomilor ”. Teoria atomică a lui Dalton a dovedit acest fapt, întrucât unul dintre postulatele sale afirmă că atomul este indestructibil.
Prin urmare, dacă efectuăm arderea cărbunelui (C) în prezența oxigenului gazos (O2), vom avea o reacție chimică între un atom de carbon și doi atomi de oxigen. Această reacție va forma dioxid de carbon (CO2), care are exact aceiași atomi care alcătuiau substanțele înainte de reacție.
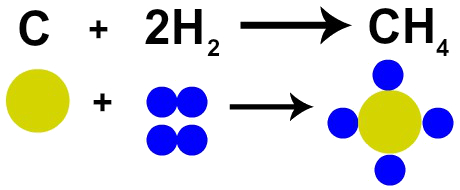
Reprezentarea legii lui Lavoisier de către modelul atomic al lui Dalton
intelegerea de substanțe simple
Folosind Modelul atomic al lui Dalton, putem înțelege o substanță simplă, adică una care are atomi de aceeași caracteristică formând o moleculă. Prin urmare, avem atomi aparținând aceluiași element chimic.
În substanță F2, de exemplu, avem doi atomi de fluor, deci trebuie să folosim două tipuri de atomi egali în reprezentare conform teoriei atomice a lui Dalton.

Reprezentarea simplă a substanței conform Modelul atomic al lui Dalton
intelegerea de substanțe compuse
Într-o substanță compusă, avem atomi de diferite caracteristici care formează molecula. Prin urmare, avem diferite elemente chimice care formează substanța.
Substanța H2O, de exemplu, are trei atomi: doi hidrogen și un oxigen. Vedeți reprezentarea sa după modelul atomic al lui Dalton:
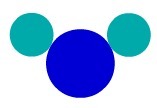
Reprezentarea unei substanțe compuse în funcție de pieleModelul atomic al lui Dalton
Înțelegerea amestecurilor
Înțelegerea unui amestec (unirea a două sau mai multe substanțe diferite) prin teoria atomică a lui Dalton este simplă: pur și simplu puneți două molecule diferite în același recipient.

Reprezentarea unui al doilea amestec Modelul atomic al lui Dalton
Alte contribuții științifice de John Dalton
a introdus conceptul de masă atomică;
A formulat legea presiunilor parțiale a gazelor (Legea lui Dalton);
Am descoperit deficiența de vedere numită daltonism;
Studiat comportamentul vaporilor și gazelor la diferite temperaturi;
El a descoperit că toate gazele se extind (încearcă să ocupe un anumit loc) în spațiu în același mod.
De mine. Diogo Lopes Dias
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/teoria-atomica-dalton.htm


