THE distilare simplă nu este altceva decât o metodă de separarea amestecurilor, folosit special atunci când avem un amestec omogen format dintr-un solid dizolvat într-un lichid, cum ar fi clorura de sodiu (NaCI) în apă.

Clorura de sodiu poate fi obținută prin distilare simplă
Este necesar să înțelegem că, în distilare simplă, apar întotdeauna două transformări fundamentale ale stării fizice, vaporizare (trecerea de la lichid la gaz) și condensare (trecerea de la abur la lichid).
În laborator, să efectueze un distilare simplă, sunt necesare următoarele echipamente:
Arzător Bunsen sau placă de încălzire (1): echipament folosit pentru încălzirea amestecului;
Balon de distilare (2): recipient în care amestecul este ambalat pentru a primi încălzire;
Suport universal (3): echipamente utilizate pentru atașarea ghearelor;
Gheara (4): echipamente utilizate pentru a ține balonul de distilare;
Termometru (5): echipamente utilizate pentru măsurarea temperaturii în timpul experimentului;
Dop (*): material din lemn pentru închiderea capătului superior al balonului de distilare;
Ieșire apă (6): cale prin care iese apa încălzită;
Admisie de apă (7): cale prin care pătrunde apa rece;
Condensator (8): echipamente unde se produce condens în timpul experimentului;
Erlenmeyer sau pahar (9): recipient în care va fi colectat lichidul distilat.
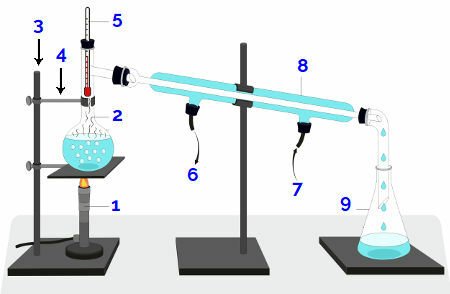
Reprezentarea schematică a unui distilator
În timpul performanței unui distilare simplă, avem următoarele evenimente:
Primul: se organizează echipamentul de distilare;
Al doilea: amestecul (de exemplu apă și clorură de sodiu) se adaugă în balonul de distilare;
Al treilea: încălzirea amestecului se începe în balonul de distilare folosind arzătorul Bunsen sau placa de încălzire;
Cameră: apa începe să se vaporizeze în balonul de distilare;
A cincea: vaporii de apă intră în mod necesar în distilator, deoarece partea superioară a balonului este închisă, transformându-se din nou în lichid;
Şaselea: Lichidul condensat este apoi colectat în paharul sau balonul erlenmeyer.

Reprezentarea lichidului distilat
De mine. Diogo Lopes Dias
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-destilacao-simples.htm