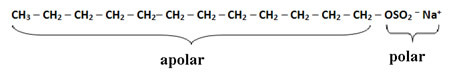
unu reacție de oxidare energetică în alchene apare atunci când există o ruptură a moleculei, adică spargerea simultană a celor două legături duble și a intrarea oxigenului în molecula organică.
Este posibil să se efectueze acest tip de reacție cu alchene atunci când se utilizează permanganat de potasiu (KMnO4) sau dicromat de potasiu (K2Cr2O7) concentrat, într-un mediu acid, în timp ce este fierbinte.
În mediul acid, există ioni H3O+ determinând descompunerea KMnO4 și eliberând 5 atomi de oxigen născut [O] pentru fiecare 2 KMnO4. Rețineți această descompunere mai jos:

Această reacție se numește „energică” deoarece rupe cele două legături ale dublei (în oxidarea ușoară doar legătura este ruptă pi), un alt factor este că această reducere a manganului într-un mediu acid este mult mai intensă decât într-un mediu bazic, așa cum se face în oxidare ușoară.
Oxigenul născut eliberat reacționează apoi cu o alchenă, dar produsul final depinde de ce tipuri de carbon care fac dubla legătură, adică indiferent dacă sunt primare, secundare sau terţiar. Vedeți ce se întâmplă în fiecare caz:
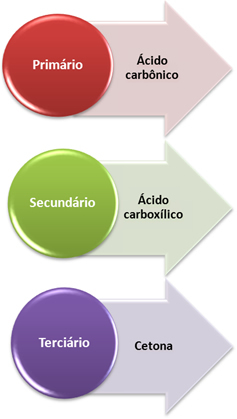
- Carbon primar: Dacă nesaturarea este între doi atomi de carbon primari, produsele formate vor fi două acizi carbonici (H2CO3). Dacă doar unul dintre carbonii din dubla legătură este primar, doar una dintre moleculele formate va fi acidul carbonic. Cu toate acestea, acest compus este instabil și nu a fost niciodată izolat, se descompune în apă și dioxid de carbon.
- Carbon secundar: Dacă nesaturarea este între doi atomi de carbon secundari, cei doi produși formați vor fi acizi carboxilici. Dacă doar unul dintre carboni este secundar, acesta va da naștere unei molecule de acid carboxilic, în timp ce celălalt va depinde de celălalt carbon.
- Carbon terțiar: Dă naștere la cetonă.
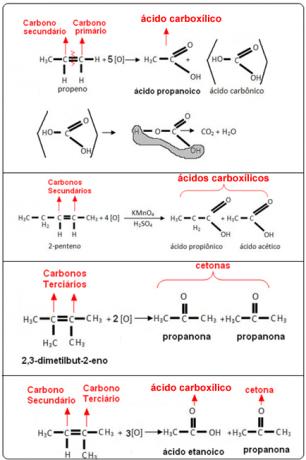
Vezi exemplele de mai jos:
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/oxidacao-energetica-alcenos.htm