Putem observa că ori de câte ori creștem concentrația unuia sau a tuturor reactanților care participă la o reacție chimică, există o creștere a vitezei sale de dezvoltare, adică a vitezei reacției.
Opusul este, de asemenea, adevărat. De exemplu, în prezent se recomandă să folosim gel de alcool în loc de alcool obișnuit, deoarece există un risc mai redus de ardere și astfel evitarea accidentelor. Alcoolul lichid obișnuit este de fapt un amestec de alcool și apă, cu alcool gel care conține o cantitate mai mică de alcool. Prin urmare, atunci când concentrația unuia dintre reactanții de ardere este redusă, în cazul alcoolului, reacția se desfășoară mai lent. Pe de altă parte, cu cât alcoolul este mai pur, cu atât reacția de ardere este mai rapidă.

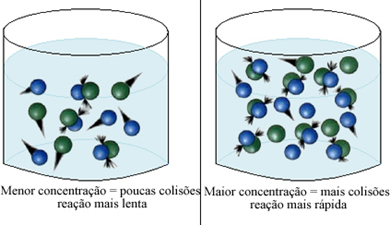
După cum se menționează în text Condiții pentru apariția reacțiilor chimice, una dintre condițiile pentru a avea loc o reacție este coliziune efectivă între particule. Prin urmare, creșterea concentrației de reactivi face posibilă o cantitate mai mare de particule sau molecule închise în același spațiu. Acest lucru mărește cantitatea de coliziuni între ele și, de asemenea, crește probabilitatea ca coliziuni efective să apară, care va duce la reacția care se produce. Rezultatul este că reacția are loc mai repede.
Pentru a vedea acest lucru, gândiți-vă la următorul exemplu: atunci când avem o ardă arzătoare și dorim ca această ardere să se proceseze mai repede, suflăm sau ventilăm brasa? De ce funcționează acest lucru?
Ei bine, unul dintre reactanții din această reacție de ardere este oxigenul din aer. Când scuturăm, curentul de aer elimină cenușa care se formează în timpul arderii și acest lucru facilitează contactul oxigenului cu brasa. În acest fel, mărim contactul dintre reactanți și accelerăm reacția de ardere.
Pe scurt, avem:

Când lucrați cu gaze, o modalitate de a crește concentrația de reactanți este scade presiunea. Când facem acest lucru, scădem volumul și, în consecință, există o creștere a concentrațiilor de reactivi.

De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/concentracao-dos-reagentes-velocidade-das-reacoes.htm
