O muscovius, numar atomic 115, situat în grupa 15 din Tabelul periodic, este unul dintre ultimele elemente incluse în acesta, în anul 2015, alături de elementele 113, 117 și 118. Numele său este o referire la regiunea din Moscova, capitala Rusiei.
Moscovium, însă, a fost produs inițial, în 2003, prin munca comună a oamenilor de știință ruși și americani. Chiar și așa, la aproape 20 de ani de la sinteza sa inițială, proprietățile sale de bază sunt încă în curs de determinare. Astfel, se speculează multe și se știe puțin despre proprietățile sale.
Aflați mai multe: Numele noilor elemente chimice - tributuri aduse orașelor, regiunilor și oamenilor de știință
Subiectele acestui articol
- 1 - Rezumat despre Moscovia
- 2 - Proprietăți Moscovium
- 3 - Caracteristicile moscoviului
- 4 - Obținerea Moscoviului
- 5 - Istoria Moscoviei
- 6 - Exerciții rezolvate pe moscovium
rezumat despre moscovius
Este un element chimic sintetic situat în grupul 15 al Tabelul periodic.
A fost sintetizată pentru prima dată, în 2003, printr-o muncă comună între oamenii de știință ruși și americani.
El alcătuiește grupul de elemente cel mai recent inclus în Tabelul periodic, în 2015.
Studiile lor sunt foarte recente, proprietățile de bază încă fiind determinate.
Producerea lui are loc prin fuziune nucleară, folosind 48Ca și atomi de 243A.m.
Nu te opri acum... Mai sunt dupa publicitate ;)
Proprietățile Moscovei
Simbol: Mc
Numar atomic: 115
Masă atomică: 288 au.m.a (neoficial de către Iupac)
Configuratie electronica: [Rn] 7s2 5f14 6d10 7p3
Cel mai stabil izotop: 288Mc (timp de înjumătățire 0,159 secunde)
seria chimica: grupa 15, elemente supergrele
Trăsături Moscovy
muscoviul este unul dintre ultimele elemente incluses în Tabelul Periodic. Includerea sa a avut loc pe 30 decembrie 2015, numele său oficial fiind lansat pe 8 iunie 2016.
Până la acea dată, elementul 115 era cunoscut în portugheză ca ununpentio, din latină, ununpentium, a cărui traducere este „unu, unu, cinci”. O altă nomenclatură adoptată a fost eka-bismut, care înseamnă „asemănător cu bismutul”, element al perioadei a șasea din grupa 15.
Moscova este o element sintetic, ceea ce înseamnă că poate fi produs doar într-un laborator. Acest lucru este foarte comun în rândul elementelor supergrele, deoarece nucleul lor, cu mulți protoni și neutroni, nu se poate stabiliza, ceea ce face imposibilă găsirea lor în natură.
pentru a fi o element instabil, acesta și celelalte elemente supergrele ajung să sufere dezintegrare radioactivă aproape instantaneu - emisii de particule elemente nucleare (cum ar fi particulele α sau β) - și transformarea ulterioară în alte elemente mai ușoare, care pot fi stabile sau Nu.
În ceea ce privește acesta, trebuie menționat că studiile sale sunt încă foarte recente, până la urmă ne aflăm în fața unui element produs cu puțin sub 20 de ani în urmă și al cărui statut oficial nu este nici măcar de 10 ani. În această privință, oamenii de știință au fost mai preocupați de determinarea caracteristicilor de bază, cum ar fi ale acestora masă atomică și comportamentul său chimic în unii compuși posibili.
De exemplu, masa atomică cea mai probabilă detectată până acum pentru Moscovy este de 288 de unități de masă atomică. Ca să nu mai vorbim că obținerea muscoviului este foarte complicată, cu a venit dintr-un singur atom pe zi.
În plus, atomul produs nu poate fi întotdeauna capturat pentru a măsura masa. În 2018, cercetătorii de la Berkeley Laboratories, California, Statele Unite, au putut măsura doar o masă pe săptămână. Prin urmare, studiile despre proprietățile compușilor săi sunt încă în domeniul chimiei teoretice, cu calcule și modele matematice pentru determinarea rezultatelor așteptate.
Obținerea Moscovei
Obținerea moscoviului se face prin Fuziune nucleară. ionii de 48Aici11+ (Z = 20) atomi loviti accelerați de 243Am (Z = 95), dispus sub formă de AmO2 pe o țintă circulară titan de 32 cm², producând moscoviul (Z = 115) și trei neutroni.
După impact, în aproximativ o microsecundă (10-6 al doilea), atomul de muscovy lovește detectorul, care se află la aproximativ patru metri distanță de locul coliziunii. Pe această cale, elementul trece și printr-un separator, astfel încât produsele de reacție mai ușoare sunt deviate. În detector, muscoviul este detectat prin modelul său de dezintegrare radioactivă.
Moscoviul, ca atom radioactiv, suferă dezintegrare alfa (o particulă radioactivă cu doi protoni și doi neutroni), producând astfel elementul 113 (nihonium, Nh) la elementul 105 (dubniu, Db). În cele din urmă, Db-ul se transformă în rutherfordiu (Rf), care se împarte rapid în două fragmente. Modelul de degradare al moscovium este prezentat mai jos.
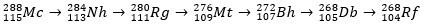
istoria Moscovei
muscoviusul a fost sintetizată pentru prima dată în 2003, în perioada 14 iulie – 10 august, prin munca comună a oamenilor de știință de la Institutul Comun pentru Cercetare Nucleară din Dubna, Rusia și Laboratorul Național Lawrence Livermore din Livermore, California.
Ioni de 48Ca astfel încât să se poată ciocni cu atomii de 243Am, producând inițial izotopul 291Mc. În timpul procesului, miezul a fost încălzit la un incredibil de 4 x 1011 K, și apoi răcit prin emisia foarte rapidă a trei neutroni și raze gamma.

Această acțiune a format izotopul 288Mc. apoi moscoviul a fost detectat și analizat pe baza modelului său de descompuneri radioactive (se descompune). Numele Moscova este un tribut adus regiunii Moscova, Rusia.
Citeste si:Seaborgium - elementul chimic sintetic numit după omul de știință Glenn Seaborg
Exerciții rezolvate pe muscovius
intrebarea 1
Moscoviul, un element recent descoperit, a fost plasat în grupa 15 din Tabelul Periodic. Pe baza celorlalte elemente din acest grup, hidrura așteptată pentru acest element ar fi:
A) McH
B) McH2
C) McH3
D) McH4
E) Mc2H3
Rezoluţie:
Alternativa C
Alte elemente din grupa 15, cum ar fi azot Este fosfor, prezentați formulele NH3 și pH3 atunci când este legat de hidrogen. Astfel, este de așteptat ca moscovia să prezinte formula McH3 de asemenea.
intrebarea 2
În 2003, moscovium (Z = 115) a fost sintetizat pentru prima dată, prin munca comună a oamenilor de știință ruși și americani. La acea vreme, izotopul 288Mc a fost detectat și producția sa a fost esențială pentru a plasa acest element în Tabelul Periodic. Numărul de neutroni din acest izotop este:
A) 115
B) 288
C) 403
D) 173
E) 170
Rezoluţie:
Alternativa D
Numarul neutroni se poate calcula astfel:
A = Z + n
Unde A este numărul de masă, Z este numărul atomic și n este numărul de neutroni. Înlocuind valorile, obținem:
288 = 115 + n
n = 288 – 115
n = 173
De Stefano Araujo Novais
Profesor de chimie
Ați auzit vreodată de elementul chimic antimoniu? Faceți clic aici și aflați despre caracteristicile, proprietățile, obținerea, aplicațiile și istoricul acestuia.
Ați auzit vreodată de elementul chimic arsen? Faceți clic aici, aflați despre principalele sale caracteristici și aflați ce măsuri de precauție trebuie luate cu el.
Ați auzit vreodată de elementul chimic bismut? Faceți clic aici și aflați despre caracteristicile, proprietățile, obținerea, aplicațiile și istoricul acestuia.
Descoperiți ce sunt elementele transuranice sintetizate în laborator, cum au fost descoperite și localizarea lor în Tabelul Periodic.
Aflați mai multe despre fosfor, precum și despre caracteristicile, proprietățile, aplicațiile, precauțiile, importanța și istoricul acestuia, precum și despre ciclul fosforului.
Faceți clic și cunoașteți istoricul, caracteristicile, sursele, modalitățile de obținere și utilizări ale Azotului.
Aflați în acest text care sunt denumirile noilor elemente chimice și de ce fiecare a primit astfel de denumiri.
Descoperiți principalele caracteristici ale celor patru noi elemente ale Tabelului Periodic.
