Tabelul periodic este un mod de organizare a tuturor elementelor chimice în funcție de proprietățile lor și de afișare a unor informații despre ele.
În viața de zi cu zi, organizarea este foarte importantă pentru a ne ușura viața. De exemplu, imaginați-vă dulapul dezordonat, cu șosete amestecate cu cămăși și pantaloni. Ar fi foarte dificil și ar dura mai mult timp să găsești un șoset specific pe care ți-ai dorit să-l porți, n-ai spune?! Dar dacă îți organizezi garderoba și îți pui toate șosetele într-un singur sertar, ai un sertar. pentru tricouri, altul pentru pantaloni scurți și așa mai departe, va fi mult mai ușor să găsiți ce nevoie. Și cu cât aveți mai multe haine, cu atât este nevoie de mai multă organizare.
La fel, oamenii de știință au descoperit de-a lungul timpului multe elemente chimice. Pentru a vă face o idee, în 1850 erau cunoscute în jur de 60 de elemente, dar astăzi știm de existența 118. Astfel, a apărut necesitatea organizării acestor elemente chimice într-un mod care să faciliteze înțelegerea proprietăților lor. Acesta este rolul Tabelului periodic al elementelor chimice.
Tabelul periodic pe care îl folosim astăzi este aranjat în linii orizontale în ordine crescătoare a numărului atomic.
Ar trebui să consultați Tabelul periodic ca și cum ați citi un text normal, adică întotdeauna începe cu primul rând și de la partea stângă la dreapta și apoi continuă până la următorul linii.Elementele chimice au fost plasate pe tabelul periodic în pătrate separate, unde simbolul elementului este în jumătate și valoarea numărului atomic este de obicei scrisă în partea de sus, așa cum se arată în exemplul de hidrogen de mai jos:

Simbolul hidrogenului și numărul său atomic, așa cum se arată în tabelul periodic
Numărul atomic este cantitatea de protoni sau sarcini pozitive pe care le au atomii elementului. Această valoare este egală cu numărul de electroni când atomul se află în starea sa de bază.Hidrogenul este un element care are doar 1 proton, adică numărul său atomic este 1. Prin urmare, hidrogenul este primul element plasat în tabel. Următorul element care se află pe aceeași linie cu hidrogenul este heliul, deoarece are un număr atomic egal cu 2.
Trecând la rândul de jos, primul este litiu cu un număr atomic egal cu 3, alături este beriliu cu numărul atomic 4 și așa mai departe.Uită-te la primele linii ale Tabelului Periodic prezentate mai jos și vezi că ordinea numărului atomic crește exact.
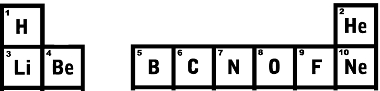
Primele două rânduri ale Tabelului periodic
Există șapte linii în tabelul periodic și aceste linii sunt numite perioade. Uite:

Perioade de tabel periodic
Există 18 coloane care sunt numite familii sau grupuri. Un aspect important este acela elementele care aparțin aceleiași familii sunt cele care au proprietăți fizice și chimice similare.

Familii sau grupuri de tabele periodice
Să vedem dacă înțelegi? Spune-mi care este elementul chimic care aparține perioadei a 4-a și a celei de-a 16-a familii?
Dacă ai spus Se (seleniu), ai dreptate! Acum spune-mi care este numărul său atomic. Așa este, sunt 34.
În fiecare pătrat mic pe care îl vede elementul există și alte informații importante, cum ar fi masă atomică si electroni care se află în fiecare strat electronic de atomi. De exemplu, vedeți în imaginea următoare că neonul are Ne ca simbol, numărul său atomic este egal cu 10, masa sa atomică este egală cu 20,1797 u și electronii sunt distribuiți astfel în straturile lor: 2 - 8, adică în stratul cel mai apropiat de nucleu există doi electroni și în cel mai îndepărtat sunt opt electroni.

Simbol de neon pe Tabelul periodic și atomul acestuia
Acum observați două aspecte interesante: (1) neonul are doar două orbite sau straturi unde sunt electronii dvs., de aceea ocupă a 2-a perioadă (A doua linie);și (2) are opt electroni pe ultimul strat, de aceea el este familia 18.
Aceasta ne arată următoarele:
* Elementele care se află în aceeași perioadă a tabelului periodic au aceeași cantitate de straturi electronice și pot avea maximum șapte;
* Elementele chimice care se află în aceeași familie pe tabelul periodic au același număr de electroni în ultima coajă de electroni:
* Familia 1: am tot 1 electron în ultimul strat electronic;
* Familia 2: am tot 2 electroni în ultimul strat electronic;
* Familia 13: am tot 3 electroni în ultimul strat electronic;
* Familia 14: am tot 4 electroni în ultimul strat electronic;
* Familia 15: am tot 5 electroni în ultimul strat electronic;
* Familia 16: am tot 6 electroni în ultimul strat electronic;
* Familia 17: am tot 7 electroni în ultimul strat electronic;
* Familia 18: am tot 8 electroni în ultimul strat electronic.
Unelor grupuri sau familii din tabelul periodic li se dau nume specifice, a se vedea unele:
Familia 1: Metale alcaline;
Familia 2: Metale alcalino-pământoase;
Familia 16: Calcogeni;
Familia 17: Halogeni;
Familia 18: Gaze nobile.

Organizarea familiilor de tabele periodice
Din nou, să vă testăm cunoștințele. Răspundeți la următoarele întrebări doar consultând Tabelul periodic:
1- Care este numele familiei de clor?
2- Care este numărul său atomic și masa sa atomică?
3- Câte straturi electronice are un atom de clor?
4- Câți electroni are un atom de clor în ultimul său înveliș de electroni?
Răspunsuri:
1- Halogeni (familia 17).
2- Numărul atomic de clor este 17, iar masa sa atomică este egală cu 35,45 u.
3- Un atom de clor are trei straturi electronice, deoarece aparține celei de-a treia perioade a tabelului.
4- Un atom de clor are șapte electroni în învelișul de valență, deoarece aparține familiei 17.
Există încă alte informații importante pe care ni le transmite Tabelul periodic și despre care vom vorbi mai bine în textele ulterioare. Dar cele discutate aici sunt principalele pentru a începe să înțelegeți modul în care elementele sunt organizate în ea. Amintiți-vă că o masă nu este făcută pentru decorare, dar trebuie să o cunoașteți bine pentru a vă putea referi la ea atunci când este necesar.
De Jennifer Fogaça
Absolvent în chimie
Profitați de ocazie pentru a vedea cursurile noastre video legate de subiect:


