Wśród złożoności badań atomowych jest określenie rozmiaru atomu lub, lepiej, promień atomowy. Ta okresowa właściwość opisuje odległość od jądra do najbardziej zewnętrznego elektronu jego poziomów elektronowych. Aby to określić, wykonuje się średnią arytmetyczną odległości między jądrami dwóch atomów, które tworzą na przykład prostą substancję.
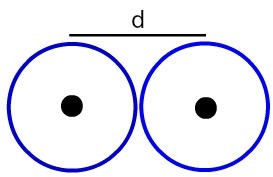
Reprezentacja odległości między dwoma jądrami atomowymi
Ustalmy promień atomowy (RA) atomów przedstawionych na obrazku. Aby to zrobić, po prostu podziel odległość między rdzeniami przez 2:
RA = re
2
O badanie promieni atomowych jest ważne, ponieważ sprzyja zrozumieniu niektórych zdarzeń fizycznych (gęstość, punkt topnienia, temperatury wrzenia i energii jonizacji) oraz substancji chemicznych (wiązań chemicznych), które występują z atomy.
Analizując układ okresowy możemy ocenić, czy atom jest większy czy mniejszy w stosunku do drugiego, a tym samym określić, czy ma większą czy mniejszą łatwość usunięcia jednego lub więcej elektronów z ich orbitali. TEN ocena i wyznaczenie promienia atomu w układzie okresowym
odbywa się według dwóch podstawowych kryteriów:a) Liczba poziomów energetycznych (rodziny lub grupy/pionowe kolumny)
Wiemy, że atomy mogą mieć do siedmiu poziomów energetycznych (K, L, M, N, O, P, Q) i każdy pierwiastek chemiczny znajduje się w rodzinach lub grupach (pionowe kolumny) oraz w okresach (kolumny poziomy). Kropki wskazują liczbę poziomów atomu pierwiastka, a rodzina wskazuje najbardziej energetyczny podpoziom atomu. W grupie lub rodzinie pierwiastki chemiczne różnią się ilością poziomów energii. Zobacz tabelę poniżej:

Im większa liczba poziomów energetycznych atomu, tym większy jego promień atomowy. Analizując powyższą tabelę, widać, że frans ma największy atom, ponieważ ma siedem poziomów. Z drugiej strony atom potasu ma mniejszy promień, ponieważ ma cztery poziomy energetyczne. Poniżej przedstawiono porównawcze przedstawienie atomu francu i atomu potasu:
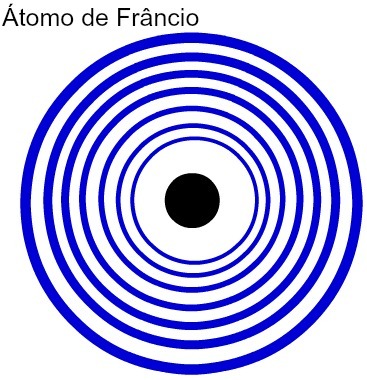
Reprezentacja siedmiu poziomów energetycznych atomu franka
Teraz nie przestawaj... Po reklamie jest więcej ;)

Reprezentacja czterech poziomów energetycznych atomu potasu
Poniższy diagram przedstawia, w jaki sposób wzrost promienia atomowego występuje w tej samej rodzinie lub grupie (pionowe kolumny) układu okresowego. Im większa liczba poziomów, tym większy promień, czyli w układzie okresowym pierwiastków promień atomowy rośnie od góry do dołu:
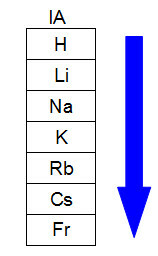
Reprezentacja wzrostu promienia atomu w rodzinie układu okresowego pierwiastków
b) Liczba atomowa (Z lub liczba protonów) w tym samym okresie (kolumna pozioma)
Gdy pierwiastki chemiczne należą do tego samego okresu, ich atomy mają tę samą ilość poziomów energii, ale ilość protonów w ich jądrach jest inna. Poniżej znajduje się sekwencja elementów należących do czwartego okresu układu okresowego:
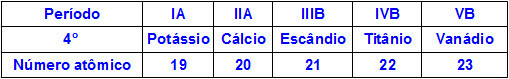
Wszystkie atomy pierwiastków przedstawionych w powyższej tabeli mają cztery poziomy energetyczne, ale każdy z nich ma inną ilość protonów w swoich jądrach. Ponieważ protony wewnątrz jądra wywierają przyciągającą siłę na elektrony obecne na poziomach energetycznych, im większa ilość protonów w jądrze, tym większe ich przyciąganie do elektronów. Rezultatem jest przybliżenie poziomów w kierunku jądra, zmniejszając rozmiar atomu.
↑Z = ↓Promień atomowy
↓Z = ↑Promień atomowy
Możemy zatem stwierdzić, że promień atomowy pierwiastka potasu jest większy niż promień wanadu ze względu na mniejszą liczbę protonów.
Poniższy diagram przedstawia wzrost promienia atomu w tym samym okresie (linia pozioma). Im mniejsza liczba atomowa, tym większy promień, czyli promień atomowy w tabeli rośnie od prawej do lewej
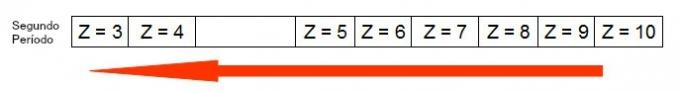
Reprezentacja wzrostu promienia atomu w okresie układu okresowego
Przeze mnie Diogo Lopes Dia
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
DNI, Diogo Lopes. "Promień atomowy"; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/raio-atomico.htm. Dostęp 28 czerwca 2021 r.