TEN Elektrochemia to dział chemii fizycznej, który bada reakcje, w których zachodzi transfer elektronów (reakcje oksy-redukcji) i jego konwersja na energię elektryczną, a także proces odwrotny, czyli konwersja energii elektrycznej na energię chemia.
Pierwszy proces ma miejsce w Baterie. Akumulatory to urządzenia utworzone przez dwie elektrody (biegun dodatni, który jest katodą i biegun ujemny, który jest anodą) oraz elektrolit (roztwór przewodzący). Elektrony są przenoszone przez zewnętrzny przewodnik z anody do katody, tworząc prąd elektryczny, który służy do włączania niektórych urządzeń. Baterie składają się z kilku ogniw połączonych szeregowo lub równolegle.
Jest to proces spontaniczny i energia jest dostarczana aż do wyczerpania reakcji chemicznej (jak w przypadku ogniw i baterii pierwotnych, takich jak suche ogniwo Leclanché i bateria alkaliczny) lub, w przypadku reakcji odwracalnych, można przyłożyć różnicę potencjałów i odwrócić reakcję, ponownie tworząc reagenty i doładowując akumulator, który jest gotowy do ponownego użycia (dotyczy to baterii i baterii wtórnych, takich jak ołowiowe, stosowane w samochodach oraz litowo-jonowe, stosowane w urządzeniach telefony komórkowe).

Ogniwa pierwotne i baterie na pierwszym planie, a na drugim ładowanie baterii wtórnych (ołowiowych i litowo-jonowych)
Z drugiej strony proces odwrotny nie jest spontaniczny i nazywa się elektroliza. Elektroliza to przepływ prądu elektrycznego pochodzącego z generatora, takiego jak ogniwo lub bateria, przez ciecz jonową. Jeśli ciecz jest jakąś stopioną substancją, mamy elektroliza magmowa, ale jeśli jest to roztwór wodny, to mamy elektroliza wodna.
Przepuszczając prąd elektryczny przez ośrodek ciekły, generator „wyciąga” elektrony z bieguna dodatniego (anoda - jest to przeciwieństwo baterii) ogniwa elektrolitycznego i przenosi je na biegun ujemny (katodę), czyli katoda ulega redukcji, a anoda ulega utlenianie. W ten sposób energia elektryczna dostarczana przez generator jest przekształcana w reakcje redoks (energia chemiczna). Poniżej znajduje się schemat elektrolizy wody:
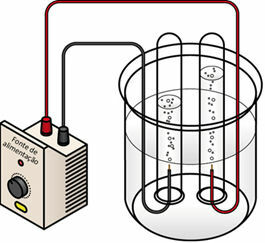
Schemat elektrolizy wody
Elektroliza jest szeroko stosowana przemysłowo w produkcji ważnych substancji, takich jak aluminium, chlor gazowy, metaliczny sód oraz do oczyszczania lub ochrony różnych metali, jak w procesach galwanizacji lub galwanizacji, które polegają na powlekaniu jakiegoś przedmiotu metalem, takim jak srebrzenie, miedziowanie, niklowanie, złocenie i chromowanie; gdy stal jest pokryta cynkiem, nazywa się to cynkowaniem.
W sekcji Elektrochemia na naszej stronie znajdziesz więcej szczegółów dotyczących wszystkich aspektów związanych z ogniwami i bateriami, a także elektrolizą.
Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eletroquimica.htm

