O równoważenie równania utleniania-redukcji opiera się na równości liczby oddanych elektronów z liczbą elektronów otrzymanych. Prosta metoda wykonania tego równoważenia jest podana w następujących krokach:
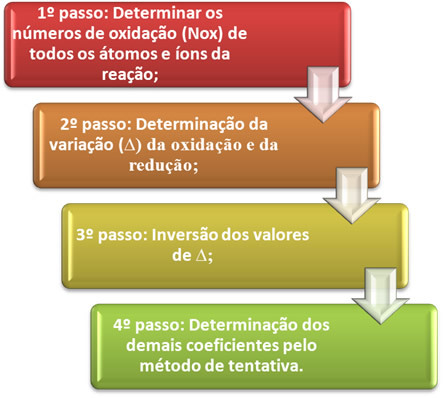
Zobaczmy w praktyce, jak zastosować te kroki na poniższym przykładzie:
Reakcja między wodnym roztworem nadmanganianu potasu i kwasu solnego:
kmnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
*Pierwszy krok:Określ stopnie utlenienia:
Ten krok jest ważny, ponieważ zwykle nie jesteśmy w stanie szybko zwizualizować, które gatunki ulegają utlenianiu i redukcji.
+1 +7 -2 +1 -1 +1 -1 +2 -1 0 +1 -2
kmnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
*Drugi krok:Oznaczanie zmienności utleniania i redukcji:

Zauważ, że mangan (Mn) jest redukowany, a chlor (Cl) jest utleniany.
MnCl2 = ∆Nox = 5
Cl2 = ∆Nox = 2
W przypadku chloru możemy zauważyć, że HCl dał początek 3 związkom (KCl, MnCl2, i Cl2), ale to, co nas interesuje, to Cl2, ponieważ to twój Nox uległ zmianie. Każdy chlor, który tworzy Cl2 stracić 1 elektron; ponieważ do utworzenia każdego Cl takes potrzeba 2 chlorów2, wtedy dwa elektrony są tracone.
Trzeci krok:Odwrócenie wartości ∆:
W tym kroku wartości ∆ są wymieniane pomiędzy wymienionymi gatunkami, stając się ich współczynnikami:
MnCl2 = ∆Nox = 5 → 5 będzie współczynnikiem Cl2
Cl2 = ∆Nox = 2→ 2 będzie współczynnikiem MnCl2
kmnO4 + HCl → KCl + 2 MnCl2 + 5 Cl2 + H2O
W tym momencie można już poznać dwa współczynniki równania.
Obserwacja: normalnie w większości reakcji to odwrócenie wartości odbywa się na 1. członku. Ale z reguły powinno się to odbywać w elemencie, który ma największą liczbę atomów, które ulegają redoksowi. Jeśli to kryterium nie może być spełnione, odwracamy wartości dla członka z największą liczbą związków chemicznych. Tak właśnie zrobiono tutaj, ponieważ drugi członek ma więcej substancji.
4 krok: Równoważenie prób:
kmnO4 + HCl → KCl + 2 MnCl2 + 5 Cl2 + H2O
- Ponieważ w drugim członie znajdują się dwa atomy manganu, jak pokazuje współczynnik, w pierwszym musi być też. Więc mamy:
2 kmnO4 + HCl → KCl + 2 MnCl2 + 5 kl2 + H2O
- Tak więc ilość potasu (K) w pierwszym elemencie wynosiła 2, co będzie tym samym współczynnikiem dla tego atomu w drugim elemencie:
2 kmnO4 + HCl → 2 KCl + 2 MnCl2 + 5 Cl2 + H2O
- Ilość chloru (Cl) w drugim członku wynosi łącznie 16, więc współczynnik HCl pierwszego członka wyniesie:
2 kmnO4 + 16 HCl → 2KCl + 2 MnCl2 + 5 Cl2 + H2O
- Liczba wodorów w pierwszym członie wynosi 16, stąd współczynnik wody (H2O) drugiego członu będzie równe 8, ponieważ pomnożenie wskaźnika wodoru (2) przez 8 wynosi 16:
2 kmnO4 + 16 HCl → 2 KCl + 2 MnCl2 + 5 Cl2 + 8 H2O
- Aby sprawdzić, czy równanie jest prawidłowo zbalansowane, możemy zobaczyć dwa kryteria:
1.) Sprawdź, czy ilość każdego atomu w dwóch członach jest równa:
2 kmnO4 + 16 HCl →2 KCl + 2 MnCl2 + 5 kl2 + 8 godz2O
K = 2K = 2
Mn = 2 Mn = 2
Cl = 16 Cl = 16
H = 16 H = 16
O = 8 O = 8
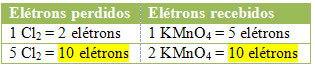
2.) Sprawdź, czy całkowita liczba utraconych elektronów jest równa całkowitej liczbie otrzymanych elektronów:
Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/balanceamento-por-oxirreducao.htm

