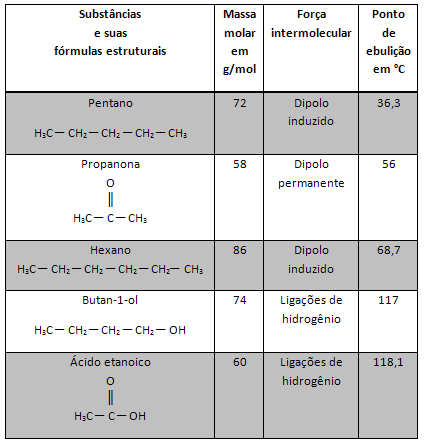
Kwasy i zasady to dwie funkcje chemiczne, które są uważane za przeciwieństwa., ponieważ ich właściwości są zwykle odwrotne. Na przykład, jeśli weźmiemy pod uwagę, że pokarmy obecne w naszym codziennym życiu są kwaśne, zobaczymy, że ich smak jest ogólnie kwaśny, jak ma to miejsce w przypadku cytryny. Jednak podstawowe produkty spożywcze mają cierpki smak (który „wiąże” usta), jak zielony banan.
Ale identyfikowanie substancji jako kwaśnej lub zasadowej tylko na podstawie smaku, a także bycie metodą, która ma wiele szans na niepowodzenie, jest również bardzo niebezpieczny, ponieważ istnieje wiele kwasów i zasad, które są silne, toksyczne i mogą nawet zabić, na przykład kwas. siarkowy (H2TYLKO4), stosowany w akumulatorach samochodowych, oraz wodorotlenek sodu (NaOH), znany pod nazwą handlową soda kaustyczna.
Zatem właściwości organoleptyczne (właściwości dotyczące naszych zmysłów, takie jak smak i zapach) nie są tymi, które wykorzystuje się do identyfikacji kwasów i zasad. Zwróć uwagę poniżej na inne właściwości tych funkcji organicznych, które służą do ich porównania i rozróżnienia:
- Rozpuszczalność w wodzie:
ty kwasy zwykle ma się dobrze rozpuszczalny w wodzie, podczas gdy większość podstawy é nierozpuszczalny. Zasady metali alkalicznych są rozpuszczalne, zasady metali ziem alkalicznych są słabo rozpuszczalne, a zasady innych metali są nierozpuszczalne (wyjątkiem jest wodorotlenek amonu, NH4OH, który występuje tylko w roztworze wodnym, bąblując gazowy amoniak w wodzie i dlatego jest w niej rozpuszczalny).
Mówiąc „nierozpuszczalne”, mamy na myśli, że substancje te są praktycznie nierozpuszczalne, ponieważ żadna substancja nie jest całkowicie nierozpuszczalna w wodzie.
- Struktura:
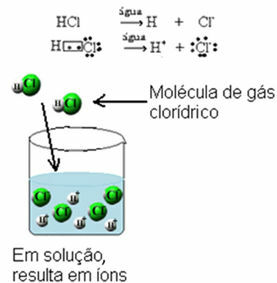
Wszystkie kwasy są molekularne, czyli utworzone przez wiązania kowalencyjne, w których współdzielone są elektrony. Przykładem jest gaz chlorowodorowy, który powstaje przez dzielenie pary elektronów między wodór i chlor:

już zasady mogą być jonowe lub molekularne. Te z metalami alkalicznymi i ziem alkalicznych są jonowe, a inne są molekularne.
Przykłady:
NaOH: zasada jonowa utworzona przez jony Na+ i och-;
NH4OH: podstawa cząsteczkowa amoniaku w wodzie.
Teraz nie przestawaj... Po reklamie jest więcej ;)
- Przewodność elektryczna:
Wszystko kwasy przewodzą prąd elektryczny tylko wtedy, gdy są rozpuszczone w wodzie, ponieważ w środowisku wodnym ulegają jonizacji, czyli uwalniają jony.
Przykład:
Wszystko podstawy również przewodzą prąd elektryczny w roztworze.jonowe bowiem ulegają dysocjacji (uwalniają już istniejące w formule jony), a molekularne ulegają jonizacji, reagując z wodą i uwalniając jony. W Bazy z metali alkalicznych również przewodzą prąd elektryczny, gdy są w stanie ciekłym (stopionym).
- Działania na wskaźnikach:
ty wskaźniki kwasowo-zasadowe to naturalne lub syntetyczne substancje, które w kontakcie z kwasem lub zasadą zmieniają kolor. Jeśli kwas spowoduje zmianę koloru wskaźnika, zasada przywróci wskaźnik do jego pierwotnego koloru i na odwrót.
Na przykład fenoloftaleina jest szeroko stosowanym wskaźnikiem kwasowo-zasadowym, a w podstawowym podłożu staje się bardzo intensywnie różowa; już w środowisku kwaśnym staje się bezbarwny. Papierek lakmusowy jest również dobrym wskaźnikiem, ponieważ w kwasie zmienia kolor na czerwony; a na jednej podstawie zmienia kolor na niebieski.
Służy to również do wskazania różnicy pH, która istnieje między kwasami i zasadami.
- PH:
Medium uważane za obojętne ma pH równe 7, podobnie jak woda destylowana.
Kwasy mają pH poniżej 7, Podczas zasady mają pH większe niż 7.
Przykłady roztworów o pH zbliżonym do wskazanego na skali:
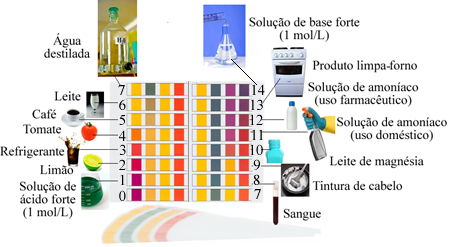
- Wzajemne działanie:
W kontakcie kwasy i zasady reagują ze sobą, neutralizując się nawzajem, czyli neutralizując pH medium. Dzieje się tak, ponieważ kation H+ z kwasu reaguje z anionem OH- z podstawy, tworząc wodę. Ten typ reakcji nazywa się a Reakcja neutralizacji a także produkuje sól.
Jennifer Fogaça
Absolwent chemii