W badaniu termologii nazywamy to przemiany adiabatyczne te przemiany gazowe, w których nie ma wymiany ciepła ze środowiskiem zewnętrznym. Dlatego w transformacji adiabatycznej ciepło wynosi zero.
Q = 0
Jeśli zastosujemy pierwszą zasadę termodynamiki, mamy:
Q = ∆U+τ
∆U = - τ
Ale co to znaczy, że nie ma wymiany ciepła między środowiskiem zewnętrznym? Oznacza to, że jeśli dojdzie do rozprężania gazowego, a gaz wykonuje zadanie 300 J, to nie jeśli zachodzi wymiana ciepła z medium, zmienność energii wewnętrznej gazu będzie ujemna, a zatem będziemy mieli:
∆U = - 300 J
Teraz, jeśli nastąpił spadek energii wewnętrznej gazu, możemy powiedzieć, że nastąpił również spadek temperatury gazu. Z ogólnego prawa gazów

możemy powiedzieć, że jeśli objętość wzrośnie, a temperatura gazu spadnie, z konieczności spadnie również ciśnienie gazu. Ogólnie można powiedzieć, że to samo dzieje się ze sprężaniem, ponieważ jeśli nastąpi sprężanie, wzrośnie energia wewnętrzna gazu, a więc ciśnienie również wzrośnie.
Mapa myśli: Transformacja adiabatyczna
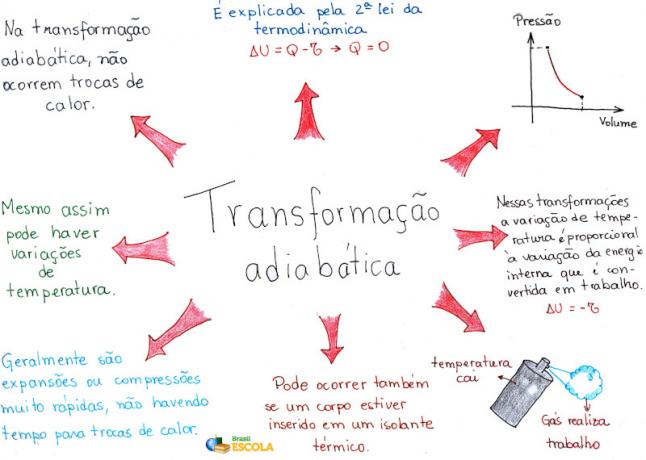
* Aby pobrać mapę myśli w formacie PDF, Kliknij tutaj!
W skrócie możemy powiedzieć, że:
- przy rozszerzaniu adiabatycznym, spadku temperatury i ciśnienia;
- w kompresji adiabatycznej wzrasta zarówno temperatura, jak i ciśnienie.
Poniższy wykres daje nam przegląd transformacji adiabatycznej:
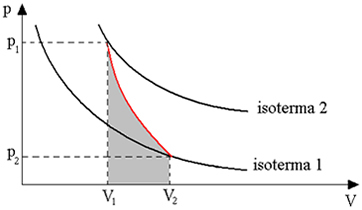
Przemiany adiabatyczne uzyskuje się za pomocą pojemników izolowanych termicznie, a także poprzez ściskanie lub bardzo szybkie rozprężanie.
Możemy zatem stwierdzić, że gdy gaz wymienia ciepło ze środowiskiem zewnętrznym, rozchodzenie się ciepła przez masę gazową i osiągnięcie równowagi zajmuje trochę czasu. Dlatego też, gdy przeprowadza się zarówno rozprężanie, jak i szybkie sprężanie, praktycznie nie ma wymiany ciepła z medium zewnętrznym.
* Mapa myśli autorstwa Rafaela Helerbrocka
Autor: Domitiano Marques
Ukończył fizykę
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/fisica/estudo-transformacao-adiabatica.htm
