O benzen jest związkiem organicznym sklasyfikowanym jako aromatyczny węglowodór. Jest szeroko stosowany jako surowiec w przemyśle, w procesach laboratoryjnych, w firmach hutniczych oraz w przemyśle petrochemicznym do rafinacji ropy naftowej.
Przeczytaj też: Metan — najmniejszy i najprostszy z węglowodorów
Formuła
Benzen jest związkiem o wzorze cząsteczkowym DO6H6i kto ma? wyjątkowo stabilna konstrukcjal. Wzór strukturalny benzenu przedstawia się następująco:
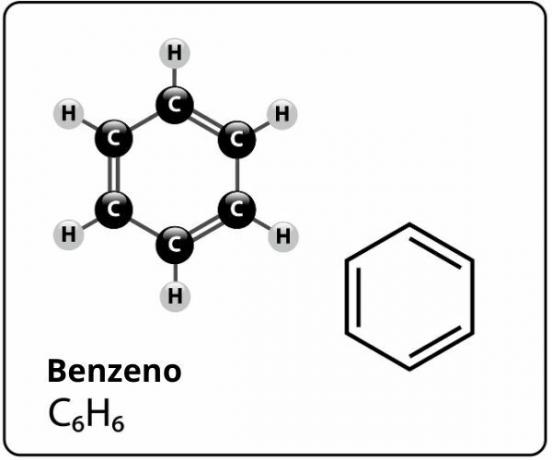
Kto zaproponował tę strukturę dla benzenu z sześć atomów węgla związanych ze sobą naprzemiennymi wiązaniami podwójnymi, tworząc sześciokąt i dołączając do każdego z nich atom wodór, to był niemiecki chemik Friedrich August Kekule, w 1866 r.
Benzen podlega zjawisku zwanemu rezonans, w którym elektrony w wiązaniach między węglami różnią się położeniem. Z tego powodu benzen można przedstawić w następujący sposób:
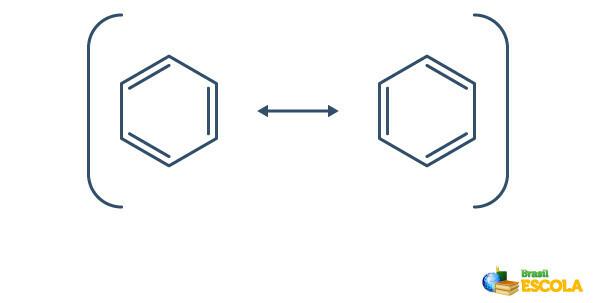
Rzeczywista struktura benzenu jest pośrednikiem między przedstawionymi powyżej strukturami rezonansowymi. Nie oznacza to, że benzen pojawia się czasami w jednej postaci, czasami w innej, ani że obie formy istnieją jednocześnie. Reprezentujemy benzen w następujący sposób:
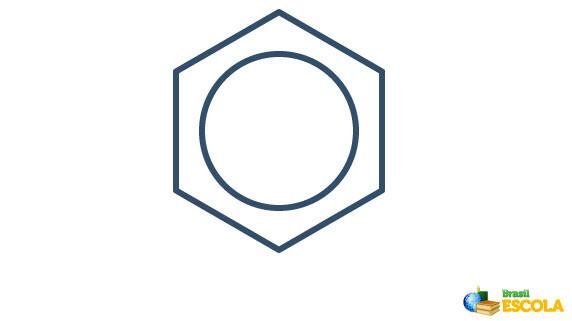
Okrąg wewnątrz sześciokąta reprezentuje rezonans między elektronami w wiązaniach.
Teraz nie przestawaj... Po reklamie jest więcej ;)
funkcje
- Benzen to ciecz bezbarwny, łatwopalny to jest powszechne przyjemny aromat Charakterystyka.
- Wzór cząsteczkowy: C6H6.
- Masa molowa: 78,11 g/mol.
- Gęstość: 0,876 g/cm³.
- Temperatura topnienia: 5,5 °C.
- Temperatura wrzenia: 80,1 ºC – niska temperatura wrzenia tłumaczy dużą lotność (łatwość parowania).
Benzen jest toksyczna substancja a jego opary mogą powodować zawroty głowy, bóle głowy i omdlenia.
Przeczytaj też:Tlenek węgla — wyjątkowo toksyczny, bezbarwny i bezwonny gaz
Zastosowania i toksyczność benzenu
benzen jest używany głównie jako surowiec w branżach do produkcji innych substancji, takich jak tworzywa sztuczne i polimery na bazie styrenu, żywic, klejów, nylonu, gumy, smarów, pestycydów itp.
Benzen został zastąpiony, głównie w laboratoriach, toluenem, który ma polarność i rozpuszczalność podobny do benzenu, ale jest mniej toksyczny i ma wyższą temperaturę wrzenia.
Benzen należy do grupy substancje chemiczne uważane za rakotwórcze, powodując uszkodzenie szpiku kostnego i białaczkę przy długotrwałym narażeniu na wysokie stężenia. W krótkim okresie benzen może powodować zawroty głowy, senność, szybkie bicie serca, drgawki i omdlenia.
Ponieważ jest to ciecz lotna, benzen łatwo uwalnia gazy i dlatego zanieczyszczenie benzenem następuje głównie przez drogi oddechowe.
Gdzie znajduje się benzen?
Większość benzenu uwalniana do środowiska wynika z ludzkiego działania, głównie w działalności przemysłowej, ale może być również uwalniany jako produkt uboczny pożarów i działalności wulkanicznej.
benzen jest jedna z substancji składowych Ropa naftowa i jest obecny w benzynie, uwalniany do atmosfery przez spalanie paliw samochodowych. Ponadto znajduje się również w napojach bezalkoholowych i papierosach.

Biegunowość
Benzen jest niepolarna cząsteczka, tak jak wszyscy inni Węglowodory i dlatego prezentuje bardzo niska rozpuszczalność w wodzie (0,8 g/lw 15°C). W niektórych procedurach laboratoryjnych benzen jest używany jako rozpuszczalnik organiczny dla substancji niepolarnych.
Nomenklatura
Istnieje zasada stosowana tylko do nomenklatury związków aromatycznych, czyli takich, które w swojej strukturze mają benzen. Zasada ta dzieli się na dwa przypadki, które zależą od ilości rodników przyłączonych do pierścienia benzenowego.
PRZYPADEK I: gdy do pierścienia benzenowego jest przyłączony tylko jeden rodnik, nazwę podaje się zgodnie z następującą zasadą:
NAZWA RADYKALNA + BENZEN
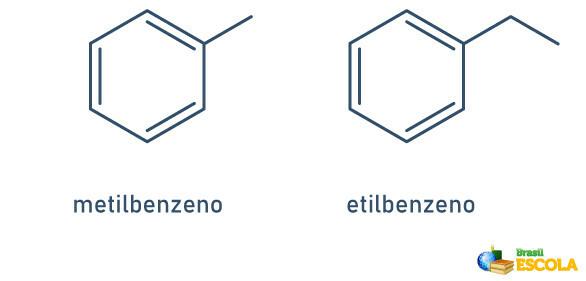
Zauważ, że nie jest konieczne wskazywanie pozycji łodygi.
PRZYPADEK 2: gdy do benzenu przyłączony jest więcej niż jeden rodnik, nazwa jest zgodna z następującą zasadą:
POZYCJA RADYKALNA + NAZWA RADYKALNA + BENZEN
Zobacz przykład:

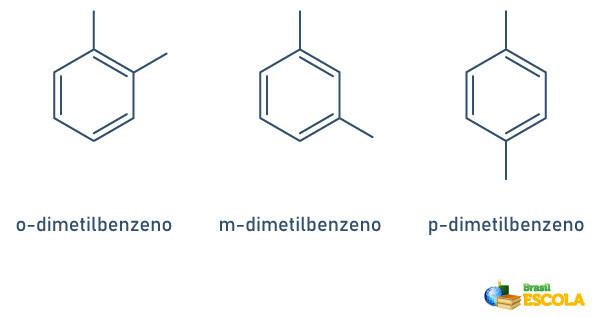
Gdy pierścień benzenowy ma tylko dwa przyłączone rodniki, istnieje specyficzna nomenklatura, której można użyć:
- 1,2 lub orto(o);
- 1.3 lub bramka (m);
- 1.4 lub do (p).
Zobacz przykłady:
Przeczytaj też: Azotan amonu — wysoce reaktywny związek stosowany w produkcji materiałów wybuchowych
Ciekawostki
- Benzen jest substancją niezwykle rakotwórczą, klasyfikowaną przez Międzynarodową Agencję badań nad rakiem, w grupie 1, razem z tytoniem, dymem z oleju napędowego i mięsem obrobiony.
- Istnieje kilka organów regulacyjnych, które ograniczają narażenie i emisję benzenu w różnych krajach. W Brazylii za tę rolę odpowiada Anvisa.
- Przed poznaniem zagrożeń, benzen był używany w kosmetykach, takich jak woda po goleniu, ze względu na przyjemny zapach.
Autor: Victor Ricardo Ferreira
Nauczyciel chemii
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
FERREIRA, Victor Ricardo. "Benzen"; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/benzeno.htm. Dostęp 27 czerwca 2021 r.
Chemia

Związki aromatyczne, areny, polarność, nierozpuszczalne, rozpuszczalne, niepolarne rozpuszczalniki, eter, czterochlorek węgla, węglowodory, insektycydy, barwniki, rozpuszczalniki, materiały wybuchowe, substancje rakotwórcze, toluen, metylobenzen, leki, klej szewc.



