Reakcje halogenowania to rodzaj reakcji podstawienia organicznego, czyli takie, w których a atom lub grupy atomów są zastąpione atomami lub grupami atomów innej cząsteczki organiczny.
Generalnie tego typu reakcja zachodzi z alkanami i węglowodorami aromatycznymi (benzen i jego pochodne).
Halogenacja jest tak nazywana, ponieważ zachodzi z prostymi substancjami halogenów: F2, Cl2, br2 Hej2. Jednak najczęstsze z nich to chlorowanie (Cl2) i bromowania (Br2), ponieważ fluor jest bardzo reaktywny, a jego reakcje są wybuchowe i trudne do kontrolowania, niszcząc nawet materię organiczną:
CH4(g) + 2 F2(g) → C(y) + 4HF(sol)
Reakcje z jodem są niezwykle powolne.
Poniżej znajdują się główne rodzaje halogenowania i kilka przykładów:
1. Halogenowanie alkanami: Ponieważ alkany są słabo reaktywne, ich reakcje halogenowania zachodzą tylko w obecności światła słonecznego (λ), światła ultrafioletowego lub silnego ogrzewania. Ten typ reakcji ma na celu uzyskanie halogenku alkilu.
Przykład: monochlorowanie metanu:
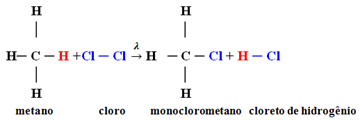
W tym przypadku pochodziło z atomu wodoru metanu (CH4) zastąpić atomem chloru, dając monochlorometan. Gdyby było za dużo chloru, reakcja ta mogła być kontynuowana, zastępując wszystkie wodory w metanie.
1.1. Halogenacja w alkanach zawierających więcej niż 3 węgle: Jeśli alkan, który ma być poddany reakcji, ma co najmniej 3 atomy węgla, otrzymujemy mieszaninę różnych podstawionych związków. Zobacz poniższy przykład monochlorowania metylobutanu:
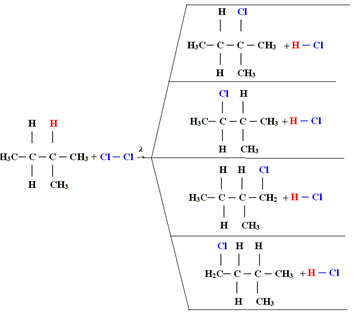
Ilość każdego związku będzie proporcjonalna do następującej kolejności łatwości, z jaką wodór jest uwalniany do cząsteczki:

Zatem w powyższym przypadku największą ilością będzie 2-metylo-2-chlorobutan, a najmniejszą będzie 2-metylo-1-chlorobutan.
2. Halogenacja benzenu: Benzen zwykle nie reaguje z chlorem lub bromem. Jeśli jednak jako katalizator stosuje się kwas Lewisa (zwykle stosuje się FeCl)3, luty3 lub AlCl3, wszystkie w postaci bezwodnej), benzen łatwo reaguje w reakcji halogenowania.
Chlorek i bromek żelazowy można otrzymać po prostu dodając żelazo do mieszaniny i w ten sposób reaguje z halogenem i wytwarza kwas Lewisa:
2 Fe + 3 Br2 → 2 lutego Fe3
Zobacz przykład halogenowania benzenu i jego mechanizm:
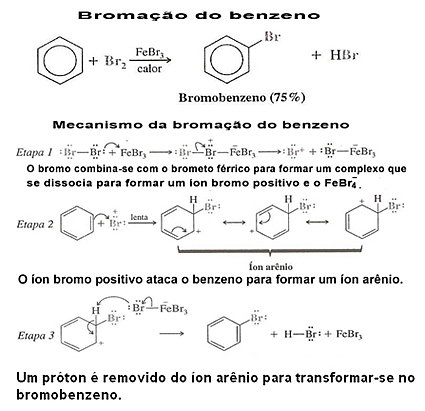
3. Halogenowanie pochodnych benzenu:W takich przypadkach podstawieniem kieruje podstawnik lub grupa funkcyjna, która jest przyłączona do pierścienia aromatycznego. Aby zobaczyć, jak to się dzieje, przeczytaj teksty ”Radykały kierujące w pierścieniu benzenowym" i "Elektroniczne efekty rodników meta i orto-dyrektorów”.
Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/reacoes-organicas-halogenacao.htm
