Aluminium pozyskiwane jest w procesach metalurgicznych. Metalurgia to dziedzina zajmująca się badaniem przemian rud w metale lub stopy metali. Metodą tą otrzymuje się kilka metali, takich jak miedź, tytan, żelazo i mangan.
W przypadku aluminium główną rudą stosowaną jest boksyt (rysunek), który zawiera uwodniony tlenek glinu (Aℓ2O3. x H2O) i różne zanieczyszczenia.

W metalurgii aluminium występują następujące cztery etapy:
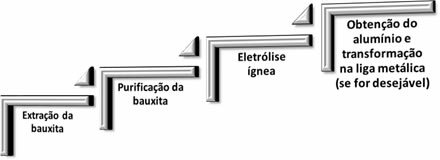
Gdy tlenek glinu (Aℓ2O3(s)) jest oddzielony od boksytu, jego nazwa staje się glinka.
Wcześniej wykonano następujące czynności: tlenek glinu potraktowano kwasem chlorowodorowym w celu wytworzenia chlorku glinu; który został umieszczony w reakcji z metalicznym potasem lub sodem, powodując redukcję związku i dając metaliczny glin:
A2O3(s) + 6 HCℓ(tutaj)→ 4 AℓCℓ3(aq) + 3 godz2O(ℓ)
ACℓ3(aq) + 3K(y)→ 3 KCℓ(y) + A(y)
Jednak ta metoda była bardzo kosztowna i nieefektywna, dlatego aluminium uznano za metal rzadki.
Ale w 1886 roku dwóch naukowców oddzielnie opracowało wspomnianą powyżej metodę, w której zastosowano elektrolizę magmową. Tymi naukowcami byli Amerykanin Charles M. Halla i Francuza Paula Héroulta, więc tę metodę zaczęto nazywać
Proces Halla-Heroulta lub po prostu,Proces Hall, natomiast Karol M. Hall go opatentował.Kluczową kwestią, którą odkryli, było to, jak zrobić płynny tlenek glinu, aby to zrobić. być w stanie przeprowadzić elektrolizę zapłonową, ponieważ problem polegał na tym, że jego temperatura topnienia była wyższa 2000°C. Użyli topnika, rudy kriolitu (Na3AℓF6), który był w stanie obniżyć temperaturę topnienia tlenku glinu do około 1000°C.
Tak więc, jak pokazano na poniższym schemacie, ta mieszanina tlenku glinu i kriolitu została umieszczona w naczyniu elektrolitycznym ze stali pokrytej węglem. Przez tę stopioną mieszaninę przepływa prąd elektryczny. Ścianki pojemnika stykające się z mieszaniną pełnią rolę ujemnego bieguna elektrolizy (katody), gdzie następuje redukcja kationów glinu. Anoda (biegun dodatni) to cylindry wykonane z grafitu lub węgla, czyli obydwa wykonane z węgla, gdzie następuje utlenianie anionów tlenu:
Reakcja połówkowa katody: 4 Aℓ3+(ℓ) + 12 i- → 4 Aℓ(ℓ)
Połowa reakcji anody: 6 O2-(ℓ) → 12 i- + 3 O2(g)
Powstający tlen reaguje z węglem w anodzie, a także generuje dwutlenek węgla:
3 O2(g) + 3 stopni Celsjusza(y) → 3 CO2(g)
Tak więc ogólna reakcja i schemat tej elektrolizy magmowej, która powoduje powstanie glinu, jest określony wzorem:

Otrzymane aluminium jest w postaci płynnej, ponieważ jego temperatura topnienia wynosi 660,37 ºC, czyli jest niższa niż mieszanina tlenku glinu i kriolitu. Aluminium jest również gęstsze niż mieszanka i dlatego osadza się na dnie pojemnika, gdzie jest gromadzone.
Do produkcji 1 tony aluminium wykorzystuje się:
- 4 do 5 ton boksytu, skąd około 2 tony tlenku glinu;
- 50 kilogramów kriolitu (Nie ma wielu naturalnych rezerw kriolitu, dlatego zwykle pozyskiwany jest on poprzez jego syntezę z fluorytu (CaF2), najobficiej występujący minerał w przyrodzie);
- 0,6 tony węgla dla elektrod.
Roczna produkcja aluminium przekracza 27,4 mln ton.
Wśród głównych stopów aluminium wyróżniamy:

Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/obtencao-aluminio-por-meio-eletrolise.htm
