TEN łagodne utlenianie w alkenach to reakcja organiczna przeprowadzana, gdy dany alken umieszcza się w pożywce utworzonej na bazie wody i soli nadmanganianu potasu (KMnO4), sól, która jest powszechnie nazywana Odczynnik Bayera.
Powstały produkt nazywa się alkohol wicynalne, czyli alkohole, które mają dwie grupy hydroksylowe (OH-) umieszczone na sąsiednich węglach, zgodnie z następującym wzorem ogólnym:
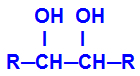
UWAGA: R może być rodnikiem lub atomami wodoru.
Odczynnik Bayera
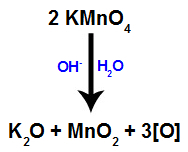
Kiedy Odczynnik Bayera (KMnO4) miesza się z wodą w obecności zasady nieorganicznej (OH-), reaguje i tworzy tlenek potasu (K2O), dwutlenek manganu (MnO2) i rodzących się tlenów (wolny tlen, reprezentowany przez [O]). Zobacz zrównoważone równanie procesu.

Te powstające tlenki powstające z odczynnika Bayera są odpowiedzialne za łagodną reakcję utleniania w alkenach (jak zobaczymy w kolejnych punktach).
Mechanizmy łagodnej reakcji utleniania w alkenach
1. mechanizm: tworzenie powstających tlenów z odczynnika Bayera;
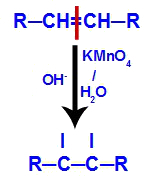
Drugi mechanizm: Atak powstających tlenów na podwójne wiązanie obecne w alkenach, powodujący rozerwanie wiązanie pi i w konsekwencji tworzenie swobodnej wartościowości w każdym z węgli związanych z łącze pi.
3. mechanizm: Powstające tlenki łączą się z hydroniami (H+) powstały w wyniku samojonizacji wody, w wyniku czego powstają grupy hydroksylowe (OH-).
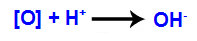
Czwarty mechanizm: Połączenie grup hydroksylowych utworzonych w każdej z wolnych wartościowości znajdujących się na węglach, w których znajdowało się wiązanie pi, tworząc wicynalny dialkohol.

Przykłady łagodnych reakcji utleniania w alkenach
→ Łagodna reakcja utleniania na but-2-enie
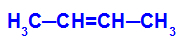
Wzór strukturalny but-2-en
Początkowo podwójne wiązanie między węglami 2 i 3 alkenu zostaje zerwane przez atak powstających tlenów, tworząc wolną wartościowość (ślad pionowy) na węglach 2 i 3.

Zerwanie wiązania pi między węglami 2 i 3 w but-2-en
Następnie powstający tlen łączy się z hydronium (H+) z jonizacji wody, tworząc grupy hydroksylowe (OH-), które wiążą się z wolną wartościowością węgli 2 i 3, dając wicynalny dialkohol.
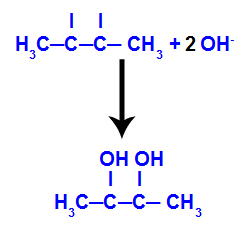
Alkohol wicynalny powstały z but-2-enu
→ Łagodna reakcja utleniania na 2-metylo-propenie
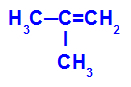
Wzór strukturalny 2-metylo-propenu
Początkowo podwójne wiązanie między węglami 1 i 2 alkenu zostaje zerwane przez atak powstających tlenów, tworząc wolną wartościowość (ślad pionowy) na węglach 1 i 2.
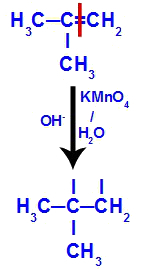
Zerwanie wiązania pi między węglami 1 i 2 w 2-metylopropenie
Następnie powstający tlen łączy się z hydronium (H+) z jonizacji wody, tworząc grupy hydroksylowe (OH-), które wiążą się z wolną wartościowością węgli 1 i 2, dając wicynalny dialkohol.
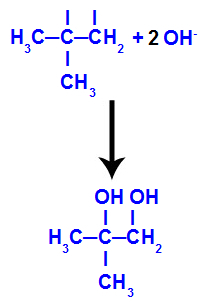
Alkohol wicynalny powstały z 2-metylo-propenu
Przeze mnie Diogo Lopes Dias
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/oxidacao-branda-alcenos.htm