Do funkcje tlenu są grupą związki organiczne które mają atomy tlenu przyłączone do łańcucha węglowego. Czy oni są:
alkohol;
keton;
aldehyd;
kwas karboksylowy;
ester;
eter.
Przeczytaj też:Węglowodory — związki zbudowane z węgla i wodoru
Tematyka tego artykułu
- 1 - Podsumowanie funkcji tlenu
- 2 - Lekcja wideo na temat funkcji tlenu
- 3 - Jakie są funkcje tlenu?
- 4 - Znaczenie funkcji tlenowych
- 5 - Alkohol
- 6 - Keton
- 7 - Aldehyd
- 8 - Kwas karboksylowy
- 9 - Ester
- 10 - Eter
- 11 - Rozwiązane ćwiczenia dotyczące funkcji tlenowych
Podsumowanie funkcji tlenu
Funkcje tlenu to grupa związków zawierających atom tlenu. tlen przyłączone bezpośrednio do łańcucha węglowego.
Różne grupy funkcyjne tlenu charakteryzują się specyficznym układem strukturalnym atomy, zwaną grupą funkcyjną.
Grupy funkcyjne są odpowiedzialne za właściwości każdej funkcji organicznej.
Funkcje tlenu to: alkohol, keton, aldehyd, kwas karboksylowy, ester i eter.
Lekcja wideo na temat funkcji tlenu
Jakie są funkcje tlenu?
Dotlenione funkcje organizmu to takie, które mają atom tlenu związany z atomem tlenu węgiel łańcucha węglowego.
Funkcje tlenu to:
alkohol;
keton;
aldehyd;
kwas karboksylowy;
ester;
eter.
Funkcje organiczne są identyfikowane przez ich grupę funkcjonalną, który jest strukturalnym układem atomów lub wiązań, odpowiedzialnym za charakterystyczne właściwości tego zestawu związków.
Teraz nie przestawaj... Po reklamie jest więcej ;)
Znaczenie funkcji tlenu
Obecność tlenu w związkach organicznych potrafi zmieniać właściwości związków, w porównaniu z odpowiednim węglowodorem, z taką samą liczbą atomów węgla.
Funkcje tlenu charakteryzują się występowaniem grup hydroksylowych, karbonylowych lub karboksylowych. A obecność atomu tlenu zwiększa charakter polarny związków, czyniąc je bardziej hydrofilowymi, czyli zwiększając ich powinowactwo do woda.
Występowanie funkcji tlenowych odpowiada również za rodzaj siła międzycząsteczkowadziałające między cząsteczkami. Charakter i intensywność oddziaływań międzycząsteczkowych wpływa na rozpuszczalność oraz temperatury topnienia i wrzenia.
Poniższa tabela przedstawia porównanie niektórych właściwości trzech związków, które mają taką samą liczbę atomów węgla, ale różnią się obecnością utlenionych grup funkcyjnych.
Kompost organiczny | |||
Butan (C4H10) |
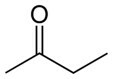
Butanon (C4H8O) |
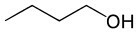
Butanol (C4H10O) |
|
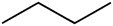 |
 |
 |
|
funkcja organiczna |
Węglowodór |
keton (funkcja tlenu) |
Alkohol (funkcja tlenu) |
Biegunowość |
apolarny |
Polarny |
Polarny |
temperatura topnienia |
-138,3°C |
-86°C |
-89°C |
temperatura wrzenia |
-0,5°C |
80°C |
118°C |
Dominująca siła międzycząsteczkowa |
Indukowany dipol |
stały dipol |
wiązania wodorowe |
Alkohol
Organiczny alkohol funkcyjny ma grupę hydroksylową (-OH) związaną bezpośrednio z nasyconym węglem, czyli ten atom węgla, który tworzy tylko wiązania pojedyncze.
Grupa funkcyjna alkoholi: R-OH (hydroksyl).
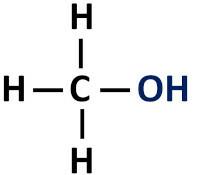
alkohole są klasyfikuje się według rodzaju węgla, do którego przyłączona jest grupa hydroksylowa. Alkohole pierwszorzędowe mają grupę hydroksylową przyłączoną do pierwszorzędowego węgla. Alkohole drugorzędowe mają grupę hydroksylową przyłączoną do drugorzędowego węgla, a alkohole trzeciorzędowe mają grupę -OH przyłączoną do trzeciorzędowych atomów węgla.
Związek organiczny, który ma tylko jedną grupę hydroksylową, nazywa się monoalkoholem. Jeśli ma dwie grupy hydroksylowe, nazywa się to dialkoholem. Powyżej tego cząsteczki nazywane są polialkoholami.
A nazewnictwo alkoholi postępuje zgodnie z zaleceniem Iupac (Międzynarodowej Unii Chemii Czystej i Stosowanej), uwzględniając składanie nazw struktur chemicznych w trzech częściach:
Przedrostek – związany z liczbą atomów węgla.
Infiks – odnosi się do rodzaju wiązania chemicznego utworzonego między atomami węgla.
Przyrostek – związany z grupą funkcjonalną. W przypadku alkoholi stosuje się przyrostek -Witam.
Zobacz przykłady:
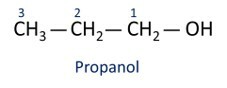
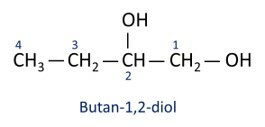
O głównym alkoholem jest etanl (CH3CH2OH), stosowany jako paliwo, w napojach alkoholowych, jako rozpuszczalnik chemiczny, środek czyszczący i dezynfekujący.
keton
Funkcja ketonu organicznego odpowiada karbonylowa grupa funkcyjna (C=O), znajdująca się pomiędzy dwoma atomami węgla łańcucha węglowego.
Grupa funkcjonalna ketonów: R1–(C=O)–R2.

Ketony są klasyfikowane według liczby grup karbonylowych:
Monoketony – mają jedną grupę karbonylową.
Diketony – mają dwie grupy karbonylowe.
Politony – mają więcej niż dwie grupy karbonylowe.
A Nomenklatura dla ketonów przestrzega zasad Iupac, ale z różnicą w pisowni sufiksu. Ketony są identyfikowane przez przyrostek -na.
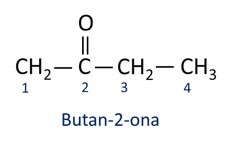
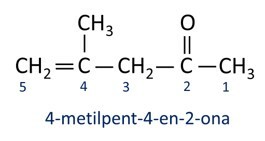
Ogólnie rzecz biorąc, ketony znajdują zastosowanie w produkcji innych chemikaliów i farmaceutyków. W przemyśle ketony są stosowane jako rozpuszczalniki do farb, barwników i lakierów. Jednym z najbardziej znanych ketonów jest propanon, popularnie znany jako aceton. Roztwory acetonowe służą do usuwania lakieru do paznokci.
Przeczytaj też:Amidy — związki, które mają atom azotu przyłączony do karbonylu
aldehyd
Organiczna funkcja aldehydowa to charakteryzuje się obecnością karbonylowej grupy funkcyjnej, którego atom węgla ma wiązanie wodorowe.
Grupa funkcyjna aldehydów: H–C=O (formyl).
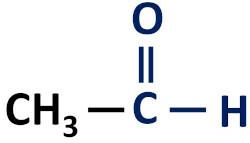
Aldehydy zawsze występują na końcu łańcuchów węglowych, ponieważ ich atom węgla musi być związany z co najmniej jednym atomem wodoru.
A nazewnictwo związków aldehydowych jest zgodny z zasadami IUPAC, różniącymi się sufiksem. Aldehydy są identyfikowane przez przyrostek -glin.
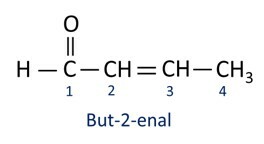
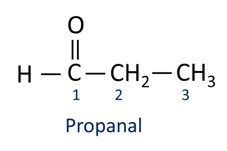
Aldehydy są wykorzystywane przemysłowo do produkcji perfum i przyprawa, ponieważ jego zapach i smak różnią się w zależności od długości łańcucha węglowego. Związki aldehydowe wykorzystywane są również m.in. do produkcji środków czystości, leków, polimerów. Aldehydy o krótkich łańcuchach węglowych mogą być stosowane jako środki konserwujące, takie jak słynne formalina, który jest aldehydem o nazwie metanal.

kwas karboksylowy
Funkcja organicznego kwasu karboksylowego jest identyfikowana przez obecność karboksylowej grupy funkcyjnej (-COOH).
Grupa funkcyjna kwasów karboksylowych: –(C=O)OH lub –COOH.

Związki należące do tej organicznej grupy funkcyjnej są słabymi kwasami, ponieważ łatwo uwalniają jony H+ w roztworze wodnym.
A nazewnictwo kwasów karboksylowych jest zgodny z zasadami Iupac, jednak termin „kwas” pojawia się przed przedrostkiem wskazującym liczbę atomów węgla, a zastosowanym przyrostkiem jest -oic.
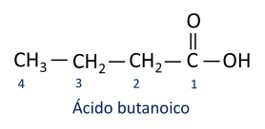
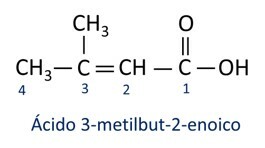
O najczęściej spotykanym kwasem karboksylowym w życiu codziennym jest Kwas octowy, substancja obecna w occie. Witamina C, występująca w wielu owocach cytrusowych, jest cząsteczką organiczną zwaną kwasem askorbinowym.
Ester
Organiczna funkcja estrowa jest identyfikowany przez obecność karbonylowej grupy funkcyjnej, którego atom węgla ma ligand tlenowy.
Grupa funkcyjna estrów: –R–(C=O)O–R'.
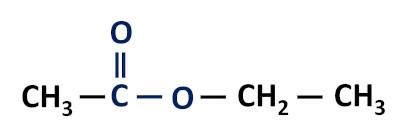
Estry są pochodne kwasów karboksylowych, różniące się od nich tym, że mają rodnik alkilowy przyłączony do atomu tlenu zamiast atomu wodoru.
Cząsteczki należące do estrowej grupy funkcyjnej powstają w reakcji między kwasem karboksylowym a alkoholem, reakcji znanej jako estryfikacja.
Zasady dot nazewnictwo estrów zdefiniowane przez Iupac uważają, że cząsteczka składa się z dwóch części:
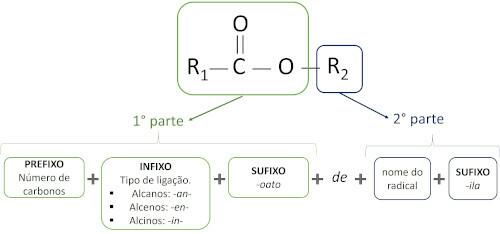
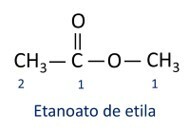
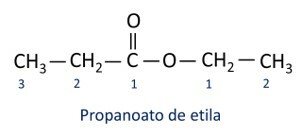
Główną cechą estrów jest ich zdolność do symulacji smaku i zapachu naturalnej żywności, w zależności od długości łańcuchów węglowych (R1 i R2). Z tego powodu estry są szeroko stosowane jako środki aromatyzujące w przemyśle spożywczym, w produkcji farmaceutyków, perfum i kosmetyków.
Eter
Eterowa funkcja organiczna to charakteryzujący się posiadaniem atomu tlenu pomiędzy dwoma łańcuchami węglowymi.
Grupa funkcyjna eterów: R–O–R.

Etery są substancjami wysoce łatwopalnymi, o charakterystycznym i silnym zapachu.
A oficjalna nomenklatura Iupac dla eterów następuje po przedrostku kolejności + wrostku + przyrostku. Jednak strona cząsteczki, która ma mniej atomów węgla, otrzymuje przyrostek -oksy, podczas gdy dłuższy łańcuch węglowy jest nazywany tak, jakby był węglowodorem, otrzymując przyrostek -o.
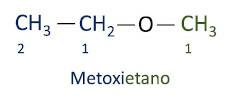
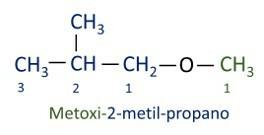
Etery są stosowany jako rozpuszczalnik do farb, żywic, olejów i tłuszczów. Dzięki temu są wykorzystywane w różnych procesach przemysłowych i farmaceutycznych. Eter był kiedyś używany jako środek znieczulający, obecnie jest zastępowany innymi, bezpieczniejszymi substancjami.
Przeczytaj też:Związki nitrowe — związki zawierające w swojej cząsteczce grupy nitrowe (NO2).
Rozwiązane ćwiczenia dotyczące funkcji tlenu
Pytanie 1
(Uece) W chemii organicznej grupa funkcyjna jest zdefiniowana jako struktura molekularna, która nadaje substancjom podobne zachowanie chemiczne. Zestaw związków, które mają tę samą grupę funkcyjną, nazywa się funkcją organiczną. Zaznacz opcję, która poprawnie przedstawia związek i funkcję organiczną, do której należy.

Rezolucja:
litera C
Wśród alternatyw jedyną, która poprawnie wyraża grupę funkcyjną do nazwy funkcji chemicznej jest pozycja C. Organiczna funkcja estrowa jest zdefiniowana przez karbonylową grupę funkcyjną, której atom węgla ma również ligand tlenowy.
W pozycji A wyrażono eterową grupę funkcyjną.
W pozycji B wyrażono ketonową grupę funkcyjną.
W punkcie D wyrażono amidową grupę funkcyjną. aminy To jest amidy należą do funkcji azotowych.
pytanie 2
(UCS-RS) W V wieku pne. C., Hipokrates, grecki lekarz, napisał, że produkt z kory wierzby łagodził ból i obniżał gorączkę. Ten sam produkt, kwaśny proszek, wspominany jest nawet w tekstach starożytnych cywilizacji Bliskiego Wschodu, Sumeru, Egiptu i Asyrii. Rdzenni Amerykanie używali go również na bóle głowy, gorączkę, reumatyzm i drżenie. Lek ten jest prekursorem aspiryny, której budowę chemiczną przedstawiono poniżej.
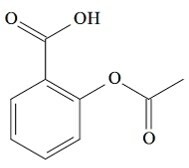
Organiczne funkcje obecne w strukturze aspiryny, przedstawione powyżej, to:
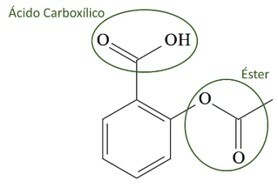
a) kwas karboksylowy i ester.
b) alkohol i eter.
c) amina i amid.
d) amina i eter.
e) aminokwas i alkohol.
Rezolucja:
Litera a
Ana Luiza Lorenzen Lima
Nauczyciel chemii
Aldehydy, związki karbonylowe, grupa karbonylowa, Główne aldehydy, Etanal, surowiec w przemyśle pestycydowym i medycznym, Metanal, formaldehyd, przemysł tworzyw sztucznych i żywic.
Ketony, substancje organiczne, karbonylowa grupa funkcyjna, otrzymywanie rozpuszczalnika do lakierów do paznokci, propanon, ciała ketonowe we krwi, ekstrakcja olejów i tłuszczów z nasion roślin, rozpuszczalniki organiczny.
Naucz się sortować ten element w łańcuchu.
Znajomość składu chemicznego, źródeł produkcji i zastosowań wielu związków organicznych, takich jak między innymi aceton, alkohol, eter.
Dowiedz się, jak powstała Nomenklatura IUPAC, jakie są jej główne cele i poznaj podstawowe zasady nazewnictwa związków organicznych.
Naucz się krok po kroku jak nazywać gałęzie związków organicznych.
Dowiedz się o wpływie struktury organicznej na polarność.
Znać zależność między polarnością a temperaturą wrzenia związków organicznych.
Zrozum, w jaki sposób w reakcji estryfikacji powstają estry, bardzo ważne związki w naszym codziennym życiu.
Dowiedz się o kwasach karboksylowych. Dowiedz się, czym się charakteryzują, jak się nazywają i które z nich są obecne w życiu codziennym.