Osmoza to ruch wody, który odbywa się wewnątrz komórek przez półprzepuszczalną błonę.
W tym procesie cząsteczki wody przemieszczają się z mniej skoncentrowanego ośrodka do bardziej skoncentrowanego ośrodka.
Dlatego osmoza służy do zrównoważenia dwóch stron membrany, powodując rozcieńczenie ośrodka bogatego w substancję rozpuszczoną przez rozpuszczalnik, którym jest woda.
Jak zachodzi osmoza?
Osmoza jest uważana za transport pasywny, tak jak w przejściu przez błonę żadna energia nie jest marnowana.
W procesie osmozy woda, która jest rozpuszczalnikiem, ma tendencję do przekraczania półprzepuszczalnej membrany w celu wyrównania stężenia roztworu. Czynność tę prowadzi się do ustabilizowania ciśnienia osmotycznego.
Dlatego woda w naturalny sposób przemieszcza się z mniej skoncentrowanego obszaru do bardziej skoncentrowanego.
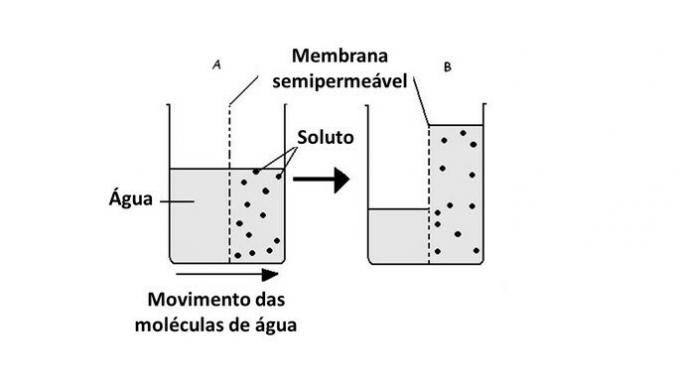
Przejście wody z jednego podłoża do drugiego odbywa się w komórkach za pomocą białek transportujących w błonie, akwaporyn. Tak więc osmoza występuje, gdy występuje różnica w stężeniu między środowiskiem zewnętrznym i wewnętrznym komórki.
Wynik osmozy jest wykorzystywany w procesach wymiany składników odżywczych w komórkach zwierzęcych i roślinnych.
Przeczytaj także o Transport pasywny i Transport aktywny.
Roztwór hipotoniczny, izotoniczny i hipertoniczny
Jak widzieliśmy, proces osmozy ma na celu wyrównanie stężeń roztworów, aż do osiągnięcia równowagi. Do tego mamy następujące rodzaje rozwiązań:
- roztwór hipertoniczny: przedstawia wyższe ciśnienie osmotyczne i stężenie substancji rozpuszczonych.
- roztwór hipotoniczny: przedstawia niższe ciśnienie osmotyczne i stężenie substancji rozpuszczonych.
- roztwór izotoniczny: stężenie substancji rozpuszczonej i ciśnienie osmotyczne są równe, osiągając w ten sposób równowagę.
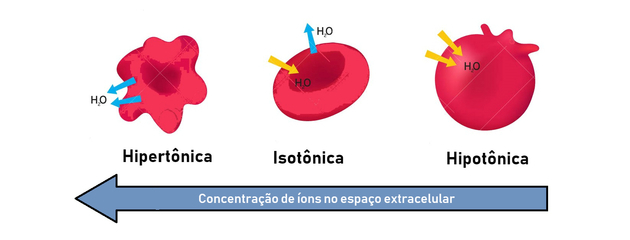
Dlatego osmoza występuje pomiędzy hipertonicznym (bardziej skoncentrowanym) a hipotonicznym (mniej skoncentrowanym) sposobem generowania równowagi.
przykłady osmozy
W komórkach błona plazmatyczna jest otoczką utworzoną przez dwuwarstwę lipidową, która utrudnia ruch wody w komórce. Istnieją jednak wyspecjalizowane w jego budowie białka, akwaporyny, które pełnią funkcję kanałów ułatwiających przechodzenie cząsteczek wody.
W środowisku hipertonicznym komórki mają tendencję do kurczenia się, gdy tracą wodę. Komórka umieszczona w pożywce hipotonicznej może pęcznieć aż do pęknięcia, ponieważ następuje ruch wody do komórki.
Zobacz poniżej, jak osmoza zachodzi w komórkach zwierzęcych i roślinnych.
Osmoza w komórce zwierzęcej
kiedy komórka zwierzęca, podobnie jak krwinki czerwone, są eksponowane na media o różnych stężeniach, ruch wody w komórce zachodzi w następujący sposób:
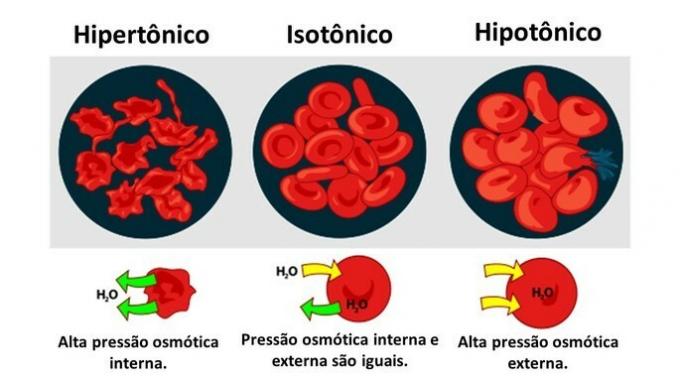
Gdy pożywka jest bogata w substancję rozpuszczoną, roztwór, który jest hipertoniczny w stosunku do cytoplazmy, komórki tracą wodę do pożywki i więdną.
Gdy pożywka jest uboga w substancję rozpuszczoną, roztwór hipotoniczny, cząsteczki wody mają tendencję do wnikania do komórki i chociaż membrana jest odporna, w zależności od ilości może wystąpić rozerwanie.
Osmoza komórek roślinnych
Ruch wody w komórkach roślinnych odbywa się pomiędzy wakuolą komórkową a środowiskiem zewnątrzkomórkowym.
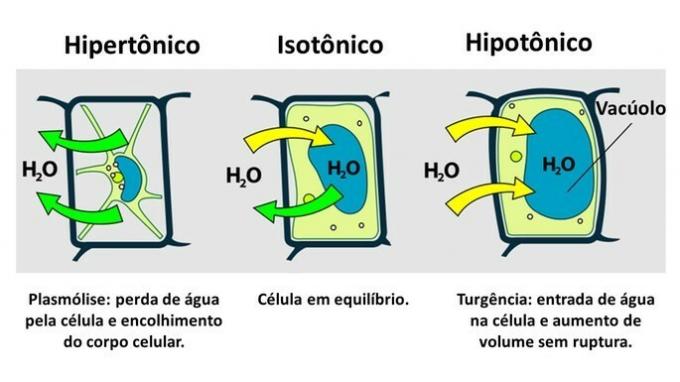
TEN komórka roślinna ma, oprócz błony komórkowej, bardzo odporną ścianę komórkową, którą tworzy celuloza.
Dlatego, w przeciwieństwie do komórki zwierzęcej, komórka roślinna jest odporna na rozerwanie, gdy jest umieszczona w środowisku hipotonicznym, gdzie woda ma tendencję do wnikania do komórki. Komórka pęcznieje, zwiększając swoją objętość, ale ściana komórkowa zapobiega pękaniu.
Utrata wody przez komórkę roślinną, która jest umieszczona w środowisku hipertonicznym, nazywana jest plazmolizą. Wejście wody do wakuoli, gdy komórka znajduje się w środowisku hipotonicznym, nazywa się turgencją, gdy następuje wzrost objętości komórki.
Jak ciśnienie osmotyczne wpływa na osmozę?
Substancją rozpuszczoną jest każda substancja, którą można rozcieńczyć w rozpuszczalniku, takim jak cukier rozpuszczony w wodzie. Podczas gdy ciśnienie osmotyczne to ciśnienie, które powoduje ruch wody.
Ponieważ osmoza jest procesem, który zachodzi od najmniej stężonego (hipotonicznego) do najbardziej stężonego (hipertonicznego) ośrodka w szukaj równowagi, ciśnienie osmotyczne to ciśnienie wywierane na system, aby zapobiec powstawaniu osmozy naturalnie.
Dlatego im większa jest różnica stężeń pomiędzy ośrodkiem hipertonicznym i hipotonicznym, tym większe powinno być ciśnienie osmotyczne przykładane do bardziej stężonego roztworu, aby uniknąć osmozy.
Dowiedz się więcej o ciśnienie osmotyczne.
Czym jest odwrócona osmoza i jak działa
Odwrócona osmoza to przepływ wody w kierunku przeciwnym do osmozy. W ten sposób woda przechodzi z bardziej stężonego roztworu do mniej stężonego.
Odwrócona osmoza odbywa się poprzez zastosowanie ciśnienia większego niż naturalne ciśnienie osmotyczne.
Ponieważ membrana półprzepuszczalna umożliwia jedynie przepływ rozpuszczalnika (czystej wody), zatrzymuje substancje rozpuszczone.
Przykładem odwróconej osmozy jest przekształcenie słonej wody w słodką w procesie odsalania.
Dowiedz się więcej o odwrócona osmoza.
Różnica między osmozą a dyfuzją
Dyfuzja to przechodzenie bardzo małych cząsteczek gazów i substancji rozpuszczonych w wodzie przez błona plazmatyczna. W takim przypadku cząsteczki substancji rozpuszczonej przesuną się z bardziej stężonego podłoża do mniej stężonego podłoża. Poruszają się po gradiencie stężeń i rozchodzą się po dostępnej przestrzeni.
TEN ułatwiona dyfuzja jest to przechodzenie przez błonę substancji, które nie rozpuszczają się w lipidach, za pomocą białek przenikających dwuwarstwę lipidową.
Podobnie jak osmoza, dyfuzja jest również uważana za transport pasywny, ponieważ występuje na korzyść gradientu stężeń.
Ciekawość
Wyrażenie „uczenie się przez osmozę” jest powszechnie używane przez studentów, którzy chcieliby uczyć się nowych treści bez konieczności nauki, czyli bez wysiłku.
Przeczytaj też:
- Substancja rozpuszczalna i rozpuszczalnik
- Pompa sodu i potasu
- Selektywna przepuszczalność


