Modele atomowe powstały z potrzeby wyjaśnienia budowy atomów. Kiedy przedstawiono nowe dowody na budowę atomów, nowy model atomowy próbował wyjaśnić odkrycia.
Greccy filozofowie Demokryt i Leucipo w V wieku; DO. zwany atomem, z greki ατoμoν, niepodzielna cząstka i najmniejsza część materii.
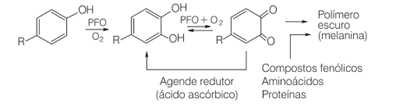
Chociaż koncepcja atomu jest stara, rozwój teorii atomowych sięga XIX i XX wieku. Dlatego głównymi modelami atomowymi opracowanymi w celu zrozumienia natury materii były:
- Model atomowy Daltona (1803) — „Model kuli bilardowej”
- Model atomowy Thomsona (1898) — „Model puddingu deszczowego”
- Model atomowy Rutherforda (1911) — „Model jądrowy”
- Model atomowy Bohra (1913) — „Model planetarny”
- Kwantowy model atomowy (1926) — „Elektroniczny model chmury”
Atomowy model Daltona
Pierwsza uznana próba opisania atomów została podjęta przez angielskiego naukowca Johna Daltona (1766-1844) w modelu, który stał się popularnie znany jako „kula bilardowa”.
Atom Daltona (1803): masywna, niepodzielna i niezniszczalna kula.

Według Daltona:
- Wszystkie substancje składają się z atomów;
- Atomy pierwiastka chemicznego są identyczne pod względem wielkości i właściwości, podczas gdy atomy różnych pierwiastków chemicznych są różne;
- Substancje powstają w wyniku reakcji chemicznej, która polega na rekombinacji atomów.
Punkty ujemne: Ponieważ elektrony nie były jeszcze znane, kiedy Dalton formułował swoją teorię, te cząstki, o których teraz wiemy, że są częścią atomów, nie były brane pod uwagę.
Dowiedz się więcej o Atomowy model Daltona.
Model atomowy Thomsona
Joseph John Thomson (1856-1940) był odpowiedzialny za odkrycie istnienia elektronów, cząstek obdarzonych ładunkiem ujemnym, wchodzących w skład atomów. Odkrycie to obaliło atomową teorię Daltona, że atom jest niepodzielny, ale składa się z jeszcze mniejszych cząstek i dlatego stał się znany jako „budyń rodzynkowy”.
Atom Thomsona (1898): dodatnio naładowana kula ze stałymi elektronami.

Według Thomsona:
- Atom jest elektrycznie obojętny;
- Elektrony przyczepiają się do dodatnio naładowanej powierzchni;
- Między elektronami rozłożonymi w atomach występuje odpychanie.
Punkty ujemne: Chociaż Thomson wziął pod uwagę istnienie elektronów, atom nie jest sferą dodatnią, ale raczej obdarzoną dodatnio naładowane cząstki, protony, zidentyfikowane w 1886 roku przez naukowca Eugene'a Goldsteina, a później potwierdzone przez Ernesta Rutherforda.
Dowiedz się więcej o Model atomowy Thomsona.
Model atomowy Rutherforda
Poprzez swoje eksperymenty Ernest Rutherford (1871-1937) zdołał wykazać, że atom nie jest niepodzielną cząstką, jak sądzono, ale że został utworzony z mniejszych cząstek.
Atom Rutherforda (1911): dodatnio naładowane jądro i elektrony znajdują się wokół niego w elektrosferze.
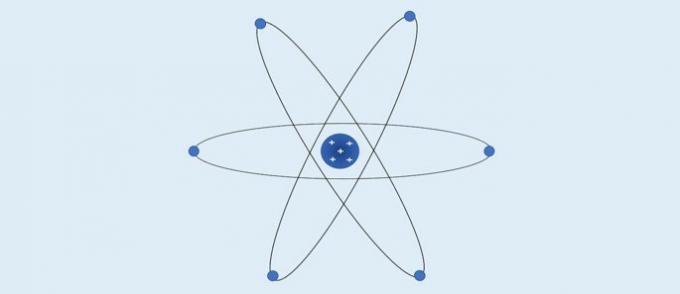
Według Rutherforda:
- Atom ma centralny obszar o wysokim stężeniu ładunku dodatniego;
- Masa atomu jest skoncentrowana w jego centralnym obszarze;
- Elektrony są lżejsze i znajdują się wokół jądra, regionu zawierającego wiele pustych przestrzeni.
Punkty ujemne: jądro atomowe zawiera nie tylko dodatnio naładowane cząstki, ale istnieją również inne cząstki subatomowe, neutrony, odkryte przez Jamesa Chadwicka w 1932 roku. Ponadto model zaproponowany przez Rutherforda nie wyjaśniał emisji światła przez atomy.
Dowiedz się więcej o Model atomowy Rutherforda.
Model atomowy Bohra
Próba wyjaśnienia, dlaczego elementy emitują charakterystyczne kolory po wystawieniu na działanie niektórych warunków i na podstawie Model atomowy Rutherforda, Niels Bohr (1885-1962) zaproponował teorię atomową, która wyjaśniała emisję światła w pewnych częstotliwości.
Atom Bohra (1913): elektrony poruszają się w ustalonych okrągłych warstwach wokół jądra.
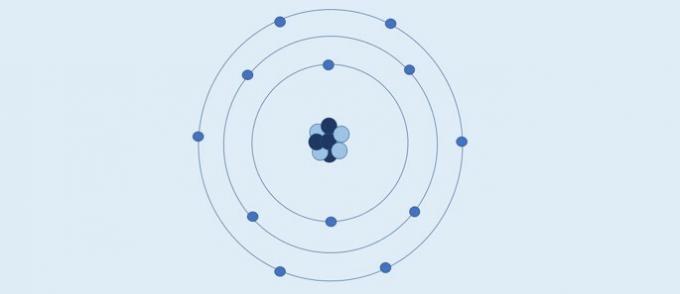
Według Bohra:
- Elektrony poruszają się w warstwach wokół jądra;
- Warstwy wokół rdzenia mają określone wartości energetyczne;
- Aby przejść na bardziej zewnętrzny poziom, elektron musi wchłonąć energię. Po powrocie do warstwy bliższej jądra elektron uwalnia energię.
Punkty ujemne: nie można powiedzieć, że elektrony krążą wokół jądra w stałych pozycjach, jak planety wokół Słońca.
Dowiedz się więcej o Model atomowy Bohra.
Kwantowy model atomowy
Wielu naukowców przyczyniło się do rozwoju mechaniki kwantowej, która stara się wyjaśnić „bardziej rzeczywistą” strukturę a atom przez połączenie kilku badań, a zatem jest najbardziej złożony.
Atom kwantowy (1926): jądro składa się z protonów (ładunek dodatni) i neutronów (ładunek zerowy), a elektrony (ładunek ujemny) tworzą chmurę elektronową wokół jądra.
Zgodnie z kwantowym modelem atomowym:
- Jądro składa się z protonów i neutronów. Ponieważ tylko protony mają ładunek, jądro jest naładowane dodatnio;
- Elektrony tworzą elektronową chmurę wokół jądra;
- Elektrony poruszają się po orbitalach, w przestrzeni trójwymiarowej;
- Nie można określić dokładnej pozycji elektronu. Dokonuje się obliczeń, które określają prawdopodobieństwo regionu, w którym elektron będzie w danym czasie.
ty liczby kwantowe mają funkcję lokalizowania elektronów. Czy oni są:
O główna liczba kwantowa (n) reprezentuje poziomy energetyczne, czyli warstwy elektronowe atomu.
O wtórna liczba kwantowa (l) wskazuje podpoziomy energii, czyli podpoziom energii, do którego należy elektron.
O magnetyczna liczba kwantowa (m) to ta, która wskazuje orbitę, na której spotykają się elektrony.
Dowiedz się więcej o modele atomowe i sprawdź swoją wiedzę z ćwiczenia na modelach atomowych.