O Schemat faz to wykres, który pozwala określić, w jakim stanie fizycznym znajduje się substancja w danym momencie, znając jej temperaturę i ciśnienie.
Pomiary laboratoryjne służą do budowy diagramu fazowego danej substancji.
Diagram podzielony jest na trzy obszary, które reprezentują stan stały, ciekły i pary.
Kropki na liniach, które wyznaczają te regiony, wskazują wartości temperatury i ciśnienia, jakie substancja może znajdować się w dwóch stanach.
Diagram fazowy składa się z następujących elementów:
- krzywa Połączenie: oddziela obszary odpowiadające stanom stałym i ciekłym.
- krzywa odparowanie: oddziela obszary odpowiadające fazie ciekłej i parowej.
- krzywa sublimacja: oddziela obszary odpowiadające fazie stałej i fazy gazowej.
- potrójny punkt: punkt przecięcia trzech krzywych (fuzja, waporyzacja i sublimacja). Ten punkt wskazuje wartości temperatury i ciśnienia, które substancja może jednocześnie znajdować się w trzech stanach.
- Punkt krytyczny: wskazuje najwyższą temperaturę, w której substancja jest parą. Od tego momentu nie jest już możliwe rozróżnienie między stanami ciekłymi i parowymi. W temperaturach powyżej punktu krytycznego substancja staje się gazem.
Na poniższym rysunku przedstawiamy reprezentację diagramu fazowego:

Przeczytaj więcej na: Zmiany stanu fizycznego.
krzywa topnienia
Ogólnie rzecz biorąc, substancje zwiększają swoją objętość, gdy ulegają stopieniu i, przeciwnie, zmniejszają objętość, gdy zestalają się. W konsekwencji wzrost ciśnienia prowadzi do wzrostu temperatury topnienia (temperatury topnienia).
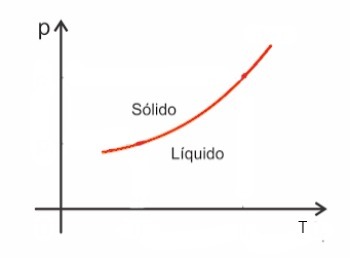
Jednak są wśród nich wyjątki woda, która podczas topnienia zmniejsza swoją objętość. W takim przypadku wzrost ciśnienia powoduje spadek temperatury topnienia.
Tak więc krzywa topnienia tych substancji będzie wyglądać tak:
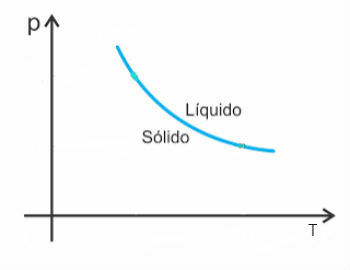
Przykład
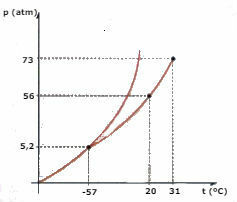
Rozważ wykres fazy CO2 (dwutlenek węgla) przedstawiony poniżej i odpowiedz na pytania:
a) W jakiej fazie jest CO2 , gdy twoja temperatura wynosi -60 °C, a ciśnienie 50 atm?
b) pewna ilość CO2 ciecz jest poddawana ciśnieniu 56 atm i jest zamknięta w pojemniku. Jeśli ciecz jest podgrzewana, utrzymując stałe ciśnienie, jaka jest wartość temperatury, przy której nastąpi parowanie?
c) Jaka jest wartość temperatury i ciśnienia punktu potrójnego CO2?
d) Kawałek suchego lodu (CO2) jest poddawany ciśnieniu 2 atm. Jest podgrzewany, utrzymując stałe ciśnienie. W pewnym momencie zaczyna następować zmiana fazy. Jak nazywa się ta zmiana?
Rozkład:
a) Obserwując wykres dochodzimy do wniosku, że CO2 będzie w fazie stałej.
b) Parowanie nastąpi, gdy temperatura osiągnie 20°C.
c) Punkt potrójny odpowiada przecięciu trzech krzywych, w przypadku CO2, gdy ma temperaturę -57°C i ciśnienie 5,2 atm, te trzy stany fizyczne mogą współistnieć.
d) Nastąpi sublimacja
Aby dowiedzieć się więcej, przeczytaj także:
- Zestalenie
- Temperatura topnienia i wrzenia
- Odparowanie
- Kondensacja
Rozwiązane ćwiczenia
1) Wróg - 2000
Nawet dzisiaj bardzo często ludzie używają glinianych pojemników (kawałków lub nieszkliwionych naczyń ceramicznych) do przechowywania wody w temperaturze niższej niż temperatura otoczenia. To dlatego, że:
a) glina izoluje wodę od otoczenia, zawsze utrzymując ją w niższej temperaturze niż jej własna, jakby była styropianem.
b) glina ma moc „zamrażania” wody dzięki swojemu składowi chemicznemu. W reakcji woda traci ciepło.
c) glina jest porowata, co umożliwia przepływ wody. Część tej wody odparowuje, zabierając ciepło z moringi i reszty wody, które są następnie schładzane.
d) glina jest porowata, co pozwala wodzie osadzać się na zewnątrz dzbanka. Woda na zewnątrz ma zawsze wyższą temperaturę niż wewnątrz.
e) Moringa to rodzaj naturalnej lodówki, uwalniającej higroskopijne substancje, które w naturalny sposób obniżają temperaturę wody.
Alternatywa c: glina jest porowata, umożliwiając przepływ wody. Część tej wody odparowuje, zabierając ciepło z moringi i reszty wody, które są następnie schładzane.
2) Ita - 2013
Rozważ hipotetyczny diagram fazowy przedstawiony schematycznie na poniższym rysunku:

Co reprezentują punkty A, B, C, D i E?
punkt A: punkt sublimacji
punkt B: potrójny punkt
Punkt C: temperatura topnienia/krzepnięcia
punkt D: punkt parowania/kondensacji
punkt E: punkt krytyczny
3) UECE - 2009
Patrząc na diagram faz PT pokazany poniżej. Można słusznie wywnioskować, że substancja, która przeszła proces sublimacji, podąża trajektorią:

a) X lub Y
b) Y lub U
c) U lub V
d) T lub X
Alternatywa b: Y lub U


