Rozważmy poniższą ogólną reakcję odwracalną, gdzie małe litery odpowiadają zrównoważonym współczynnikom reakcji, a duże litery to reagenty, a wszystkie produkty są w stanie gazowym:

Rozpatrując każdy z kierunków reakcji z osobna, ich szybkości rozwoju (Td) wyrażają wzorem:
*Reakcja bezpośrednia: aA + bB → cC + dD
Wszystkobezpośredni = Kbezpośredni. [TA]. [B]b
*Reakcja odwrotna: cC + dD → aA + bB
Wszystkoodwrotność = Kodwrócić. [DO]do. [RE]re
Stała równowagi chemicznej pod względem stężenia w ilości materii (Kdo) oraz pod względem ciśnienia cząstkowego (KP) otrzymamy dzieląc Kbezpośredni przez Kodwrócić.
Więc mamy:
Kbezpośredni. [TA]. [B]b = 1 → Kbezpośredni__ = __[DO]do. [RE]re___
Kodwrócić. [DO]do. [RE]re Kodwrócić [TA]. [B]b
Istota, Kdo =_Kbezpośredni_
Kodwrócić
Więc mamy:
Kdo =__[DO]do. [RE]re___ lub KP =__(Praca)do. (pD)re___ |
Gdzie p jest ciśnieniem cząstkowym każdej substancji w równowadze.
W ten sposób każde stężenie jest podnoszone do wykładnika odpowiadającego współczynnikowi danej substancji w reakcji, a Kdo nie ma jednostki*.
Ponadto bardzo ważnym aspektem, który należy podkreślić, jest to, że w tym wyrażeniunie należy przedstawiać ani składników stałych, ani czystych cieczy., ponieważ w tym wyrażeniu biorą udział tylko sprawy, które mogą ulegać zmianom. Stężenie ilości materii substancji w stanie stałym jest stałe i dlatego jest już zawarte w samej wartości K.do. To samo dotyczy czystych płynów, takich jak woda. W skrócie, w ekspresji biorą udział tylko substancje w stanie gazowym iw roztworze wodnym.
Teraz nie przestawaj... Po reklamie jest więcej ;)
Zwróć uwagę na poniższe przykłady:
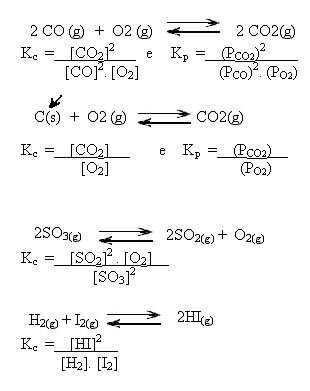
Wartości Kdo może nam pokazać, czy stężenie reagentów i produktów jest takie samo, czy też jedno jest większe od drugiego:
- gdyby Kdo lub KP jest równy jeden (Kdo = 1)oznacza to, że stężenie reagentów i produktów jest równe;
- jeśli wartość Kdo lub KP być wysokim, oznacza to, że produkty są w większej koncentracji, ponieważ w wyrażeniu Kdo produkty są w liczniku;
- jeśli wartość Kdo lub KP jest niski, oznacza to, że odczynniki są w wyższym stężeniu, ponieważ w wyrażeniu Kdo odczynniki są w mianowniku.
*Kdo i KP są to liczby bezwymiarowe, to znaczy czyste liczby, bez jednostki związanej z jakąkolwiek wielkością lub relacją między wielkościami.
Jennifer Fogaça
Absolwent chemii
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
FOGAÇA, Jennifer Rocha Vargas. „Stałe równowagi Kc i Kp”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm. Dostęp 28 czerwca 2021 r.

