Aldehyd jest to funkcja organiczna, której główną cechą jest obecność grupa karbonylowa (C=O)na krawędzi łańcucha węglowego. Poniżej znajduje się reprezentacja karbonylu na końcu łańcucha:
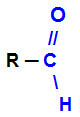
Karbonyl na końcu łańcucha wskazujący funkcję organiczną aldehydu
Ilekroć karbonyl znajduje się na końcu łańcucha węglowego, będzie miał bezpośrednio do niego przyłączony atom wodoru. Grupa R przyłączona do węgla może być wodorem lub dowolną rodnik. Zatem najmniejszy istniejący aldehyd ma tylko jeden atom węgla:
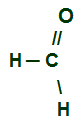
Wzór strukturalny najmniejszego aldehydu
Istnieje również możliwość, że aldehyd ma więcej niż jeden karbonyl w łańcuchu:
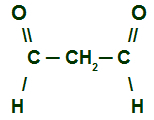
Wzór strukturalny aldehydu, który ma dwa karbonylki
Spotkajmy się teraz nazewnictwo, charakterystyka i zastosowania aldehydów:
a) Nomenklatura IUPAC
TEN zasada nomenklatura ustanowiona przez IUPAC dla aldehydu é:
Przedrostek (oznaczający liczbę węgli) + wpisać rodzaj wiązań + al
zagryźć kilka przykładów zastosowań zasady nazewnictwa dla aldehyd:
Przykład 1: Propanal
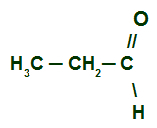
Propanal wzór strukturalny
Mamy aldehyd z łańcuch nasycony (tylko wiązania pojedyncze) i normalny (bez rozgałęzień). Tak więc, aby to nazwać, po prostu postępuj zgodnie z sekwencją prefiksu, infiksu i sufiksu (al). On prezentuje trzy węgle(prefiks prop) i proste linki (infix). Jego imię to zatem:
Propanal
Przykład 2: 2-metylobutanal
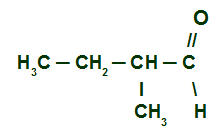
Wzór strukturalny 2-metylobutanalu
tutaj mamy aldehyd rozgałęziony i nasycony (tylko wiązania pojedyncze), więc musimy zlokalizować łańcuch główny, który musi mieć węgiel karbonylowy i największą liczbę węgli. Główny łańcuch to pozioma sekwencja węgli. W końcu, numerujemy łańcuch od węgla karbonylowego:
Teraz nie przestawaj... Po reklamie jest więcej ;)
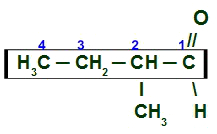
Numeracja głównego łańcucha 2-metylobutanalu
Aby nazwać ten aldehyd, bierzemy pod uwagę, że na węglu 2, mamy obecność rodnikmetyl (CH3-) i że główny łańcuch ma cztery węgle (przedrostek ale) i tylko proste połączenia (wrostek an). Jego imię to zatem:
2-metylobutanal
Przykład 3: 3-etyloheks-4-enal
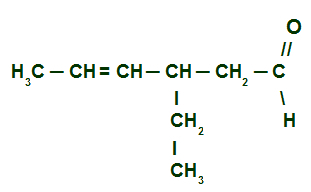
Wzór strukturalny 3-etyloheks-4-enalu
tutaj mamy aldehyd rozgałęziony i nienasycony (ma podwójne wiązanie), więc musimy zlokalizować łańcuch główny, który musi mieć węgiel z karbonylu i węgle z podwójnego. Głównym łańcuchem w tym przypadku będzie pozioma sekwencja węgli. W końcu, numerujemy łańcuch od węgla karbonylowego:
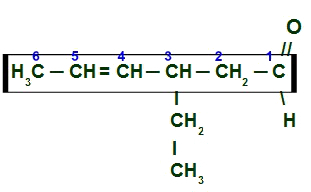
Numeracja głównego łańcucha 3-etyloheks-4-enalu
Aby nazwać ten aldehyd, bierzemy pod uwagę, że na węglu 3, mamy obecność radykała etyl (CH3-CH2) i że główny łańcuch prezentuje sześć węgli (przedrostek hex) i jedno podwójne wiązanie (przedrostek o), znajduje się na węglu 4. Jego imię to zatem:
3-etyloheks-4-enal
b) Charakterystyka aldehydów
W Główne cechy aldehydów to:
Są to niezwykle reaktywne substancje;
Mają mniejszą gęstość niż woda;
Stan fizyczny (stały, ciekły lub gazowy) zależy od ilości węgla w aldehydzie. Na przykład aldehydy, które mają do dwóch atomów węgla, są gazami;
Większość z nich ma przyjemne zapachy;
Jego cząsteczki są polarne;
Charakteryzują się łatwą palnością (łatwo się palą).
c) Zastosowania aldehydów
Produkcja perfum
Produkcja tworzyw sztucznych
Przemysł farmaceutyczny
Przemysł spożywczy
Jako rozpuszczalnik przemysłowy
Produkcja luster
Produkcja środków dezynfekujących
produkcja żywicy
Produkcja środków owadobójczych
Przeze mnie Diogo Lopes Dias
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
DNI, Diogo Lopes. „Co to jest aldehyd?”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-aldeido.htm. Dostęp 28 czerwca 2021 r.
Chemia

Aldehydy, związki karbonylowe, grupa karbonylowa, główne aldehydy, etanol, surowiec w przemyśle pestycydów i leków, metalal, formaldehyd, przemysł tworzyw sztucznych i żywic.


