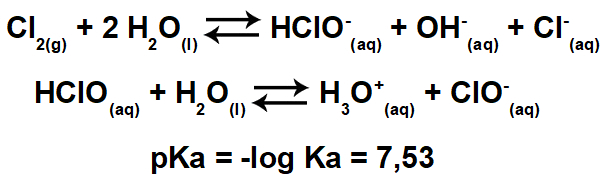Ilość kalorii zależy od składu pokarmu. Tak więc, aby eksperymentalnie określić ilość ciepła uwalnianego przez żywność i jaka może zostać wchłonięta przez organizm, używamy urządzenia o nazwie kalorymetr.
To urządzenie mierzy ciepło uwalniane przez żywność podczas jej spalania. Istnieje kilka rodzajów kalorymetrów; pierwszy z nich został stworzony w 1780 roku przez Lavoisiera i Laplace'a i był kalorymetr lodowy.
Obecnie najczęściej używanym i uwzględniającym opisaną powyżej koncepcję kalorii jest kalorymetr wodny. To urządzenie jest pokryte materiałem izolacyjnym, aby zapobiec utracie ciepła z medium; a żywność do analizy jest umieszczana w placed Komora spalania, który zawiera gazowy tlen i elektrody. Elektrody te ulegają wyładowaniu elektrycznemu i powodują ich zapłon i spalanie żywności.
Znana masa wody zawarta w kalorymetrze pochłania ciepło wydzielane przez przypaloną żywność i a termometr mierzy wzrost temperatury wody. Ponadto kalorymetr zawiera mieszadło co pozwala na utrzymanie jednolitej temperatury wody przez cały czas.
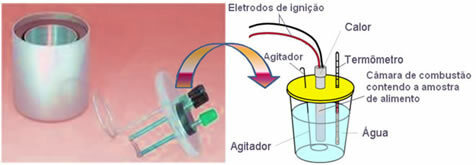
Jeśli więc użyjemy np. masy 1 grama cukru, a kalorymetr ma 1000 g wody i zaobserwujemy, że w końcu reakcji temperatura wody wzrosła z 20°C do 24°C, czyli wzrosła o 4°C, możemy wtedy osiągnąć wartość energetyczną cukier. Lubić? Cóż, biorąc pod uwagę początkową koncepcję kalorii, mamy:
| Podnieś z 1°C → 1 cal na gram wody |
| Podnieś z 4°C → 4 kcal na gram wody |
Tak więc 1 g wody pochłania 4 wapno. Zużyto jednak 1000 g wody i biorąc pod uwagę, że całe ciepło uwolnione podczas spalania zostało przez nią pochłonięte, całkowita energia pochłonięta przez wodę wyniosła 4000 cal lub 4 kcal. Dlatego stwierdzamy, że:
Teraz nie przestawaj... Po reklamie jest więcej ;)
| Wartość energetyczna cukru = 4000 cal/g lub 4 kcal/g. |
Przekształcenie do SI:
1 kcal 4,18 kJ
4 kcal/g x
x = 16,72 kJ/g
Dodatkowo możemy użyć następującego równania do obliczenia ilości ciepła oddanego lub pochłoniętego przez wodę:
| Q = m. do. t |
Gdzie:
Q = ciepło oddawane lub pochłaniane przez wodę;
m = masa wody;
c = ciepło właściwe wody, które wynosi 1,0 cal/g. °C lub 4,18 J/g. °C;
Δt = zmienność temperatury, jakiej doznaje woda, wyrażona spadkiem temperatury końcowej o temperaturę początkową (tfa – tja).
Używając tej formuły otrzymujemy ten sam wynik:
Q = m. do. t
Q = 1000g. 1,0 kcal/g. °C. (24-20)°C
Q=4000 kcal
Q = 4,0 kcal
lub
Q = m. do. t
Q = 1000g. 4,18 kJ/g. °C. (24-20)°C
Q= 16,72 kJ
Jennifer Fogaça
Absolwent chemii
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
FOGAÇA, Jennifer Rocha Vargas. „Pomiar kalorii w żywności za pomocą kalorymetru”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/medindo-as-calorias-dos-alimentos-por-meio-um-calorimetro.htm. Dostęp 27 czerwca 2021 r.