TEN energia aktywacji jest to minimalna ilość energii niezbędna do zajścia zderzenia cząstek reagentów w korzystnej orientacji i wywołania reakcji.
Reakcje zachodzą tylko wtedy, gdy reagenty mają energię aktywacji (lub minimalną potrzebną energię, która zmienia się w zależności od reakcji; w ilości lub formie) lub gdy jest im dostarczany.
Na przykład, gdy metaliczny sód wchodzi w kontakt z wodą, reaguje gwałtownie. Oznacza to, że zawartość energetyczna tych reagentów jest już wystarczająca do zajścia reakcji.
W przypadku włączenia kuchenki reakcja spalania nastąpi tylko wtedy, gdy w pobliżu gazu, który uwalnia się z kuchenki, postawimy zapaloną zapałkę lub inne źródło ognia. Oznacza to, że w tym przypadku konieczne było dostarczenie energii do układu tak, aby osiągnął energię aktywacji i nastąpiła reakcja.
W przypadku samego luminoforu, do jego spalenia, energię aktywacji zapewnia tarcie. To samo dzieje się z zapalniczkami, które również potrzebują iskry dającej niezbędną energię aktywacji do spalania zawartego w nich gazu.
Energia aktywacji może być również dostarczana przez światło, jak ma to miejsce w przypadku rozkładu nadtlenku wodoru. Dlatego jest przechowywany w ciemnych lub nieprzezroczystych butelkach.
Teraz nie przestawaj... Po reklamie jest więcej ;)

Możemy zatem stwierdzić, że energia aktywacji (Eaż do) jest różnicą między energią potrzebną do rozpoczęcia reakcji (E) a energią zawartą w substratach (Epr):

Energia aktywacji jest przeszkodą w zajściu reakcji i jest potrzebna do zerwania wiązań reagentów. Dzięki temu zachodzi reakcja i powstają nowe połączenia w celu utworzenia produktów.
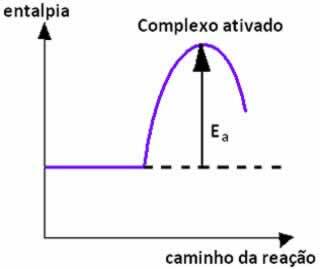
Gdy zderzenie cząstek reagentów o korzystnej orientacji zachodzi z równą energią lub wyższa niż energia aktywacji, przed powstaniem produktów powstaje stan pośredni i niestabilny, denominowany aktywowany kompleks, w którym wiązania reagujące są osłabione i powstają wiązania produktowe. A zatem, energia aktywacji to energia potrzebna do utworzenia aktywowanego kompleksu.
Poniżej mamy wykres, który pokazuje energię aktywacji jako barierę dla zajścia reakcji:
Jennifer Fogaça
Absolwent chemii
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
FOGAÇA, Jennifer Rocha Vargas. „Energia aktywacji”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/energia-ativacao.htm. Dostęp 27 czerwca 2021 r.