TEN stężenie w ilości materii to relacja między ilością materii w solute, mierzone w molach (n1) i objętość rozwiązanie w litrach (V). To stężenie jest mierzone w molach na litr (mol/L).
Rozważmy sok żołądkowy, który wytwarza nasz żołądek w celu przeprowadzenia procesu trawienia. W rzeczywistości jest to roztwór kwasu solnego (HCl) o stężeniu 0,01 mol/L. Oznacza to, że na każdy litr soku żołądkowego przypada 0,01 mola HCl.
TEN stężenie w ilości materii Niektórzy autorzy często nazywają to stężeniem molowym lub molarnością, ale poprawne terminy to „stężenie w mol/L” lub „stężenie w ilości materii”. Ponadto stężenie to jest najbardziej zalecane przez Międzynarodowy Układ Jednostek Jednostek (SI) oraz Międzynarodową Unię Chemii Czystej i Stosowanej (IUPAC); dlatego jest najczęściej stosowany w laboratoriach i przemyśle chemicznym.
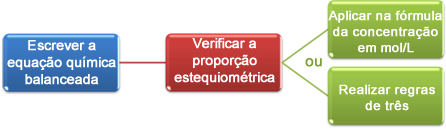
Mapa myśli: Jednostka koncentracji w Mol/L

* Aby pobrać mapę myśli w formacie PDF, Kliknij tutaj!
Formuły stosowane w molarności
Wzór matematyczny używany do obliczenia tego stężenia jest określony wzorem:

W wielu przypadkach nie podaje się wartości ilości materii w substancji rozpuszczonej, ale jej masę wyrażoną w gramach (m1). W takich przypadkach mamy, że ilość materii w substancji rozpuszczonej w molach (n1) można osiągnąć dzieląc masę substancji rozpuszczonej przez masę molową samej substancji rozpuszczonej, zgodnie z następującym wzorem:
Teraz nie przestawaj... Po reklamie jest więcej ;)

Wymiana n1 w równaniu mamy:

Przykład obliczenia molarności
Rozważ następujący przykład, aby zobaczyć, jak wykonuje się to obliczenie:
“100 ml roztworu wodnego zawiera 20 g NaCl. Jak postępować, aby wyrazić stężenie tego roztworu w ilości materii na objętość?”
Rozkład:
Cóż, wzór, który należy zastosować, jest taki sam, jak pokazano powyżej, ale objętość nie jest w litrach. Musimy więc wykonać następującą konwersję jednostek:
1 l 1000 ml
V 100 ml
V = 0,1 l
Konieczne jest również ustalenie wartości masy molowej soli NaCl. Aby to zrobić, konieczne jest poznanie wartości mas atomowych obu pierwiastków i wykonać obliczenia mas molowych, o których mowa w tekście “Masa molowa i liczba molowa”:
M (NaCl) = 1. 23 + 1. 35, 46
M (NaCl) = 58,46 g/mol
Teraz możemy podmienić wszystkie wartości we wzorze i znaleźć wartość stężenia w mol/L:
m = Nie1
M1.V
M = 20
58,46.0,1
M = 3,4 mo/L
*Mapa mentalna mojego autorstwa Diogo Lopes
Jennifer Fogaça
Absolwent chemii
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
FOGAÇA, Jennifer Rocha Vargas. „Stężenie w mol/l lub molarności”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/concentracao-mol-l-ou-molaridade.htm. Dostęp 27 czerwca 2021 r.