Rozważ następującą równowagę chemiczną w stałej temperaturze:
3 godziny2(g) + N2(g) ↔ 2 NH3(g)
Według Gay-Lussaca proporcja objętości gazowych uczestników reakcji jest równa stosunkowi odpowiednich współczynników stechiometrycznych. W uproszczeniu możemy powiedzieć, że liczba cząsteczek obecnych w substratach i produktach jest równa współczynnikom w równaniu.
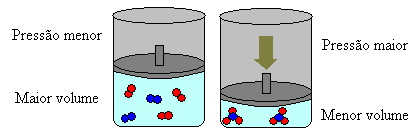
W powyższym przypadku w odczynnikach mamy 4 cząsteczki, a w produktach 2 cząsteczki, co oznacza, że objętość odczynników jest większa, a produktów mniejsza.
Jeśli zwiększymy ciśnienie w tym systemie, równowaga przesunie się w kierunku mniejszej objętości, aby zmniejszyć to ciśnienie. W przypadku rozważanej reakcji przemieszczenie będzie przebiegało w kierunku tworzenia się produktu (NH3(g)).
Jeśli jednak zmniejszymy ciśnienie, reakcja posunie się w kierunku największej objętości, czyli przeciwnego kierunku powstawania reagentów (3 H2(g) + N2(g)).
Teraz nie przestawaj... Po reklamie jest więcej ;)
Dzieje się tak zgodnie z zasadą Le Chateliera, która mówi, że wszelkie zakłócenia (takie jak zmniejszenie lub zwiększenie ciśnienia) powodowały w układzie w równowadze sprawi, że porusza się on w kierunku, który minimalizuje to zakłócenie, dostosowując się do nowego saldo.
Krótko mówiąc, w przypadku wpływu zmian ciśnienia na równowagę chemiczną możemy powiedzieć:
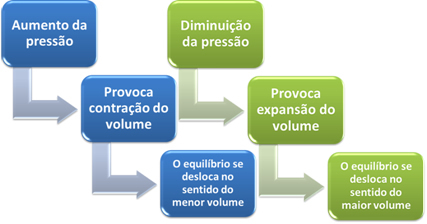
W przypadku reakcji, w których objętość reagentów jest równa objętości produktów, równowaga chemiczna nie ulega zmianie.
Jennifer Fogaça
Absolwent chemii
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
FOGAÇA, Jennifer Rocha Vargas. „Zmienność ciśnienia i przemieszczenie równowagi chemicznej”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/variacao-pressao-deslocamento-equilibrio-quimico.htm. Dostęp 28 czerwca 2021 r.
Chemia

Sprawdź swoją wiedzę i dowiedz się więcej dzięki tej liście rozwiązanych ćwiczeń dotyczących bilansów chemicznych. Dzięki temu materiałowi będziesz w stanie lepiej zrozumieć, jak pracować ze stałymi równowagi (Kp, Kc i Ki), przesunięciem równowagi, pH i pOH, a także równowagą w tak zwanych roztworach buforowych.



