Otacza nas sprzęt, który do funkcjonowania potrzebuje ogniw lub baterii. Jednak wiele z tych przenośnych urządzeń staje się coraz mniejszych, a wraz z tym pojawia się ogromne zapotrzebowanie na miniaturowe baterie.
Przykładem tego typu baterii jest bateria rtęciowa lub zwana również stos rtęciowo-cynkowy.
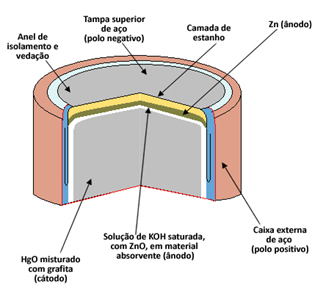
Każde ogniwo składa się z dwóch elektrod, anody (biegun ujemny) i katody (biegun dodatni) oraz elektrolitu. W przypadku ogniwa rtęciowego anoda składa się z kapsułki cynk metaliczny (Zn(y)) to jest katoda za tlenek rtęci II (HgO(y)). Zarówno Zn, jak i HgO są mielone na proszek i zagęszczane, aby stos był jak najmniejszy. O elektrolit jest wykonany z roztworu nasycony wodorotlenek potasu (KOH(tutaj)).
Zn utlenia się, oddając swoje elektrony HgO, jak pokazano w poniższych półreakcjach i reakcji globalnej tego ogniwa:
Połowa reakcji anody: Zn(y) + 2 OH1-(tutaj) → ZnO(y) + 2 godz2O(1) + 2e-
Półreakcja katodowa: HgO(y) + H2O(1) + 2e- → Hg(1) + 2 OH1-(Theq)
Reakcja globalna: HgO(y) + Zn(y) → ZnO(y) + Hg(1)
Teraz nie przestawaj... Po reklamie jest więcej ;)
Ogniwa rtęciowe są stosowane w zegarkach cyfrowych, zegarkach na rękę, aparatach fotograficznych, kalkulatorach, organizerach elektronicznych, aparaty słuchowe i inne przenośne urządzenia elektryczne, które wymagają wydajnej pracy i trwałości, ponieważ te baterie mają napięcie 1,35V.

Niestety niewłaściwa utylizacja tych baterii może stanowić poważne zagrożenie dla środowiska, ponieważ zawierają one rtęć, która jest metalem ciężkim. Rtęć może skazić glebę, wody gruntowe, wody w jeziorach i rzekach, docierając do zwierząt i ludzi. Jest toksyczny nawet w niewielkich ilościach. Wśród problemów zdrowotnych, jakie może powodować rtęć, znajdują się: uszkodzenie błon śluzowych, skóry, nerek, gwałtowne nudności, wymioty, bóle brzucha, krwawa biegunka, które mogą prowadzić do śmierci.
Aby dowiedzieć się więcej o tym, dlaczego baterie są odpadami toksycznymi, w jaki sposób rtęć jest zanieczyszczona i co powinniśmy zrobić ze zużytymi bateriami, przeczytaj teksty cytowane poniżej.
Jennifer Fogaça
Absolwent chemii
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
FOGAÇA, Jennifer Rocha Vargas. „Baterie rtęciowe”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/pilhas-mercurio.htm. Dostęp 28 czerwca 2021 r.
Chemia

Zagrożenie przez baterie, zanieczyszczenie metalami ciężkimi, sprzęt AGD i RTV, akumulatory, Skład chemiczny baterii niklowo-kadmowych, prawidłowa utylizacja baterii do telefonów komórkowych, globalna objętość baterie



