ty aldehydy i ketony są to bardzo podobne funkcje organiczne. Oba mają w swojej strukturze karbonylową grupę funkcyjną (C = O), z tą tylko różnicą, że w przypadku aldehydy, zawsze pojawia się na końcu łańcucha węglowego, to znaczy jednym z ligandów węgla karbonylowego jest wodór; ketony mają karbonyl pomiędzy dwoma innymi atomami węgla.
Aldehydowa grupa funkcyjna:Grupa funkcjonalna ketonów:
O O
║ ║
C C ─ H C C ─ C
Z tego powodu zdarzają się przypadki funkcjonalnej izomerii między aldehydami i ketonami. Na przykład poniżej przedstawiamy dwa funkcjonalne izomery, które mają ten sam wzór cząsteczkowy (C3H6O), ale jeden to aldehyd (propanal), a drugi to keton (propanon). Zobacz, jak całkowicie zmienia to ich właściwości i zastosowanie:
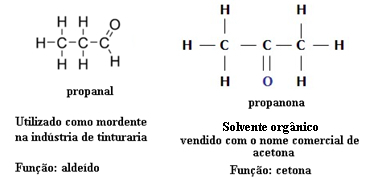
Przykład izomerii funkcji między aldehydem a ketonem
Wyobraź sobie, że jesteś w laboratorium i znajdujesz fiolkę z bezbarwną cieczą, która ma tylko wzór cząsteczkowy C3H6O. Co byś zrobił, aby dowiedzieć się, czy to keton czy aldehyd?
Aby rozwiązać takie problemy,
istnieją metody różnicowania aldehydów i ketonów na podstawie reakcji tych związków ze słabymi czynnikami utleniającymi. Jak pokazano niżej, w kontakcie ze słabymi utleniaczami aldehydy reagują utlenianiem, podczas gdy ketony nie reagują. Mówimy, żealdehydy działają jako reduktory, ale ketony nie, reagują jedynie jako środki redukujące w kontakcie z utleniaczami energetycznymi.Aldehydy + słabe utleniacze → kwas karboksylowy
O O
║ ║
C ─ C ─ H + [O] → C ─ C ─ OH
Ketony + Słabe utleniacze → Nie reaguj
O
║
C ─ C ─ C + [O] → Brak reakcji
Na tej podstawie wystarczy przeprowadzić tę reakcję i sprawdzić, czy związek reaguje, czy nie. Jeśli zareaguje, wiemy, że to aldehyd; jeśli nie reaguje, to jest keton.
Ponadto produkty powstałe w tych reakcjach utleniania aldehydów są dość widoczne, z zachodzącymi zmianami koloru, co zostanie pokazane później.
Istnieją trzy główne metody różnicowania aldehydów i ketonów, którymi są:
1- Tollens reaktywne: Ten odczynnik jest amoniakalny roztwór azotanu srebra, czyli zawiera azotan srebra (AgNO3) i nadmiar wodorotlenku amonu (NH4O):
AgNO3 + 3 NH4OH → Ag (NH3)O + NH4NA3 + 2 godz2O
Tollens Reactive (nazwany na cześć niemieckiego chemika Bernharda Tollensa (1841-1918))
Jak wyjaśniono w tekście Tworzenie srebrnego lustra, gdy aldehyd wchodzi w kontakt z reaktywnym Tollensem, utlenia się do odpowiedniego kwasu karboksylowego, podczas gdy jony srebra są redukowane do Ag0 (srebrny metalik). Jeśli ta reakcja jest przeprowadzana na przykład w probówce, to metaliczne srebro osadza się na ściankach probówki, powodując powstanie filmu zwanego srebrne lustro. Ten obserwowany wynik jest bardzo piękny i jest wykorzystywany w procesie produkcji luster przemysłowych.
Zachodzącą reakcję można przedstawić w następujący sposób:
O O
║ ║
R ─ C ─ H + H2O → R ─ C ─ OH + 2e- + 2 H+
2 Ag+ + 2e- → 2 Ag0
2 NH3 + 2 godz+ → 2 NH4+
O O
║║
R C ─ H + 2 Ag+ + 2 NH3 +H2O → R C ─ OH + 2 Ag0 + 2 NH4+
aldehyd Tollens reaktywnekwas karboksylowy srebrny metalik (srebrne lustro)
Z drugiej strony, jeśli wprowadzimy keton do reakcji z reaktywnym Tollensem, nie nastąpi tworzenie metalicznego srebra, ponieważ ketony nie mogą zredukować jonów Ag.+.
2- Fehling Reaktywne: Ta reaktywna jest niebieskim roztworem siarczanu miedzi II (CuSO4) w środowisku zasadowym, ponieważ miesza się go z innym roztworem utworzonym przez wodorotlenek sodu (NaOH) oraz winian sodu i potasu (NaOOC-CHOH-CHOH-COOK). Do roztworu siarczanu miedzi II dodaje się winian, aby go ustabilizować i zapobiec jego wytrącaniu.
CUSO4 + 2 NaOH → Na2TYLKO4 + Cu(OH)2
Fehling Reactive (nazwany na cześć niemieckiego chemika Hermanna von Fehlinga (1812-1885))
W kontakcie z reaktywną Fehlinga aldehyd tworzy kwas karboksylowy poprzez jego utlenianie, podczas gdy jony miedzi (Cu)2+) obecne w środku ulegają redukcji, tworząc czerwonobrązowy osad (bardziej ceglasty), który jest tlenkiem miedzi. Ketony natomiast nie reagują - ponieważ nie mogą redukować jonów Cu2+.
O O
║ ║
R ─ C ─ H + 2 Cu(OH)2 → R ─ C ─ OH + Tyłek2O + 2 godz2O
aldehyd czerwonawo-brązowy osad
3- Reaktywny Benedykta: Ta reaktywna jest również tworzona przez roztwór siarczanu miedzi II (Cu (OH)2) w podstawowym podłożu, ale miesza się go z cytrynianem sodu.
Podobnie jak w przypadku odczynnika Fehlinga, w przypadku reakcji aldehydu z odczynnikiem Benedicta, występują również jony miedzi (Cu2+) obecne w środowisku, które są zredukowane i tworzą czerwony tlenek miedziawy.
Odczynnik ten jest szeroko stosowany w testach wykrywających obecność i zawartość glukozy w moczu. Glukoza ma w swojej strukturze grupę aldehydową, więc reaguje z odczynnikiem Benedicta obecnym w paskach do tych testów. Następnie porównaj kolor wstążki z kolorem skali na opakowaniu produktu.

Odczynnik Benedicta służy do oznaczania zawartości glukozy w moczu.
Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/diferenciacao-aldeidos-cetonas.htm
