Amerikansk kjemiker Gilbert N. Lewis (1875-1946) foreslo oktettregelen, som sier:
"Atomer med forskjellige grunnstoffer etablerer kjemiske bindinger, donerer, mottar eller deler elektroner, for å tilegne seg den elektroniske konfigurasjonen av edelgass, det vil si med 8 elektroner i det siste skallet (eller med 2 elektroner når det gjelder de atomene som bare har ett elektronskall, slik det skjer med hydrogen). "
I 1916 foreslo Lewis at for å forbli stabil, nå oktetten eller duetten, elementene som utgjør molekylære stoffer utføre en deling av par elektroner. Disse stoffene dannes bare av atomer av hydrogen, ikke-metaller og halvmetaller, alt sammen med tendens til å motta elektroner. Derfor er det ingen måte for noen av dem å donere noe elektron (som skjer med metaller i ioniske bindinger), men alle trenger å motta, så de deler elektronene sine gjennom en kovalent binding eller molekylær.
Dermed foreslo Gilbert Lewis en måte å representere den kovalente eller molekylære bindingen, som ble kjent som
Lewis formel. Hun blir også kalt elektronisk formel eller ennå, Lewis 'elektroniske formel, fordi hovedkarakteristikken er at den viser elektronene i valensskallet til hvert atom og dannelsen av elektroniske par.Hvert elektron er representert med en prikk., som omgir symbolet for det tilsvarende kjemiske elementet. Bare valensskallelektronene er rundt elementet.
Som vist i tabellen nedenfor, for å kjenne til mengden elektroner i valensskallet, bare kjenn den periodiske tabellfamilien:

I Lewis-formelen, hvert delte elektronpar representerer en kjemisk (kovalent) binding, hvor elektronene møtes i det området av elektrosfæren som er felles for hvert par atomer som er sammenføyd. Derfor, i representasjonen, er de plassert side om side.
La oss for eksempel finne ut hva Lewis-formelen er for hydrogengass, hvis molekylære formel er: H2.
Hvert hydrogenatom har bare ett elektron i valensskallet, da dette elementet tilhører familie 1 i det periodiske systemet. Hver trenger å motta ett elektron til, for å være stabilt, med to elektroner i K-elektronskallet. Så de deler elektronene sine og begge får to. Se:
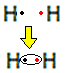
Dette er Lewis-formelen for hydrogengassmolekylet.
Oksygen har seks elektroner i elektronskallet, så hver trenger å motta to elektroner til for å være stabile, med åtte elektroner. Derfor er Lewis-formelen for oksygengassmolekylet:

Se at det er to lenker, ettersom det er to delte par.
Se andre eksempler på elektroniske formler av molekylære stoffer nedenfor:
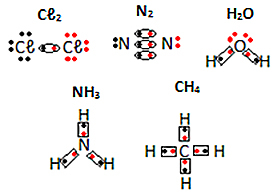
Av Jennifer Fogaça
Uteksamen i kjemi
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/formula-eletronica-lewis.htm
