På organiske eliminasjonsreaksjoner er de atomer eller grupper av atomer i et molekyl blir fjernet eller eliminert fra det, skape en ny organisk forbindelse, i tillegg til en uorganisk forbindelse som dannes av den delen som var slettet.
En type eliminasjonsreaksjon er dehydrering, hvor molekylet som går tapt er vann. Dehydrering av alkoholer (forbindelser som har OH-gruppen bundet til et mettet karbon i en åpen kjede) kan finne sted på to måter: intramolekylær og intermolekylær.
"Intra" betyr "inni", derfor intramolekylær dehydrering av alkoholer oppstår når et vannmolekyl går ut fra "innsiden" av selve alkoholmolekylet. I dette tilfellet vil det dannede organiske produktet være et alken.
Denne reaksjonen foregår bare i nærvær av en katalysator som fungerer som et tørkemiddel, og mesteparten av tiden er det konsentrert svovelsyre (H2KUN4) og temperaturen skal være rundt 170 ° C.
Eksempel:
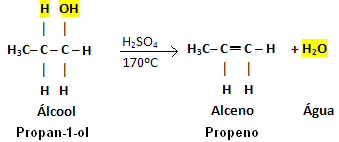
Merk at OH-gruppen forlot og hydrogen forlot det nærliggende karbonet, noe som ga vann. Videre ble dobbeltbindingen som ga opphav til alkenen opprettet.
Anlegget for å bli dehydrert følger følgende fallende rekkefølge:
Tertiære alkoholer> Sekundære alkoholer> Primære alkoholer
Men hva med når OH-gruppen kommer midt i karbonkjeden? Hydrogenatomet som nærliggende karbonatom vil frigjøres fra og danner vannmolekylet?
For eksempel er neste 2-metylpentan-3-ol. Merk at det ene nærliggende karbonatomet er tertiært (uthevet i rødt), mens det andre er sekundært (uthevet i blått):
H OH H
│ │ │
H3C─ Ç ─ Ç ─ Ç ─ CH3
│ │ │
H H CH3
Hydrogenet bundet til det tertiære karbonatomet vil være lettere å forlate, fordi dets elektronegative karakter er lik δ+1Dermed jo mindre negativ karbonkarakteren er, jo svakere er båndet mellom dem og jo lettere blir det å bryte båndet.
I tilfeller som dette dannes alle mulige forbindelser, men overvekt vil bli gitt i rekkefølgen: Tertiære alkoholer> Sekundære alkoholer> Primære alkoholer.
Så vi har:
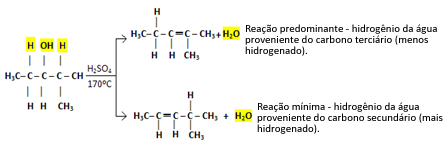
Denne typen reaksjon adlyder Saytzefs styre, som sier det det vil være en større tendens for at hydrogen etterlater karbon mindre hydrogenert. Denne regelen er nøyaktig det motsatte av Markovnikovs regel brukes til tilleggsreaksjoner.
For å utfylle din kunnskap om dette emnet, les også teksten "Intermolekylær dehydrering av alkoholer”.
Av Jennifer Fogaça
Uteksamen i kjemi
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/desidratacao-intramolecular-dos-Alcoois.htm

