Du estere er oksygenerte organiske forbindelser som dannes ved den kjemiske reaksjonen mellom a karboksylsyre det er en alkohol. Presentere den funksjonelle gruppen (sammensatt av to oksygenatomer og to radikale R) representert nedenfor:
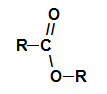
Generell funksjonell gruppe av en ester
Strukturelt, hva som kjennetegner ester det er tilstedeværelsen av noen alkylradikaler festet direkte til oksygenatomet. I dette tilfellet kan radikalen (R) festet til karbon - som i sin tur er dobbelt bundet til oksygen - være enten et alkylradikal eller et hydrogenatom.
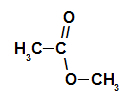
Kullkjede av en ester
forestringsreaksjon
det handler om kjemisk reaksjon som stammer fra en ester og et vannmolekyl fra samspillet mellom en karboksylsyre og en hvilken som helst alkohol, som i ligningen nedenfor:
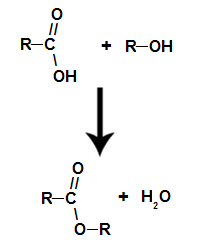
Kjemisk ligning som representerer dannelsen av en ester
Under forestring samhandler hydroksylgruppen (OH) av alkoholen med alkoholen hydrogen (H) ioniserbar fra hydroksylen av syren og danner vannmolekyl.
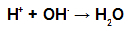
Vannmolekyledannende grupper i forestring
allerede den ester den dannes ved å binde alkoholen (R) til alkoholen med oksygen, som blir til overs fra hydroksylen av syren etter dannelsen av vann.
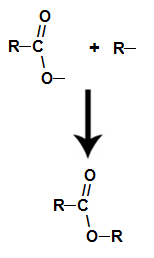
Dannelse av estermolekylet
Kjennetegn ved estere
Viktigste fysiske egenskaper presentert av estere:
De har frukt- og blomsteraromaer;
lave estere molær masse de er flytende ved romtemperatur og de med høy molar masse er faste;
Sammenlignet med alkoholer og karboksylsyrer, har estere lavere smelte- og kokepunkter;
Sammenlignet med vann er estere med lavere molare masse mindre tette;
Estere med lavere molær masse er polare og de høyere molare ikke-polare;
I polare estere dominerer krefter permanent dipol; i det ikke-polære dominerer kreftene indusert dipol;
Estere med lavere molær masse er lite oppløselige i vann og de med større masse er uoppløselige i vann.
En Ester Naming Rule
Før du bruker navneregelen til a ester, er det viktig å huske at denne forbindelsen er dannet av foreningen av to deler, den ene kommer fra av karboksylsyre (i rødt) og den andre av alkohol (i blått), som representert av bilde a Følg:
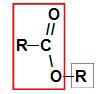
Identifikasjon av delene som stammer fra esteren
I følge International Union of Pure and Applied Chemistry (IUPAC), er den offisielle regelen for å navngi en ester:
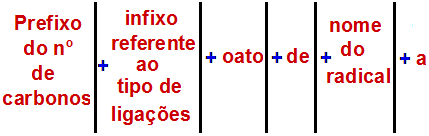
En Ester Naming Rule
Merk: Prefikset og infikset tilsvarer alltid karboksylsyredelen, og radikalet tilsvarer alkoholdelen.
Se nedenfor noen eksempler på anvendelse av navneregelen for estere:
Første eksempel: bringebæressens
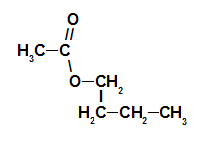
Strukturformel av bringebæressensesteren
For å navngi denne esteren bruker vi:
Nei prefiksO karbon: et, da den dannende syren har to karbonatomer;
Informasjon om typen lenker: en, da den dannende syren bare har enkeltbindinger mellom karbonatomer;
handlingen;
i;
Radikal: butyl, for å ha fire karbonatomer i rekkefølge;
De.
Dermed er navnet på esteren som tilsvarer bringebæressensen butyletanoat.
Andre eksempel: furu kjegle essens
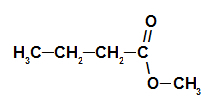
Strukturformel av furuskegleesteren
For å danne navnet på denne esteren bruker vi:
Nei prefiksO karbon: men, siden dannelse av syre har fire karbonatomer;
Informasjon om typen lenker: en, da den dannende syren bare har enkeltbindinger mellom karbonatomer;
handlingen;
i;
Radikal: metyl, ettersom den dannende alkoholen bare har ett karbon;
De.
Dermed er navnet på esteren som tilsvarer furu kjegle essensen metylbutanoat.
3. eksempel: jordbæressens
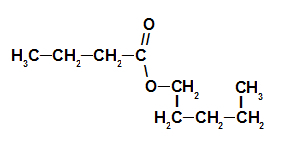
Strawberry Essence Ester Structural Formula
For å navngi denne esteren bruker vi:
Nei prefiksO karbon: men, siden den dannende syren har fire karbonatomer;
Informasjon om typen lenker: en, da den dannende syren bare har enkeltbindinger mellom karbonatomer;
handlingen;
i;
Radikal: pentyl, da den dannende alkoholen har fem karbonatomer i rekkefølge;
De.
Dermed er navnet på esteren som tilsvarer jordbæressensen pentylbutanoat.
Bruk av estere
Estere er kjent for sin bruk som smaksstoffer i bearbeidet mat, det vil si stoffer som simulerer den karakteristiske smaken og aromaen til naturlig mat, for eksempel frukt. Dessuten, estrene brukes fortsatt til fremstilling av medisiner, kosmetikk, parfymer og voks.
Av meg. Diogo Lopes Dias
Kilde: Brasilskolen - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ester.htm