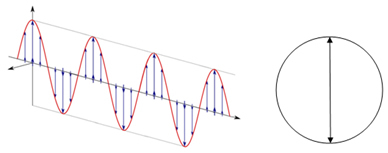
Hvorfor øker trykket på en gass når den komprimeres? Svaret på dette spørsmålet gjelder bevegelse av gassmolekyler i en lukket flaske, se:
Røde partikler: molekyler i gassform.
En nøye observasjon av illustrasjonen lar oss se at molekylene i et mindre rom er mer konsentrerte. Når du komprimerer en gass, begynner den å utøve et visst trykk på beholderens vegger. Den raske og kontinuerlige bevegelsen av molekyler som kolliderer med veggene er det som gjør fenomenet mulig.
Derfor, for å øke trykket til en gass, er det ikke nødvendig å øke temperaturen, bare senk volumet (komprimer gassen).
På den annen side, for en økning i gjennomsnittlig kinetisk energi (Ecin) er det nødvendig å fremme en endring i temperaturen på gassen.
Når vi varmer opp gassen inne i kolben, begynner de tilstedeværende molekylene å bevege seg med større hastighet, noe som fører til en økning i den gjennomsnittlige kinetiske energien. Vi sier da at Ecin er direkte proporsjonal med temperaturen, som vist i ligningen:
OGcin = KT
Gassen som følger denne ligningen regnes som en perfekt gass (eller ideell gass).
Av Líria Alves
Uteksamen i kjemi
Brasil skolelag
Se mer!
Gasser - lær mer om denne klassen av forbindelser.
Generell kjemi - Kjemi - Brasilskolen
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/teoria-cinetica-dos-gases.htm