Saken kan gjennomgå to hovedtyper av transformasjoner, fysiske og kjemiske. Fysisk transformasjon er når materiens natur ikke endres, det vil si dens sammensetning. For eksempel, når vi kappet et treverk, gjennomgikk det en transformasjon, men det var et fysisk fenomen, fordi det fremdeles er tre, dets konstitusjon er den samme som i begynnelsen.
På den andre siden, en kjemisk transformasjon eller et fenomen oppstår når stoffets natur eller sammensetning endres. I dette tilfellet er de første partiklene (som kan være molekyler, atomer, ioniske klynger, ioner, etc.) som demontert og atomene deres omorganiserer seg, og monterer nye molekyler, klynger, atomer, ioner etc., det vil si nye stoffer. Dette er en kjemisk reaksjon.
Tenk deg for eksempel at vi tar en tent fyrstikk nær etylalkohol. Vi vet hva som vil skje: alkoholen begynner å brenne. Dette betyr at den gjennomgår en kjemisk reaksjon med oksygen i luften (O2) og vil endre sammensetningen, ikke lenger være etanol (C2H6O), og oksygen vil heller ikke lenger ha sin opprinnelige sammensetning, med opprinnelse fra nye stoffer, som er karbondioksid (CO
2) og vann (H2O).
Alkohol i brann - forbrenningsreaksjon
I kjemiske reaksjoner kalles de første stoffene reagenser og slutten av Produkter, og reaksjonene er representert gjennom kjemiske ligninger, som følger følgende generelle struktur:
REAGENSER → PRODUKTER
Tatt i betraktning det forrige eksemplet på fullstendig forbrenningsreaksjon av alkohol (etanol), har vi følgende kjemiske ligning:
Etanol + oksygengass → karbondioksid + vann
Denne kjemiske reaksjonen er representert nedenfor ved hjelp av atomer i henhold til Dalton-modellen, i form av enkle sfærer:
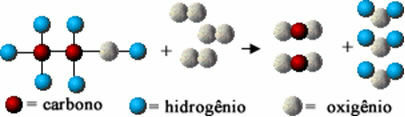
Modellrepresentasjon av en etanol forbrenningsreaksjon
Legg merke til at de opprinnelige bindingene mellom atomene ble brutt og de dannet nye bindinger, og nye stoffer dukket opp.
Dermed blir kjemiske ligninger skrevet med formler og symboler som best representerer ovenstående ordning. I det vurderte tilfellet (etanol forbrenningsreaksjon) har vi at den kjemiske ligningen uttrykkes som følger:
Ç2H5Åh(?) + 3 O2 (g) → 2 CO2 (g) + 3 H2O(v)
Det er noen visuelle faktorer som indikerer at det var en kjemisk reaksjon, som er:
* Gassutslipp;
* Fargeendring;
* Nedbør dannelse;
* Utseende av flamme eller lysstyrke.
Viktige prosesser som forekommer i kroppen vår, i naturen og i næringer, som produksjon av medisiner og industrialiserte matvarer, er kjemiske reaksjoner. Derfor er de ekstremt viktige for fremveksten og vedlikeholdet av livet.
Det er flere typer kjemiske reaksjoner, som kan klassifiseres i henhold til forskjellige kriterier, men hovedtyper studert i kjemi er:
1. Uorganiske reaksjoner: De klassifiseres vanligvis i henhold til antall dannede stoffer, antall reagenser og tilstedeværelsen eller fraværet av enkle og sammensatte stoffer. Det er fire hovedtyper av uorganiske reaksjoner:
1.1. Syntese eller tilleggsreaksjoner;
1.2. Nedbrytning eller analysereaksjon;
1.3. Enkel utveksling, forskyvning eller redoksreaksjon;
1.4. Dobbel utveksling eller metatesereaksjon;
2. Organiske reaksjoner: Dette er de som involverer karbonforbindelser. De er generelt klassifisert i tre hovedtyper:
2.1. Tilleggsreaksjoner;
2.2. Erstatningsreaksjoner;
2.3. Eliminasjonsreaksjoner.
Av Jennifer Fogaça
Uteksamen i kjemi
Kilde: Brasilskolen - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-reacao-quimica.htm
