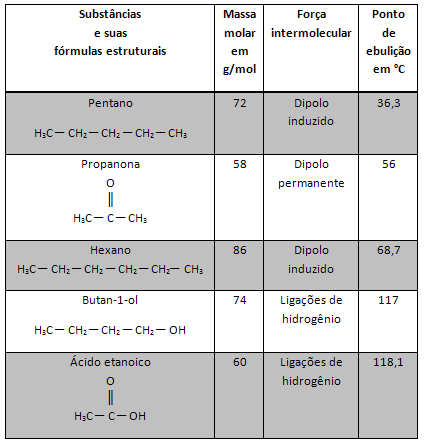
DE vanlig konsentrasjon, også kalt konsentrasjon i g/L, er forholdet mellom massen av oppløst stoff i et volum av løsningen.
Matematisk uttrykkes den vanlige konsentrasjonen gjennom formelen:
C = m/v
Hvor,
C: vanlig konsentrasjon;
m: masse av oppløst stoff;
V: volum av løsning.
Den mest brukte enheten for vanlig konsentrasjon er g/L, da massen av oppløst stoff beregnes i gram (g) og volumet av løsningen i liter (L).
For eksempel har sjøvann en stor mengde oppløste salter og natriumklorid (NaCl), populært kjent som bordsalt, er en av dem.
Konsentrasjonen av natriumklorid i sjøvann er i gjennomsnitt 2,5 g/L. Så det er 2,5 gram salt, som er det oppløste stoffet, i hver 1 liter sjøvann, som er løsningen.
Hvordan beregne vanlig konsentrasjon?
En løsning er en homogen blanding dannet av et stoff i mindre mengde, kalt oppløst stoff, oppløst i et løsemiddel, som er i større mengde.
Derfor refererer vanlig konsentrasjon til mengden oppløst stoff i et gitt volum av løsningen. Jo mer oppløst stoff som er oppløst i løsningen, jo mer konsentrert er det. Ellers, det vil si at lavt oppløst stoff indikerer at løsningen er fortynnet.
Eksempel 1: Hva er konsentrasjonen i g/L av en løsning av sølvjodid (AgI) som inneholder 2,6 g i 1L løsning?
Når vi får mengden oppløst stoff og volumet av løsningen, kobler vi bare verdiene inn i den vanlige konsentrasjonsformelen for å finne verdien.
Derfor, i en 2,6 g/L løsning av sølvjodid er det 2,6 g oppløst stoff i hver 1 liter løsning.
Eksempel 2: Når man fordamper løsningsmidlet fra 500 mL saltvannsløsning med en konsentrasjon på 6 g/L, hva er massen av løst stoff som oppnås?
Merk at i noen beregninger kan vi finne den vanlige konsentrasjonen beskrevet slik at vi kan beregne massen av oppløst stoff.
Det er også nødvendig å ta hensyn til enhetene. Siden den vanlige konsentrasjonen er gitt i g/L, må vi i dette tilfellet konvertere volumenheten før vi bruker formelen.
Ettersom 1 L inneholder 1000 mL, tilsvarer 500 mL 0,5 L.
Når løsningsmidlet ble fordampet fra løsningen med en konsentrasjon på 6 g/l, ble det således oppnådd 12 g løst stoff.
Få mer kunnskap med innholdet:
- Løsningskonsentrasjon
- molar konsentrasjon
- Fortynning av løsninger
Løste vanlige konsentrasjonsøvelser
Bruk følgende spørsmål for å sjekke kunnskapen som er tilegnet tidligere.
Spørsmål 1
(Unicamp) Løsningsmidlet er fullstendig fordampet fra 250 ml av en vandig løsning av MgCl2 med konsentrasjon 8,0 g/L. Hvor mange gram oppløst stoff oppnås?
a) 8,0
b) 6,0
c) 4,0
d) 2,0
e) 1,0
Riktig alternativ: d) 2.0.
spørsmål 2
Se bildet nedenfor.
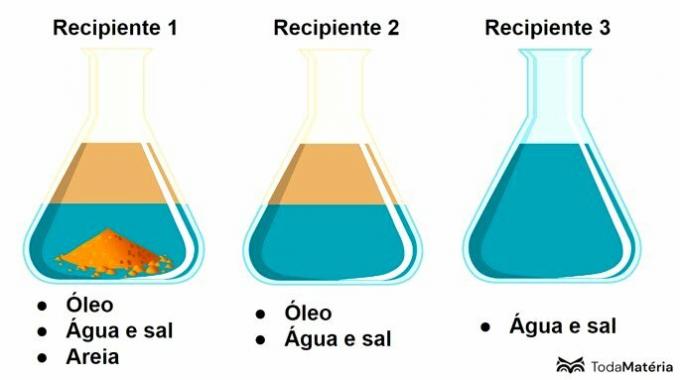
I dette opplegget inneholder beholder 3 en
a) heterogen blanding
b) rent stoff
c) Løsning
d) kolloidblanding
Riktig alternativ: c) Løsning.
Beholder 3 inneholder en løsning, som er en homogen blanding dannet av løst stoff og løsningsmiddel, hvor salt er løst stoff og vann er løsningsmiddel.
Generelt kan vi si at det oppløste stoffet er komponenten i den minste mengden og løsningsmidlet er tilstede i den største mengden.
Beholder 1 presenterer en heterogen blanding med 3 faser og beholder 2 tilsvarer en heterogen blanding av 2 faser.
spørsmål 3
En løsning ble fremstilt ved å oppløse 4,0 g magnesiumklorid MgCl2 til en konsentrasjon på 2,0 g/L. Hvilket volum av løsningen ble tilberedt?
a) 1 L
b) 2 L
c) 4 L
d) 6 L
Riktig alternativ: b) 2 L.
Sjekk ut flere problemer med kommentert oppløsning på vanlige konsentrasjonsøvelser.
Bibliografiske referanser
FONSECA, M. R. M. Kjemi, 1. 1. utg. São Paulo: Attica, 2013.
SANTOS, W.L.P; MOL, G.S. Citizen Chemistry, 1. 2. utg. São Paulo: Editora AJS, 2013.
USBERCO, J. Koble til kjemi, 1. 2. utg. São Paulo: Saraiva, 2014.
- Øvelser om felles konsentrasjon med kommentert tilbakemelding
- kjemiske løsninger
- Løsningsmiddel og løsemiddel: hva de er, forskjeller og eksempler
- Løsningskonsentrasjon
- Løselighet
- Molaritet eller molar konsentrasjon: hva det er, formel og hvordan du beregner
- Fortynning av løsninger
- Øvelser om materiens egenskaper