Molekyl er et sett med atomer, det samme eller forskjellige, forbundet med kovalente bindinger.
Disse kjemiske artene er elektrisk nøytrale og representerer den dannende enheten til et stoff.
Det er enkle molekyler som oksygen (O2) av luften vi puster inn. Imidlertid er det også komplekse forbindelser, som f.eks buckyballs (60 karbonatomer bundet i en kuleform), som er de største molekylene som noensinne er funnet i rommet.
Molekylstudie
Kovalent binding i et molekyl tilsvarer delingselektroner, vanligvis mellom ikke-metalliske elementer.
Se vannmolekylet som et eksempel på en enkel forbindelse.
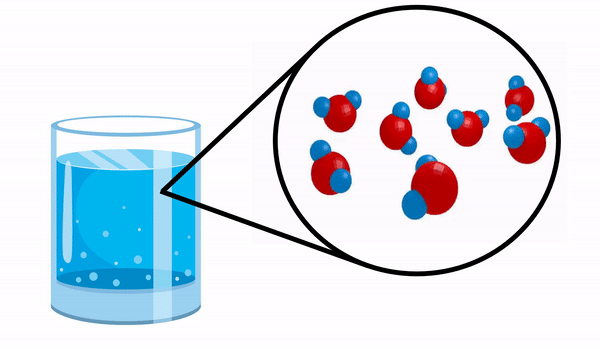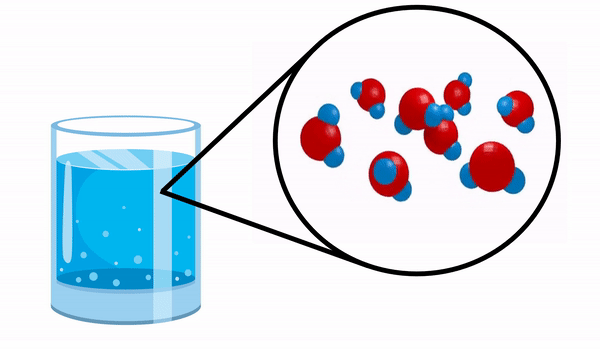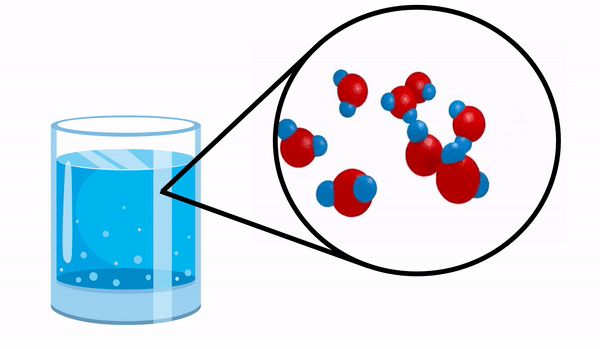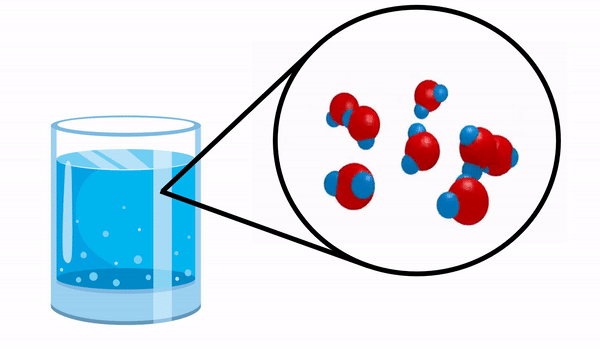
Når vi observerer et glass med Vann vi aner ikke at dette stoffet består av flere H-molekyler2O. Denne formelen indikerer at vann består av 3 atomer: to hydrogen- og ett oksygenatomer, som deler elektroner med hverandre.
Sukker, som vi bruker for å søte juice og lage kaker, består også av molekyler. Dannerenheten av sukker er sukrose.

Dette molekylet er mye mer komplekst, ettersom det er 45
atomer tilkoblet. Den dannes av: 12 karbonatomer, 22 hydrogenatomer og 11 oksygenatomer.Molekyler er strukturer med kjent molekylvekt, men det er også makromolekyler, som er "gigantiske strukturer" dannet av så mange atomer at deres sammensetning til og med er udefinert. Et eksempel på denne typen er diamant, et makromolekyl dannet av mange atomer av karbon i et kovalent nettverk.
Kovalent binding
En kovalent kjemisk binding opprettes mellom to atomer når de deler sine elektroner mer ekstern (av valens). Molekyler kan ha to typer bindinger:
Molekylær kovalent binding: paret elektroner til de to bindingsatomene deles.

Kovalent kovalent binding (dativ): de delte elektronene kommer fra bare ett av atomene som er involvert.
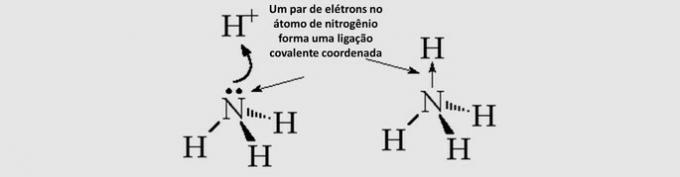
Molekylær geometri
Når et molekyl dannes, plasseres atomene på forskjellige måter, slik at det romlige arrangementet er mer stabilt. Derfor har kompositter forskjellige geometrier.
Her er noen av geometriene som molekyler kan ha.
| Molekylær geometri | ||
|---|---|---|
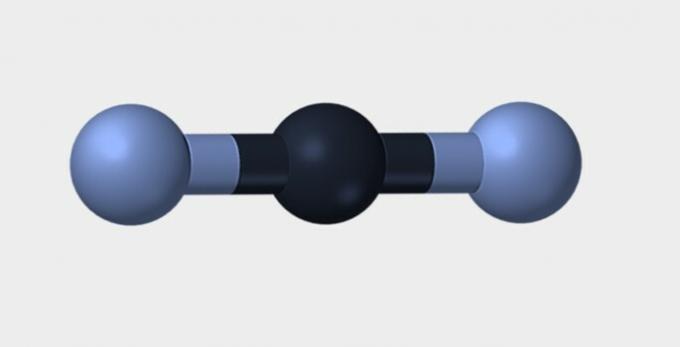
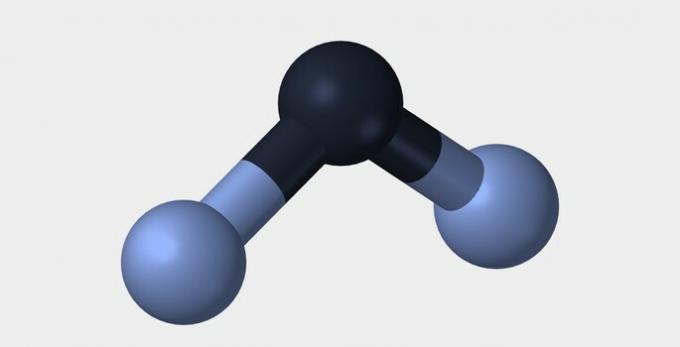
| Lineær | Vinklet | Trekantet |
 |
 |
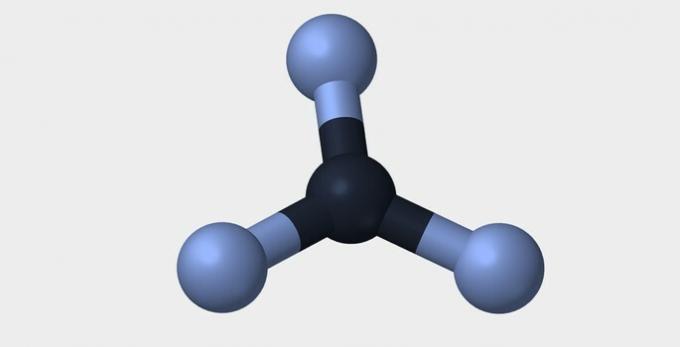 |
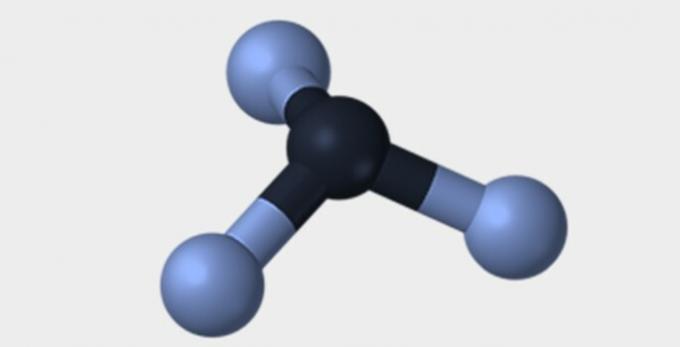
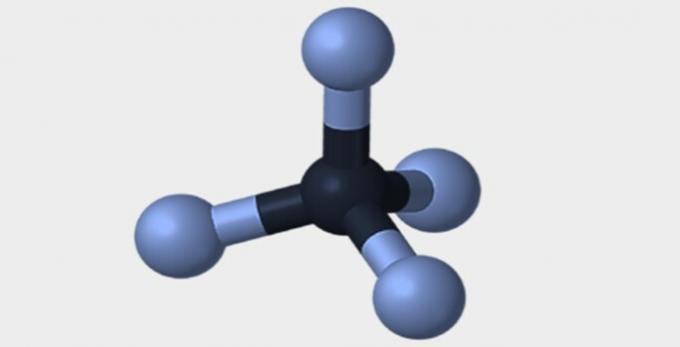
| Pyramidal | tetraeder | oktaedrisk |
 |
 |
 |
Polare og ikke-polære molekyler
Molekyler er klassifisert i henhold til polaritet.
ikke-polare molekyler: det er ingen forskjell i elektronegativitet mellom atomer.
| Nitrogen (N2) | karbondioksid (CO2) |
|---|---|
 |
 |
Nitrogen (N2) er et ikke-polært molekyl fordi det er dannet av det samme kjemisk element og derfor er det ingen forskjell i elektronegativitet. karbondioksid (CO2) er ikke-polær på grunn av sin lineære geometri, som stabiliserer tiltrekningen av oksygen av elektroner.
polare molekyler: det er en forskjell i elektronegativitet mellom atomene, med en positiv pol og en negativ pol.
| Vann (H2O) | Ammoniakk (NH3) |
|---|---|
 |
 |
I begge eksemplene ser vi at de sentrale atomene, oksygen og nitrogen, har uparrede elektronpar som danner elektronskyer. Siden det er flere elektroniske skyer rundt de sentrale atomer enn det er etablerte kjemiske bindinger, er molekylene polare.
Eksempler på molekyler
| Substans | Funksjoner | Molekyl | Formel |
|---|---|---|---|
| Hydrogen | Drivstoff og rikelig i jordskorpen. | 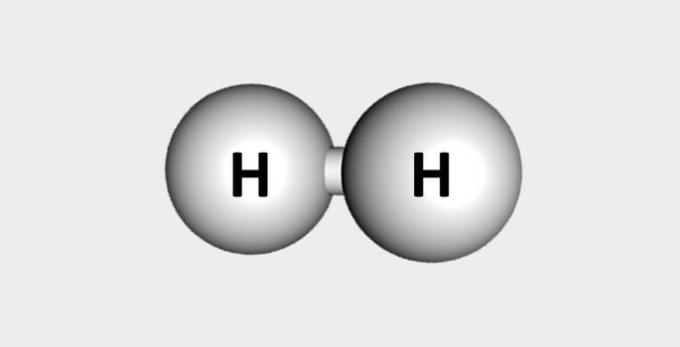 |
H2 |
| Oksygen | Viktig for å puste og deltar i ulike kjemiske reaksjoner | 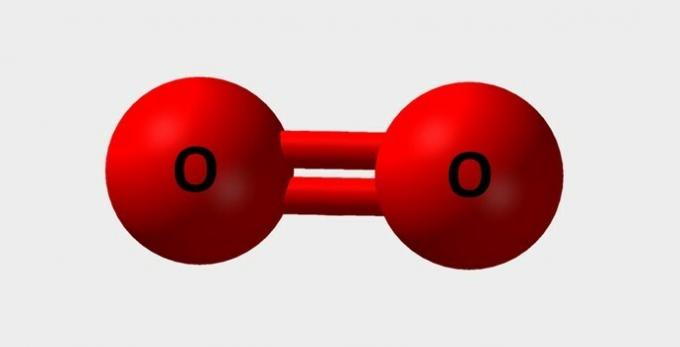 |
O2 |
| Svovel | Gult pulver som brukes til å lage fargestoffer. | 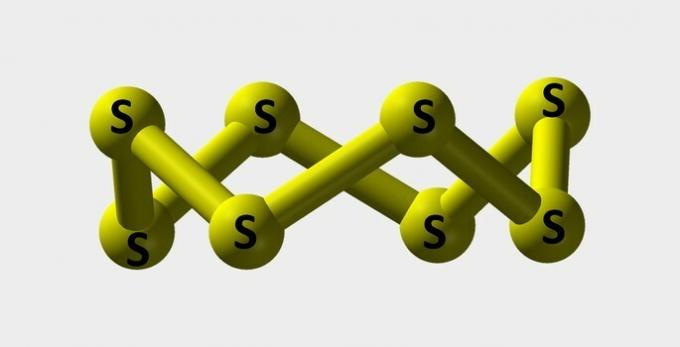 |
s8 |
| Karbondioksid | Brukes i brannslukningsapparater og kjølemedier. | 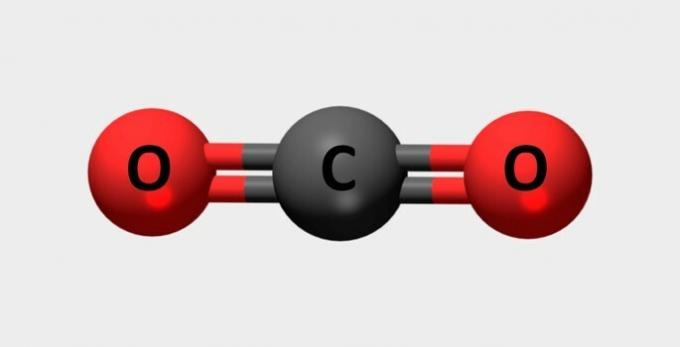 |
CO2 |
| Etanol | Vanlig alkohol brukt som drivstoff og i parfymer. | 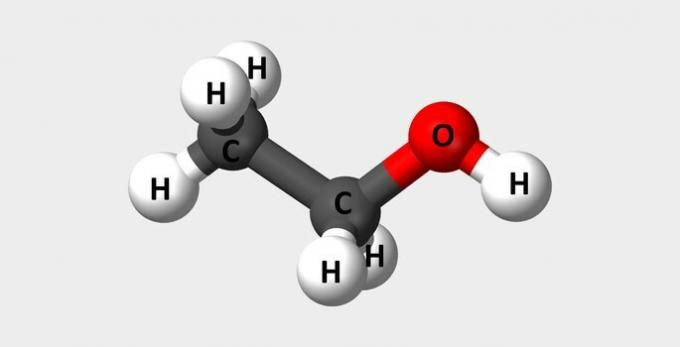 |
Ç2H6O |
Husk å sjekke ut disse tekstene om emner relatert til det du nettopp har lært:
- Biomolekyler
- Organiske forbindelser
- Molekylær masse
- Oktettregel
- Kjemiske bindinger
- Tilkoblingspolaritet
- Intermolekylære styrker