Strukturell formel er skjemaet som indikerer strukturen, det vil si arrangementet av atomene som utgjør de kjemiske elementene, samt forbindelsen mellom dem. Den kan vises på forskjellige måter: flat, kondensert eller elektronisk.
Blant faktorene som betinger strukturene som brukes, er antall elektroner i valensskallet en av dem.
Flat formel
Den flate formelen bruker bindestreker for å representere kovalente bindinger, som kan være enkle, doble eller tredoble og representert på følgende måter:
- enkel tilkobling (når to elektroner deles)
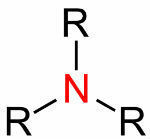
= dobbeltbinding (når 4 elektroner deles)
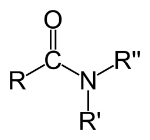
≡ trippel lenke (når 6 elektroner deles)
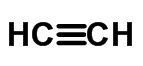
Kondensert eller forenklet formel
I den kondenserte strukturformelen vises ikke bindingene.
I sin representasjon er antall atomer for hvert element angitt på en kondensert måte, det vil si forenklet:
H3C CH2 CH2 CH3
Lineær kondensert formel
Den lineære kondenserte formelen bruker sikksakklinjer, i hvis hjørner karbonene er representert:
Elektronisk eller Lewis-formel
Den elektroniske formelen, også kalt Lewis-formelen, er representert med prikker.
Gjennom disse punktene vises mengdene elektroner som er tilstede i valenslagene:
H: H
Og den molekylære formelen?
DE molekylær formel, uten å referere til dens struktur, angir antall elementer som utgjør a molekyl. I tillegg til å indikere antall atomer som er tilstede i hvert element og deres proporsjoner.
Den kan oppnås gjennom den minimale eller empiriske formelen og prosent- eller centesimalformelen.
Les også Isomerisme og Valencia lag.
Løste øvelser
1. (Vunesp-2000) Skriv strukturformelen og gi det offisielle navnet:
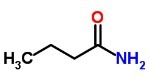
a) et mettet forgrenet karbonkjede keton med totalt 7 karbonatomer.
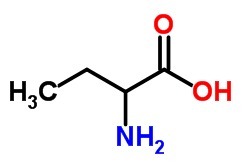
b) en aminosyre, med 4 karbonatomer.
De)

B)
2. (FGV-2005) Aspartam er et kunstig søtningsmiddel som ved et uhell ble oppdaget i 1965 av en uforsiktig kjemiker, som slikket de skitne fingrene og følte at de var søte.
Disse uhygieniske vanene anbefales ikke, da mange stoffer i små mengder er svært giftige.
Strukturformelen for aspartam er vist nedenfor:

Fra strukturformelen til aspartam ser det ut til at det er
a) 13 karbonatomer per molekyl.
b) 1 eter funksjonell gruppe.
c) 1 dipeptid
d) 2 tertiære karbonatomer
e) bare 1 asymmetrisk karbonatom.
Alternativ c: 1 dipeptid
For å fortsette å teste din kunnskap, se også disse øvelseslistene:
- Øvelser på hydrokarboner
- Øvelser om organisk kjemi
- Øvelser på flat isomerisme